Все стероидные гормоны синтезируются из холестерина (рис.22). При этом происходит укорочение или удаление боковой цепи, а также реакции гидроксилирования сиспользованием восстановителей (НАДФН+Н+, аскорбат).
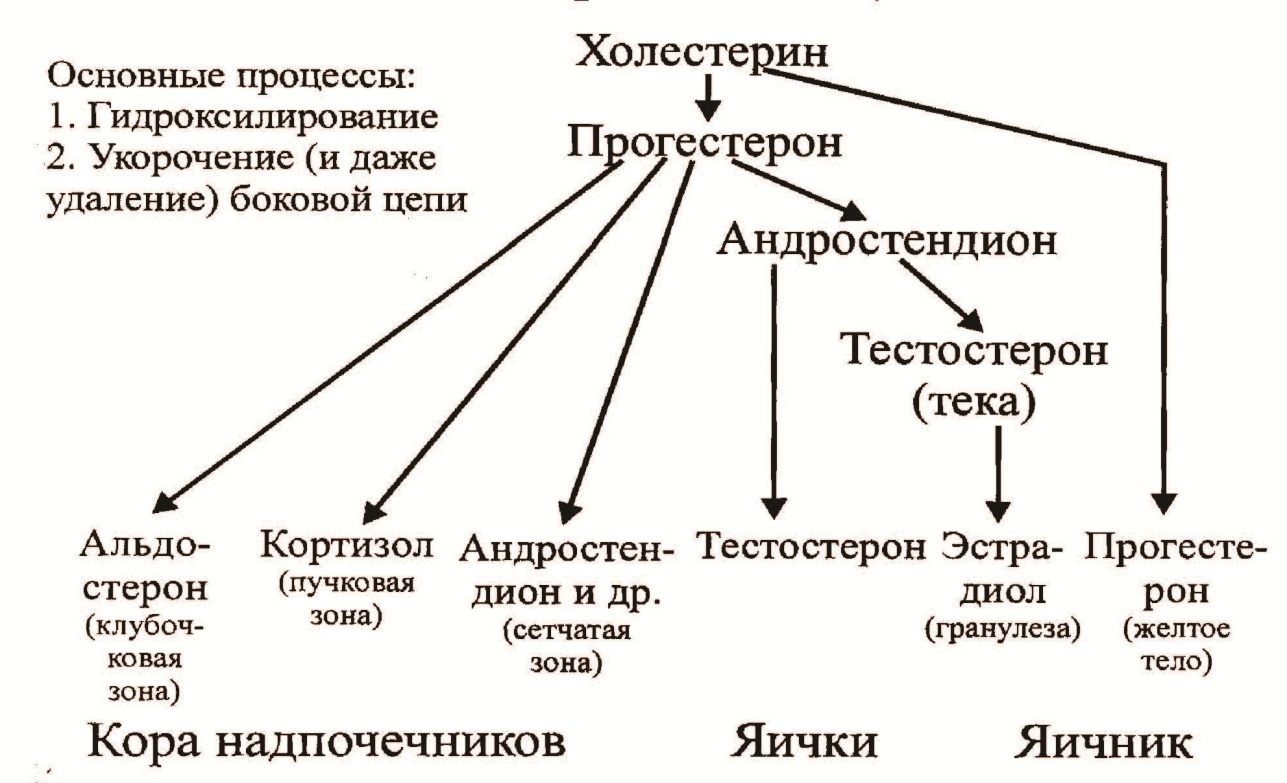
Рис.22. Синтез стероидных гормонов
В процессе стероидогенеза первым синтезируется прогестерон – гормон жёлтого тела. В коре надпочечников и в половых железах прогестерон является предшественником андрогенов. Андрогены – андростендион образуется в сетчатой зоне надпочечников и у мужчин и у женщин. Тестостерон образуется в половых железах мужчин. У женщин тестостерон является промежуточным метаболитом при синтезе эстрогенов. Из эстрогенов наиболее активен эстрадиол. Стероидные гормоны кровью транспортируются в комплексе со специфическими транспортными белками. Основной механизм действия стероидов через рецепторы гиалоплазмы – это гормонозависимые транскрипционные факторы. Комплекс гормон-рецептор поступает в ядро, связывается с регуляторными участками ДНК, изменяя экспрессию генов.
Андрогены сетчатой зоны. Сетчатая зона коры надпочечников находится на границе с мозговым веществом (рис.23). Андрогены сетчатой зоны имеют отношение к формированию агрессивного, доминантного поведения, вызывают анаболические эффекты, особенно в мышцах. Их биохимическая функция состоит в увеличении синтеза нуклеиновых кислот и белков в тканях. Они способствуют заживлению ран. На основе андрогенов получены синтетические анаболические стероиды (ретаболил, нераболил), у которых снижено андрогенное действие и более выражены анаболические эффекты, например у тестостерона соотношение анаболической и андрогенной активности 1:1, а у современных анаболических стероидов 20:1. Их назначают после тяжелых травм, операций, тяжёлых ожогов, при инфаркте миокарда на стадии репарации, при язвенной болезни, истощении. Анаболические стероиды являются допинговыми препаратами, использование в спорте запрещено. И в медицине их длительный приём может вызывать повреждение печени, сердечно-сосудистой системы, изъязвления слизистых, импотенцию.
Регуляция пучковой и сетчатой зоны. Пучковая зона (в меньшей степени сетчатая) контролируется системой гипоталамус – гипофиз – кора надпочечников. В гипоталамусе вырабатывается кортиколиберин. Кортиколиберин вырабатывается в ответ на стрессовые факторы: травма, инфекция, кровотечение, гипогликемия и др. Кортиколиберин в 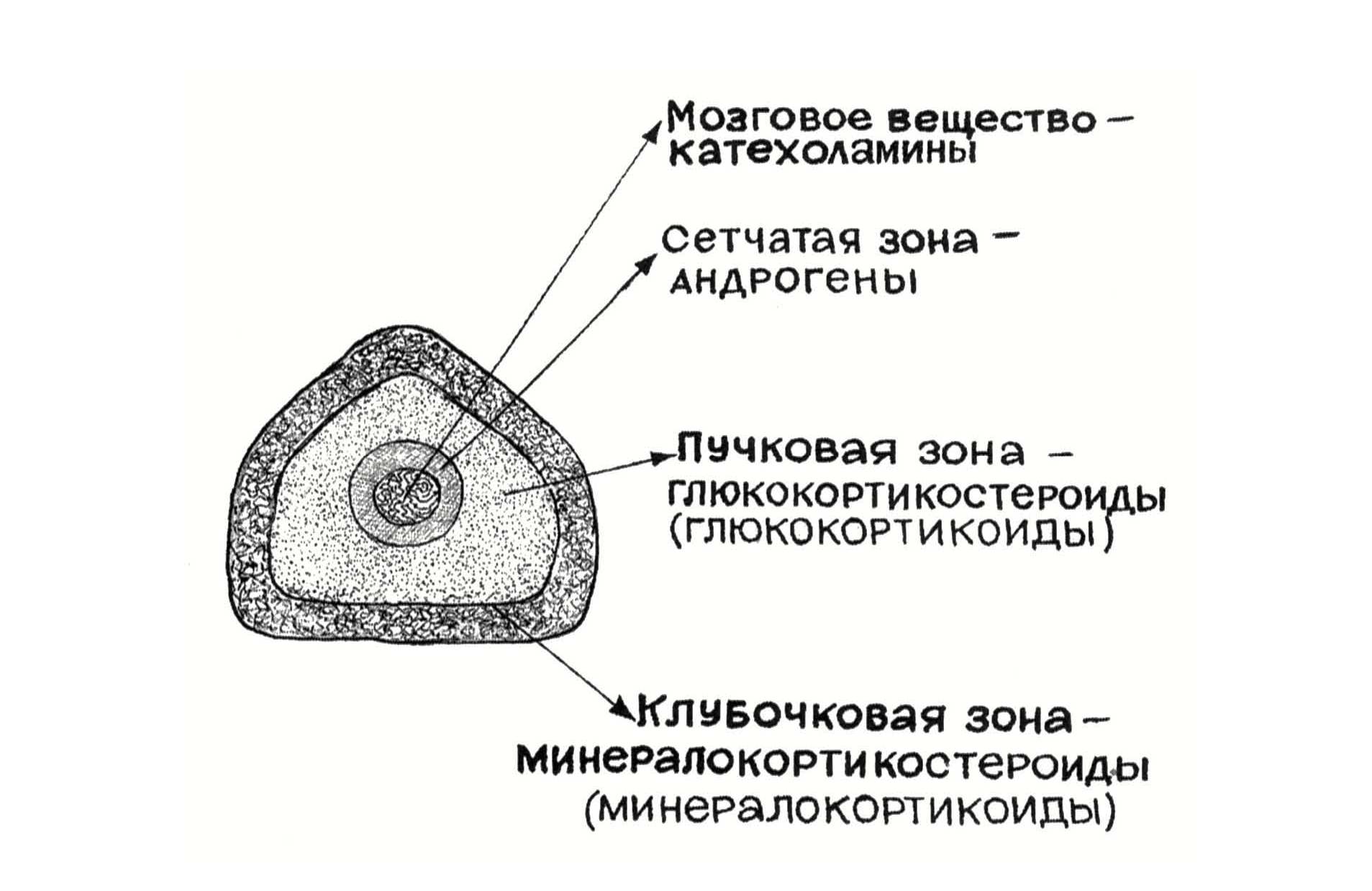
Рис.23. Надпочечник и его гормоны
аденогипофизе вызывает образование и секрецию в кровь кортикотропина (АКТГ). Кортикотропин действует на пучковую и в меньшей степени на сетчатую зоны коры надпочечников. В пучковой зоне вырабатываются глюкокортикостероиды (ГКС). ГКС (кортизол) по механизму отрицательной обратной связи тормозит секрецию АКТГ гипофизом и кортиколиберина гипоталамусом.
Глюкокортикостероиды: основные метаболические и функциональные эффекты. ГКС – это гормоны широкого действия, влияют на все виды обменов: углеводный, липидный, белковый, минеральный, процессы воспаления и иммунитета и т.д. ГКС индуцируют синтез ключевых ферментов глюконеогенеза и повышают уровень глюкозы крови. Глюкоза крови повышается и потому, что снижается утилизация глюкозы (гликолиз, пентозофосфатный путь, синтез гликогена). Существует неправильный термин «стероидный диабет». ГКС увеличивают катаболизм белков (аминокислоты нужны для глюконеогенеза), индуцируют синтез аминотрансфераз. ГКС индуцируют синтез белков острой фазы при любом воспалении. В легких ГКС индуцируют синтез сурфактанта. Для предупреждения респираторного дистресс-синдрома (особенно у недоношенных детей) применяют ГКС с целью индукции сурфактанта. В жировом обмене эффект ГКС – увеличен липолиз в конечностях, а синтез жира увеличен на лице, шее и туловище. Слабее, чем минералокортикоиды влияют на минеральный обмен (увеличивают реабсорбцию натрия и воды). Оказывают пермессивное действие на катехоламины и глюкагон, т.е. оптимизируют их эффекты. ГКС снижают освобождение гистамина, репрессируют синтез эйкозаноидов, цитокинов, NO●, молекул клеточной адгезии. ГКС репрессируют синтез проопиомеланокортина.
ГКС, как и катехоламины увеличивают работоспособность мышц. ГКС увеличивают секрецию желудочного и кишечного соков, увеличивают прочность и снижают проницаемость сосудов. Это очень важно при стрессе, так как катехоламины при их избытке или длительном действии повреждают стенки мелких сосудов, способствуют переходу шока в необратимую фазу. Поэтому ГКС увеличивают устойчивость к стрессу, обладают противошоковым и антитоксическим действием. Очень важный для медицины эффект ГКС – их противовоспалительное действие, очень сильное и генерализованное. Противовоспалительное действие обусловлено: снижением синтеза и увеличением катаболизма белков в лимфоидной ткани, снижением освобождения гистамина и кининов, репрессией синтеза эйкозаноидов, цитокинов, NO●, молекул клеточной адгезии, провоспалительных транскрипционных факторов. А также увеличением прочности и снижением проницаемости сосудов, снижением миграции и активности макрофагов, натуральных киллеров (лимфоцитов врожденного иммунитета, обладающих цитотоксичностью “без предварительной подготовки”), тучных клеток. ГКС вызывают апоптоз лимфоцитов и макрофагов, но снижают апоптоз других клеток.
ГКС назначают при лечении бронхиальной астмы, ревматизма, для подавления иммунитета при пересадке органов и аутоиммунных заболеваниях, при тяжёлых аллергиях, вводят при шоке. Обычно применяют синтетические агонисты рецепторов ГКС (преднизолон, дексаметазон, флютиказон). Они эффективнее кортизола, так как труднее метаболизируются и почти не влияют на водно-солевой обмен, т.е. меньше побочных эффектов.Необходимо помнить, что ГКС очень сильные лекарства и лёгкое воспаление лечить препаратами ГКС не нужно. Существуют другие противовоспалительные средства. Кроме того, всегда, если возможно, ГКС следует применять локально (в мазях, ингаляциях, вводить не в кровь, а в полость сустава). Длительное лечение большими дозами, а не по строгим схемам, может вызывать осложнения: изъязвления слизистой ЖКТ, так как увеличивается секреция соляной кислоты, снижается синтез простагландинов с цитопротекторным действием. Из-за снижения иммунитета происходит генерализация некоторых заболеваний (туберкулёз). Появляются симптомы кушингизма. Синдром Кушинга (болезнь Иценко-Кушинга, гиперкортицизм) – это эндокринное заболевание, которое может возникать при опухолях гипоталамуса, гипофиза, надпочечников или при нарушениях отрицательной обратной связи. Клинические проявления: снижение толерантности к глюкозе, гипергликемия, гипертония, мышечная слабость, истончение кожи. Возникает специфическое ожирение, с отложением жира на лице, шее, животе. Может появиться гирсутизм – рост волос по мужскому типу у женщин.
Частой причиной гипофункции коры надпочечников является подавление звена гипофиз – надпочечник глюкокортикостероидами, назначаемыми в терапевтических целях. Гипокортицизм возникает в результате резкой отмены ГКС или не назначения увеличенных доз стероидов во время стресса при операции, инфекции, травме. Болезнь Аддисона (бронзовая болезнь) возникает при туберкулёзе надпочечников, аутоиммунном повреждении, кровоизлиянии в надпочечник. При гипокортицизме увеличивается пигментация кожи из-за усиленной продукции проопиомеланокортина, снижается давление, слабость, утомляемость, непереносимость стресса. В крови снижается уровень глюкозы, натрия. Отменять ГКС необходимо, постепенно снижая дозу, так как восстановление секреции собственных гормонов происходит очень медленно.
Метаболиты стероидных гормонов. Метаболизм стероидов происходит в печени. Метаболиты в виде конъюгатов выводятся с мочой. Метаболиты андрогенов – 17-кетостероиды у женщин отражают работу сетчатой зоны, у мужчин на 1/3 – сетчатой зоны, на 2/3 – семенников. Метаболиты ГКС – 17-оксикортикостероиды, по их количеству судят об активности пучковой зоны. Определение 17-кетостероидов и 17-оксикортикостероидов в крови и моче помогает в диагностике эндокринных и некоторых других заболеваний.
 2015-04-08
2015-04-08 2242
2242








