Степень диссоциации электролитов зависит от природы электролита, температуры и концентрации раствора. Для слабых бинарных электролитов зависимость от концентрации подчиняется закону разбавления Оствальда:
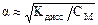 ,
,
то есть, чем более разбавлен раствор, тем больше степень диссоциации и, соответственно, больше электропроводность раствора. Для подтверждения этой зависимости провести следующий опыт.
Выполнение опыта. В стакан налить вначале ледяную (концентрированную) уксусную кислоту, отметить отсутствие тока в системе. Затем прибавлять постепенно воду и наблюдать отклонение стрелки прибора.
Опыт повторить с серной кислотой, для чего в четыре стакана налить одинаковые примерно до половины объемы растворов серной кислоты различной концентрации: в первый – концентрированный, во второй – разбавленный водой в 25, в третий – в 50, в четвертый – в 250 раз. Собрать установку, состоящую из источника тока (2 - 4 В), амперметра (3 - 5 А) и угольных электродов (рис. 6). По очереди определить электропроводность всех четырех растворов, начиная с наиболее разбавленного.
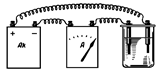 |
Рис. Установка для сравнения электропроводности растворов
Записать результаты опыта в виде таблицы:
| Степень разбавления раствора серной кислоты | показания амперметра, А | Выводы |
| Без разбавления | ||
| 1:25 | ||
| 1:50 | ||
| 1:250 |
Построить график зависимости электропроводности раствора от концентрации раствора.
 2015-04-01
2015-04-01 733
733








