Лицензия – специальное разрешение на осуществление конкретного вида деятельности при соблюдении лицензионных требований и условий, выданное лицензирующим органом юридическому лицу или индивидуальному предпринимателю.
Законодательной основой лицензирования в РФ является Федеральный закон от 08.08.01 г. № 128 «О лицензировании отдельных видов деятельности».
Основными принципами лицензирования являются:
· обеспечение единства экономического пространства на территории РФ;
· установление единого перечня лицензируемых видов деятельности и порядка лицензирования на территории РФ;
· закрепление лицензионных требований и условий в положениях и лицензировании конкретных видов деятельности;
· гласность и открытость;
· соблюдение законности.
Минздрав России осуществляет лицензирование деятельности (с 06.04.04 г. Министерство здравоохранения и социального развития):
· фармацевтической (предприятиями торговли и аптечными организациями);
· связанной с оборотом наркотических средств и психотропных веществ, внесенных в Списки II и III в соответствии с Федеральным законом «О наркотических средствах и психотропных веществах»;
Лицензирующие органы, помимо осуществления мероприятий лицензирования, имеют полномочия по ведению реестра лицензий, в котором указываются наименование и организационно-правовая форма лицензии, лицензируемая деятельность (с перечислением выполняемых работ), код по Общероссийскому классификатору предприятий и организаций (ОКПО), идентификационный номер налогоплательщика (ИНН), номер свидетельства о государственной регистрации в качестве юридического лица, место его нахождения, дата принятия решения о предоставления лицензии, ее номер и срок действия, сведения о продлении срока действия лицензии, переоформлении, основания даты приостановления, возобновления или аннулирования лицензии.
Положения о лицензировании:
· дятельности по культивированию растений, используемых для производства наркотических средств и психотропных веществ (от 14.06.03 г. № 432);
· дятельности, связанной с оборотом наркотических и психотропных веществ (от 21.06.02 г. № 454);
· фрмацевтической деятельности (от 01.07.02 г. № 489);
· поизводства лекарственных средств (от 04.07.02 г. № 500);
· поизводство медицинской техники (от 16.08.02 г. № 612).
Правовой основой проведения лицензирующим органом экспертной проверки субъекта, осуществляющего деятельность по отдельным направлениям обращения ЛС на территории РФ, являются отдельные пункты соответствующих Положений о лицензировании, в которых говорится, что «лицензирующий орган при проведении лицензирования имеет право на проверку соответствия соискателя лицензии требованиям и условиям».
Требования рационального менеджмента, направленные на максимально эффективное использование ограниченных ресурсов лицензирующего органа:
· формализации процедуры проведения проверки;
· стандартизация требований и условий осуществления фармацевтической деятельности;
· документальное оформления процедуры проверки;
· формирование команды экспертов.
Экспертные проверки можно разделить:
- проверки, проводимые при первичном лицензировании;
- плановые;
- внеплановые;
- проверки соблюдения правил обращения наркотических средств и психотропных веществ.
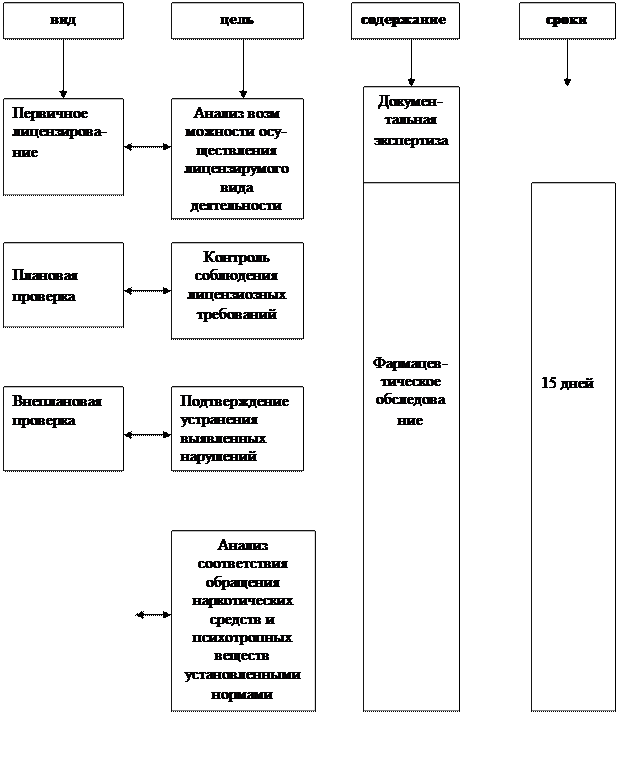
Главной целью экспертной проверки при первичном лицензировании является анализ возможности осуществления соискателем лицензии деятельности в определенной области сферы обращения ЛС.
Документальная проверка проводится юристом и включает:
1. проверку наличия документов:
- заявления;
- копии учредительных документов и свидетельства о государственной регистрации;
- копию свидетельства о постановке на учет в налоговом органе;
- документ, подтверждающий уплату лицензионного сбора за рассмотрение заявления о предоставлении лицензии;
- сертификат специалиста, подтверждающий соответствие профессиональной подготовки руководителя юридического лица и руководителя соответствующих подразделений лицензируемой деятельности;
- документы, подтверждающие право соискателя на использование помещений для осуществления лицензируемой деятельности;
- копии документов, подтверждающие получение работниками соискателя высшего или среднего фармацевтического образования;
- копию выданного в установленном порядке санитарно-эпидемиологического заключения о соответствии помещений предъявляемым требованиям.
2. сопоставление содержания и оформления представленных документов требованиям регламента;
3. составлении описи принятых документов и выдачи копии соискателю лицензии с указанием даты приема документов (срок начала экспертной проверки);
Плановые проверки проводятся с целью контроля соблюдения лицензиатом лицензионных требований и проводятся не чаще 1 раза в 2 года и их продолжительность не должна превышать 15 дней.
Внеплановые проверки осуществляют для подтверждения устранения лицензиатом выявленных при проведении плановой проверки нарушений и требований и условий осуществления фармацевтической деятельности.
Проверки соблюдения правил обращения наркотических и психотропных веществ предусматривают в качестве основной целевой задачи анализ соответствия обращения наркотических и психотропных веществ установленным правилам.

Результаты инвентаризации объектов оформляются в «Акте фармацевтического обслуживания».
Характеристика основных видов экспертной проверки:
|
|
Целью лицензирования фармацевтической деятельности является повышения качества обслуживания населения, создание барьеров для проникновения на фармацевтический рынок недоброкачественной продукции, которая может нанести ущерб здоровью граждан.
 2015-04-17
2015-04-17 4427
4427