| n | l | ml | ms |
| ±1/2 | |||
| 0, 1 | 0; 1, 0, –1 | ±1/2 | |
| 0, 1, 2 | 0; 1, 0, –1; 2, 1, 0, –1, –2 | ±1/2 | |
| 0, 1, 2, 3 | 0; 1, 0, –1; 2, 1, 0, –1, –2; 3, 2, 1, 0, –1, –2, –3 | ±1/2 |
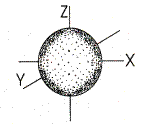
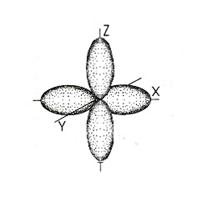
| Форма s-электронной орбитали | Форма d-электронной орбитали | |||
| 
| |||
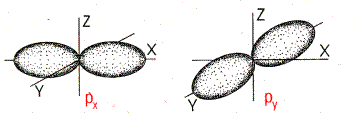
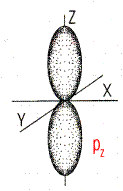
| Форма и ориентация p-электронных орбиталей | ||||
| ||||
Пространство вокруг ядра, в котором наиболее вероятно нахождение электрона, называется орбиталью.
Совокупность электронов с одинаковым квантовым числом n называется электронным слоем или уровнем. Электроны, которые движутся в орбиталях близкого размера и образуют энергетические уровни. Они номеруются от ядра 1;2;3;4;5;6;7.
Энергетические уровни подразделяются на подуровни, которые отличаются друг от друга энергией связи с ядром. Совокупность электронов с одинаковыми значениями n и 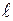 образуют подуровень.
Число подуровней равно n, но не более 4–х. образуют подуровень.
Число подуровней равно n, но не более 4–х.
|
| Подуровни состоят из орбиталей: s– первый подуровень состоит из одной s- орбитали; p – второй подуровень состоит из трёх p-орбиталей; d– третий подуровень состоит из пяти d-орбиталей; f – четвёртый подуровень состоит из семи f-орбиталей. |
 2015-04-01
2015-04-01 570
570