Рассмотрим идеальную газовую неравновесную систему, в которой идет химическая реакция:
а А + b В = с С + d D.
Начальные неравновесные парциальные давления p'A, p'B, p'C, p'D отличаются от равновесных парциальных давлений без штрихового индекса pA, pB, pC, pD.
Опустим вывод уравнения изотермы химической и приведем только конечное уравнение:
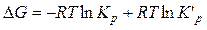 (48)
(48)
Здесь
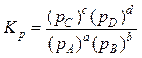
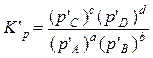
Иногда величину К’p называют «константой неравновесия» по аналогии с константой равновесия Кp,т.к. она тоже выражается через парциальные давления, однако, неравновесные.
Введем понятие стандартных условий: пусть начальные неравновесные давления компонентов реакции равны 1 атм: p'A = p'B = p'C = p'D = 1 атм. В таких стандартных условиях уравнение (48) определяет стандартное изменение энергии Гиббса - DG0:
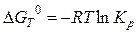 (48’)
(48’)
С учетом (48’) уравнение (48) запишется в таком виде:
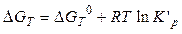 (48’’)
(48’’)
Аналогичные выражения можно получить для Кc, КХ, Кf и Ка для гетерогенных равновесий и равновесий в растворах. Так, для V = const и Т = const уравнение изотермы химической реакции запишется следующим образом:
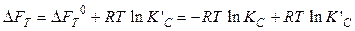
Здесь K’C – «константа неравновесия», выраженная через неравновесные концентрации С’ исходных веществ и продуктов:
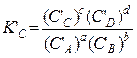
Чем больше 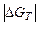 или
или 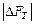 , тем дальше система от равновесия.
, тем дальше система от равновесия.
Будем для определенности анализировать уравнение изотермы химической реакции для изобарно-изотермических условий (48).
Для состояния равновесия Δ GТ = 0 и КР = К’p. Величина Δ GТ является мерой отклонения системы от равновесия.
По знаку Δ GТ в уравнении (48) можно судить о направлении химического превращения в неравновесной смеси реагентов и продуктов:
Если Δ GТ < 0, то реакция возможна в прямом направлении от реагентов к продуктам. Это значит, что К ’ р < Kр и, следовательно, чтобы К’р росло и приближалось к равновесному значению Кр, должен расти числитель, т.е. концентрации продуктов реакции.
Если Δ G > 0 – реакция возможна в обратном направлении.
Отметим разный физический смысл очень близких по написанию выражений:
Δ GТ < 0 (a)
Δ G Т 0 < 0 (b)
а также
Δ GТ > 0 (c)
Δ GТ 0 > 0 (d)
Выражение (a) означает, что реакция в системе протекает в сторону образования продуктов при данной температуре и соответствующих неравновесных давлениях (концентрациях) компонент.
Выражение (б) означает, что при данной температуре константа равновесия больше единицы. При этом в стандартных условиях (при исходных неравновесных давлениях, равных единице) процесс пойдет в сторону образования продуктов. Однако, в принципе, варьируя неравновесные давления (концентрации) веществ, процесс можно направить в любую сторону.
Выражение (с) означает, что реакция в системе протекает в сторону образования исходных веществ при данной температуре и соответствующих неравновесных давлениях (концентрациях) компонент.
Выражение (в) означает, что при данной температуре константа равновесия меньше единицы. Процесс также можно направить в любую сторону, варьируя неравновесные давления (концентрации) веществ.
Дальнейший анализ уравнения изотермы химической реакции позволяет сделать некоторые выводы:
1) Так как Δ GТ зависят от неравновесных давлений (концентраций), то можно всегда подобрать такую смесь, чтобы реакция прошла в нужном направлении.
2) Изменить знак Δ GТ можно, изменяя температуру, так как Кр (см. следующий раздел) и, следовательно, Δ GТ 0 зависят от температуры.
3) Если в исходной неравновесной смеси все газы находятся при стандартных давлениях 1 атм, то в случае Δ GТ 0 < 0 реакция пойдёт в сторону образования продуктов.
4) Скорость процесса перехода к равновесию не зависит от абсолютного значения Δ GТ в большинстве случаев, а определяется кинетическими характеристиками системы.
5) Из условия Δ GТ 0= 0 и известного уравнения Δ GТ 0= Δ НT 0 -Т Δ ST 0, можно найти температуру Т = Δ H 0 T/ Δ S 0 T, при которой в равновесии будут находиться газообразные участники реакции в стандартном состоянии (парциальные давления каждого равны 1 атм.).
Следует отметить, что знак «0» в уравнениях (48’-48’’) не указывает на стандартную температуру (а только на равенство единице неравновесных парциальных давлений), и данные уравнения применяются для всех температур.
 2015-04-01
2015-04-01 1509
1509
