Одним из эффективных методов очистки хромовых сточных вод является реагентный метод, основанный на применении химического реагента. В качестве восстановителей используются Na2SO3, SO2, FeSO4 и др.
1. Напишем уравнение реакции восстановления бихромата калия сульфитом натрия с учетом того, что полное восстановление Cr(VI) происходит в сильнокислой среде:
K2Cr2O7 + 3Na2SO3 + 4H2SO4 = Cr2(SO4)3 + 3Na2SO4 + K2SO4 + 4H2O.
2. Определим, сколько молей K2Cr2O7 содержится в 1,5 м3 (или 1500 л) электролита:
1,5 моля K2Cr2O7 содержится в 1 л раствора
Х молей –«– –«– –«– –«– в 1500 л –«–
Х = 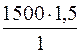 = 2250 молей;
= 2250 молей;
3. Из уравнения реакции видно, что на восстановление 1 моля K2Cr2O7 требуется 3 моля Na2SO3, а на восстановление 2250 молей K2Cr2O7 потребуется 2250×3 = = 6750 молей Na2SO3, что составляет 6750×126 г = 850500 г = 850,5 кг.
Пример 3.4. При электролизе сточной воды объемом 1,5 м3 в течение 2 час получено 5 кг металлического никеля. Определите силу тока, прошедшего через раствор. Выход по току 80 %.
 2015-04-06
2015-04-06 1569
1569








