Реакциями сульфирования называют химические процессы, в результате которых в органическую молекулу вводятся соответственно сульфокислотная группа —SО2ОН или ее производные (—SО2С1,
—SО2ОNа).
Функциональные группы связываются непосредственно с атомом углерода, что отличает рассматриваемые реакции от процессов образования соответствующих сложных эфиров, в которых эти группы связаны с углеродом через атом кислорода.
Скорость процесса сульфирования, глубина, состав и выход продуктов зависят от структуры исходного соединения, условий проведения процесса и сульфирующего агента.
Реакции сульфирования протекают с выделением тепла. Теплота реакции зависит от природы сульфирующего агента и сульфируемого соединения. Обычно для оценки теплоты реакции в качестве эталона используют теплоту сульфирования исследуемого соединения в паровой фазе триоксидом серы. Большую часть промышленных процессов осуществляют без катализаторов, но известен ряд реакций сульфирования, где катализаторы используют. В качестве катализаторов можно использовать также медь, натрий, бихромат калия, ванадат аммония, йод, которые избирательно изменяют скорость образования какого-либо изомера.
В качестве сульфирующих агентов ароматическах углеводородов применяют:
1.концентрированную серную кислоту:  Менее энергична чем другие агенты, так как при взаимодействии с ароматическими веществами выделяется вода, тормозящая процесс сульфирования. По этой причине при сульфировании серной кислотой обычно необходима повышенная температура (80—100°С и выше). Реакция обратима.
Менее энергична чем другие агенты, так как при взаимодействии с ароматическими веществами выделяется вода, тормозящая процесс сульфирования. По этой причине при сульфировании серной кислотой обычно необходима повышенная температура (80—100°С и выше). Реакция обратима.
2.олеум:  - сильный сульфирующий агентом, активность которого возрастает с повышением концентрации избыточного серного ангидрида. Активен при комнатной температуре. Реакция обратима.
- сильный сульфирующий агентом, активность которого возрастает с повышением концентрации избыточного серного ангидрида. Активен при комнатной температуре. Реакция обратима.
3.серный ангидрид:  ; Активен при комнатной температуре. Практически эта реакция необратима.
; Активен при комнатной температуре. Практически эта реакция необратима.
Реакция сульфирования ароматических соединений относится к процессу электрофильного замещения в ароматическом ядре. Агентом непосредственно атакующим ароматическое ядро являются
--ион S+O2OH, тогда: 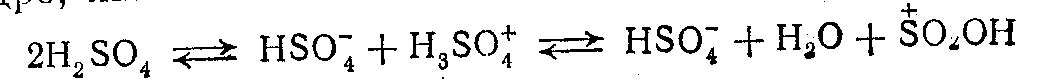
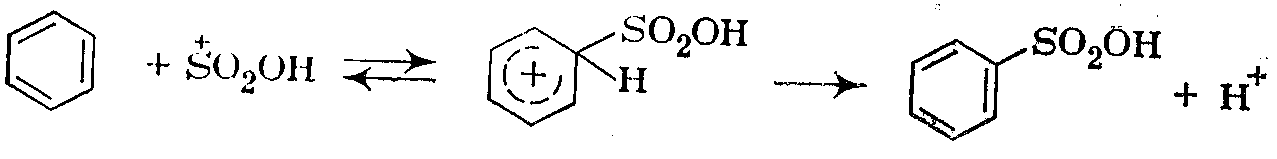
--молекула серного ангидрида:
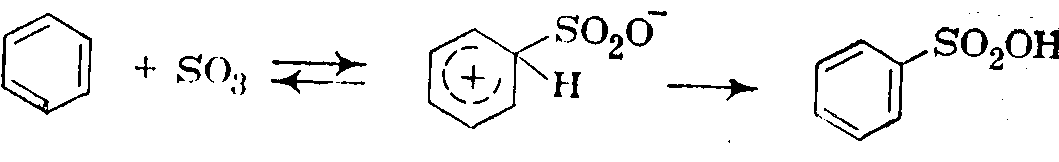
Побочными реакциями при сульфировании аренов являются:
1.Образоваие ди- и трисульфопроиводных: Как и другие реакции замещения в ароматическом ядре, сульфирование представляет собой последовательно-параллельный процесс, при котором можно ввести одну за другой две или более сульфогруппы:
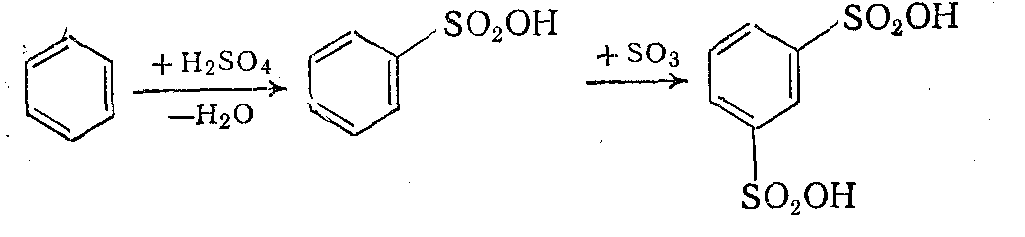
Вторая стадия протекает много медленнее первой и требует более жестких условий. Поэтому при получении моносульфокислот побочное образование дизамещенного продукта обычно незначительно, однако с ним приходится считаться при использовании активных сульфирующих агентов — серного ангидрида и олеума.
2. Образование сульфонов: 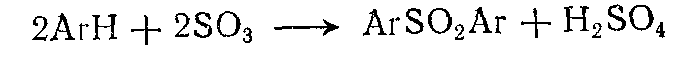 ; Эта реакция ограничивает применение олеума при сульфировании бензола, но для алкилбензолов она наблюдается в незначительной степени. долю ее можно снизить, изменив порядок смешения реагентов (прибавлять ароматическое соединение к избытку сульфирующего агента, а не наоборот).
; Эта реакция ограничивает применение олеума при сульфировании бензола, но для алкилбензолов она наблюдается в незначительной степени. долю ее можно снизить, изменив порядок смешения реагентов (прибавлять ароматическое соединение к избытку сульфирующего агента, а не наоборот).
3.Образование ангидридов сульфокислот: 
4.Окисления, отщепления алкильных групп и др.,
5. Гидролиз (или десульфирование) – процесс обратный сульфированию, является кислотно-каталитической реакцией:

Скорость ее возрастает с увеличением концентрации кислоты. Установлено, что при повышении температуры на 10°С скорость гидролиза возрастает в 2,5—3,5 раза. Скорость десульфирования зависит также от природы заместителя в молекуле арилсульфокислот. Изучение кинетики показало, что при определенных условиях скорость десульфирования не зависит от концентрации сульфокислоты и природы аниона неорганической кислоты; она пропорциональна активности ионов водорода в растворе.
Образование побочных продуктов можно также уменьшить, понижая температуру, применяя растворители и т. д. Следовательно, необходимость предотвращения побочных реакций обязательно нужно учитывать при выборе условий реакции..
Сульфопроизводные высших углеводородов служат исходным сырьем для получения красителей поверхностно-активных веществ (ПАВ) и синтетических моющих средств (СМС) и т. д. Алкиларилсульфонаты — твердые кристаллические вещества. Когда алкильная цепь разветвлена, они хорошо растворяются в воде; спрямление и удлинение алкильной цепи ведет к снижению растворимости. в воде и спиртах. Они почти бесцветны и не имеют запаха. Их применяют при изготовлении моющих композиций для стирки одежды и тканей, для мойки посуды, различной тары и шерсти, для отбеливания химических волокон и др.
Олефины значительно легко подвергаются сульфированию. Производные продукты сульфирования олефинов служат исходным сырьём для получения поверхвостно-активных веществ.
В качестве сульфирующих агентов олефинов применяют:
1. Оксид серы VI, реагирует с олефинами с образованим карбилсульфата:
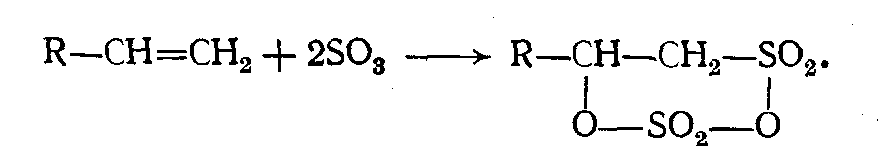
При гидролизе образующихся сульфатов получают α-окси- алкилсульфокислоты:
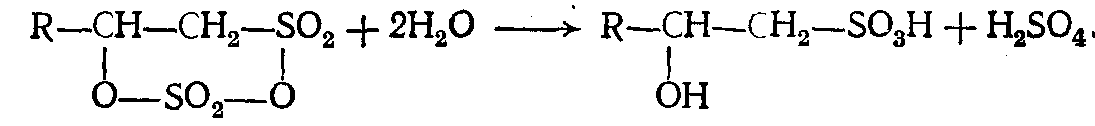
2. 98%-ная серная кислота, в основном для высших углеводородов:
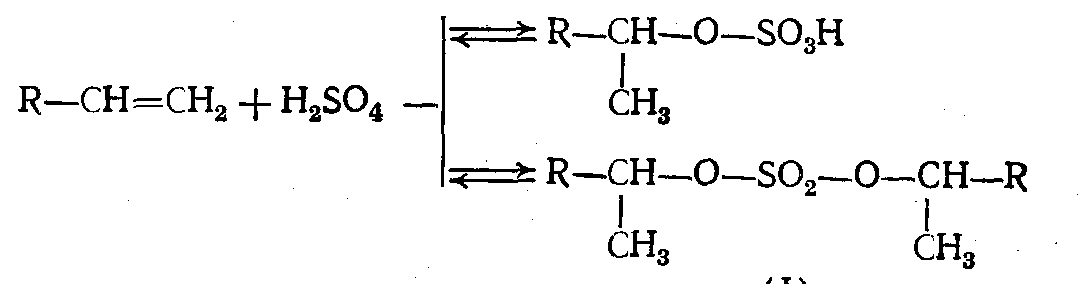
Механизм реакции сульфирования олефинов также ионный: H2SO4↔H++ HSO4;
R – CH=CH2+ H+→ R – C+H – CH3 + HSO4−→R – CH(CH3) – O – SO3H
R – CH(CH3)– O – SO3−+ R – C+H – CH3→ R – CH(CH3) – O – SO2 – O – CHR – CH3
Побочные реакции процесса следующие:
1. образования полимеров, чтобы избежать этого процесс необходимо проводить в мягких условиях (особенно е отношении температуры, концентрации серной кислоты и продолжительности реакции). Обычно сульфирование проводят при температуре от +5 До —15 С (в зависимости от температуры плавления исходного углеводорода), в растворителе — н-пентане (соотношение пентан: олефин= 1: 1) при мольном соотношении Н2SO4 : олефин= 1,5: 1,0.
2. гидролиз продуктов,
3. окисление углеводородов до продуктов полного и неполного окисления.
Парафины нормального строения и циклопарафины (содержащие более пяти атомов углерода в цикле) практически не реагируют с концентрированной серной кислотой даже при нагревании. В случае изопарафинов происходит разрыв цепи, в результате чего кроме других продуктов образуется небольшое количество сульфокислот. При использовании концентрированной серной кислоты с содержанием более 20% SО2 можно получить сульфокислоты и из н-парафинов, но с невысоким выходом.
Для введения сульфогрупп в насыщенную молекулу органического вещества можно использовать следующие методы:
1. реакции присоединение бисульфита натрия к карбонильным соединениям и а-окисям:
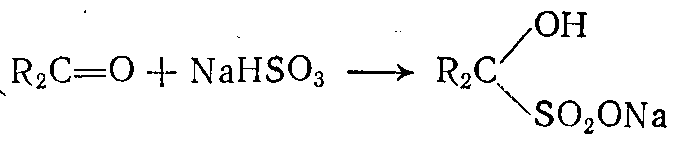
2. замещение атомов хлора в хлорпроизводных при действии сульфита натрия:
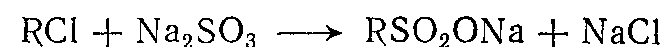
3. сульфохлорирование – это совместное действие диоксида серы и хлора на парафины при освещении:
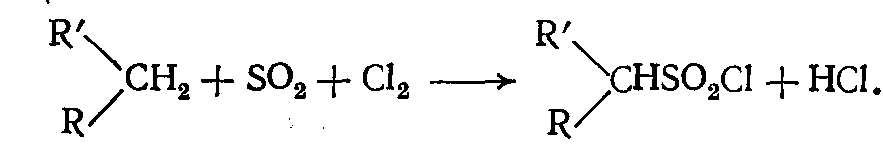
Реакция необратима и сильно экзотермична.
Сульфохлорированиепротекает по радикально-цепному механизму следующим образом:
1 Зарождение цепи: 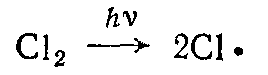
2 Рост цепи: 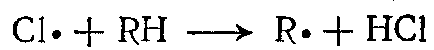 ,
, 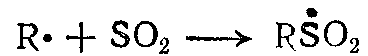 ,
, 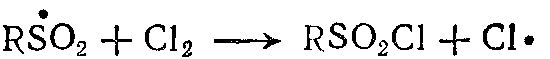
3 Обрыв цепи- это взаимодействие между свободными радикалами, например: R∙+Cl∙→R: Cl
Относительная реакционная способность различных атомов водорода при сульфохлорировании иная, чем при хлорировании, по-видимому, из-за пространственных затруднений при подходе молекулы сернистого ангидрида к третичному алкильному радикалу: втор-> перв-> трет-.
Сульфохлорирование принадлежит к типу последовательно-параллельных процессов,
вторая стадия протекает медленнее первой, так как сульфохлоридная группа снижает способность к дальнейшему замещению.
Побочными реакциями, сопровождающими процесс сульфохлорирования, являются:
а) фотохимическое хлорирование исходных реагентов с образованием хлорпроизводных:
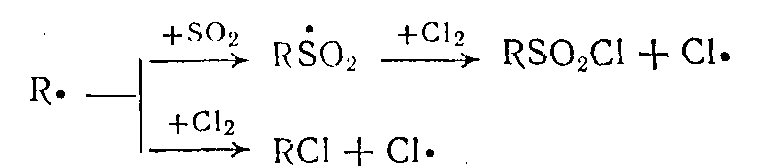
б) десульфировавия сульфохлоридов с выделением сернистого ангидрида:
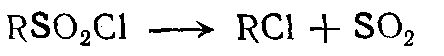
в) образование хлорсульфохлоридов: 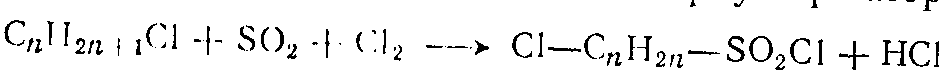
4. сульфоокисление - совместное действие диоксида серы и кислорода на насыщенные парафины или циклопарафины, протекает по следующему уравнению:
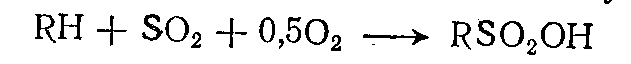
Реакция необратима и сильно экзотермична.
Механизм реакции радикально-цепной и состоит из следующих стадий:
1 Зарождение цепи происходит в результате разрушения связи между атомом углерода и водородом в молекуле парафина за счёт непрерывного облучения ультрафиолетовыми лучами: 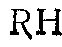 →
→ 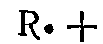

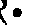 ; Для образования свободных радикалов при сульфоокислении можно использовать инициаторы, которые в небольших количествах непрерывно подаются в реактор. В качестве таких добавок используют ангидриды низкомолекулярных кислот (уксусной, пропионовой), хлорангидриды этих кислот и т. п.
; Для образования свободных радикалов при сульфоокислении можно использовать инициаторы, которые в небольших количествах непрерывно подаются в реактор. В качестве таких добавок используют ангидриды низкомолекулярных кислот (уксусной, пропионовой), хлорангидриды этих кислот и т. п.
2. свободный радикал, образовавшийся при зарождении цепи:, начинает цепь превращений, состоящую из следующих элементарных стадий:
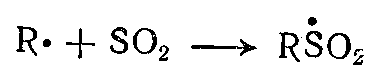 ;
;  ;
; 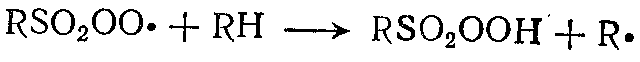
При этом промежуточно образуются сульфоперекисный радикал и сульфогидроперекись.
3. Обрыв цепи: сульфогидроперекись достаточно стабильна при температуре реакции, и без введения посторонних веществ является ее конечным продуктом. Для получения сульфокислот пользуются следующими методами
а) водно-световой - введении в реакционную смесь воды, при этом сульфогидроперекись окисляет SO2 в серную кислоту, сама превращаясь в сульфокислоту:
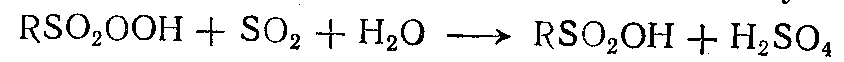
б) безводный, состоит из двух этапов:
- разрушение перекисной группировки при освещении в присутствии уксусного ангидрида, который связывает сульфогидроперекись в довольно устойчивую к разложению ацетилсульфоперекись: 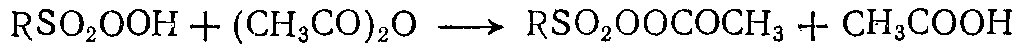 ;
;
- второй этап идет без освещения и при более высокой температуре, при которой ацетилсульфоперекись становится способной инициировать радикально-цепной процесс сульфоокисления 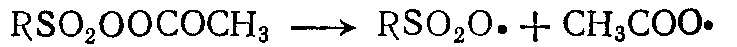 ;
;
 ;
; 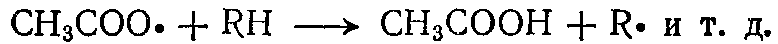
Относительная реакционная способность различных атомов водорода при сульфоокислении иная, чем при окислении, по-видимому, из-за пространственных затруднений при подходе молекулы сернистого ангидрида к третичному алкильному радикалу: втор-> перв-> трет-.
Сульфоокисление принадлежит к типу последовательно-параллельных процессов, вторая стадия протекает медленнее первой, так как сульфоокисная группа снижает способность к дальнейшему замещению.
Побочными реакциями, сопровождающими процесс сульфоокисления, являются различные процессы окисления радикалов:
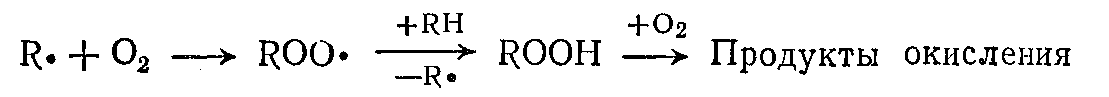
Продуктами, получаемыми реакциями сульфохлорирования и сульфоокисления являются поверхностно-активные вещества типа алкилсульфонатов. Алифатические сульфохлориды и сульфокислоты — весьма реакционноспособные вещества, пригодны для синтеза ряда ценных продуктов. Они реагируют со спиртами, фенолами, аминами и дают сложные эфиры и амиды, которые находят применение в качестве пластификаторов, промежуточных продуктов и т. д. Сульфохлорирование полиэтилена дает каучукоподобный полимер, легко вулканизуемый диаминами.
 2015-04-20
2015-04-20 4534
4534








