Прежде чем сформулировать первый закон термодинамики рассмотрим такие понятия, как термодинамический процесс, работа процесса, внутренняя энергия.
Под термодинамическим процессом понимают последовательное изменение состояния рабочего тела, которое происходит под влиянием механического (сжатие или расширение) или термического (нагрев или охлаждение) воздействия окружающей среды.
Процессы бывают:
- равновесные;
- неравновесные.
Под равновесным понимают процесс, который протекает с бесконечно малой скоростью так, что в каждый момент времени в рабочем теле успевает установиться равновесное состояние, т.е. такое состояние, при котором во всех точках рабочего тела параметры имеют одинаковые, не изменяемые во времени значения. Равновесный процесс есть процесс идеальный. Равновесные процессы называют обратимыми, так как они могут протекать сначала в прямом, а затем в обратном направлении через одну и ту же последовательность равновесных состояний, т.е. термодинамическая система возвращается в исходное состояние.
Под неравновесным процессом понимают все действительные (реальные) процессы, в которых рабочее тело проходит через неравновесные состояния. Неравновесные процессы называют необратимыми, т.е. система при этом не возвращается в исходное состояние. Все естественные самопроизвольные процессы необратимы. Обратимых процессов в природе не существует. Типичным примером необратимого процесса является процесс трения. Работа, затраченная на преодоление трения, превращается в теплоту.
В термодинамике широко используется диаграмма, в которой по оси абсцисс откладываются значения удельных объёмов υ, а по оси ординат – значение давлений p. По этим координатам можно определить состояние рабочего тела. Рассмотрим процесс изменения параметров рабочего тела в
цилиндре со свободно перемещающимся поршнем рис.1.
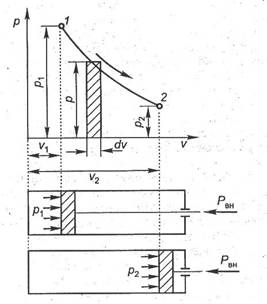 В цилиндре находится газ с начальными параметрами p1, v1, Т1. Это состояние на диаграмме изображено точкой 1. Давление газа на поршень в начальном состоянии уравновешивается внешней силой Рвн, приложенной к штоку, и давлением атмосферы. При уменьшении внешней силы поршень под действием давления газа начнёт перемещаться вправо, увеличивая объём газа и уменьшая давление и температуру.
В цилиндре находится газ с начальными параметрами p1, v1, Т1. Это состояние на диаграмме изображено точкой 1. Давление газа на поршень в начальном состоянии уравновешивается внешней силой Рвн, приложенной к штоку, и давлением атмосферы. При уменьшении внешней силы поршень под действием давления газа начнёт перемещаться вправо, увеличивая объём газа и уменьшая давление и температуру.
Рис.1.Процесс расширения газа.
Состояние газа в конце процесса расширения изобразим точкой 2. Соединив, все точки промежуточных состояний между точками 1 и 2,получим кривую 1-2 процесса расширения.
Работа расширения газа будет равна площади, ограниченной сверху кривой процесса 1-2, снизу осью абсцисс, а слева и справа двумя крайними ординатами процесса, соответствующими начальному и конечному состояния газа. Рабочее тело может произвести работу только при переходе из неравновесного состояния в равновесное. Поршень рис.1 будет перемещаться только до тех пор, пока давление над поршнем не станет равно давлению окружающей среды.
Первый закон термодинамики устанавливает количественную меру при переходе одного вида энергии в другой и является частным случаем всеобщего закона сохранения и превращения энергии.
Изменение внутренней энергии системы при её переходе из одного состояния в другое равно сумме количества теплоты, подведённого к системе извне, и работы внешних сил, действующих на неё.
Теплота может превращаться в механическую работу, а работа в теплоту лишь в строго эквивалентных количествах, причём количество теплоты, полученное рабочим телом от какого-либо источника тепла, равна сумме приращения внутренней энергии этого тела и количества совершенной им работы, т.е.
Q = AL + (U2 – U1), где Q - подведённая к рабочему телу теплота; A – коэффициент пропорциональности; L– работа, произведённая рабочим телом в результате подвода теплоты; U1- внутренняя энергия рабочего тела в начале подвода теплоты; U2- внутренняя энергия рабочего тела в конце подвода теплоты.
 2015-05-05
2015-05-05 547
547








