Задание: Приготовить 200 мл 0,5н раствора CuSO4 из кристаллогидрата CuSO4 · 5Н2О.
1. Вычислите массу (mВ) безводной соли CuSO4, необходимую для приготовления 200 мл 0,5 н раствора сульфата меди
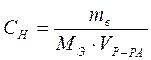 ;
;
где СН – эквивалентная концентрация раствора, моль/л;
МЭ – эквивалентная масса растворенного вещества (сульфата меди), г/моль;
VР-РА – объем раствора, л;
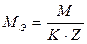 ;
;
где М – молярная масса растворенного вещества, г/моль;
К – количество катионов или анионов в сульфате меди;
Z – заряд катиона меди или аниона (сульфат-иона) по модулю;
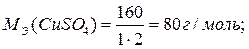
mВ = СН·VВ·МЭ = 0,5 · 0,2 · 80 = 8 г;
2. Вычислите массу кристаллогидрата CuSO4·5Н2О, необходимую для приготовления 200 мл 0,5 н раствора сульфата меди
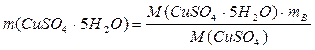 ;
;
где М(CuSO4·5Н2О) – молярная масса кристаллогидрата сульфата меди (медного купороса), г/моль;
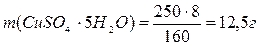
3. Взвесьте расчетное количество кристаллогидрата с помощью весов и предварительно взвешенного часового стекла.
4. Высыпьте навеску через воронку в мерную колбу на 250 мл и тщательно смойте дистиллированной водой из промывалки часовое стекло над воронкой. Воронку также тщательно обмойте из промывалки дистиллированной водой.
5. Навеску растворите в небольшом количестве воды, затем долейте колбу до метки, закройте пробкой и хорошо перемешайте.
6. Определите ареометром с помощью руководителя плотность полученного раствора.
7. Рассчитайте массовую долю CuSO4 в полученном растворе.
8. Рассчитайте нормальную (эквивалентную) и молярную концентрации полученного раствора.
9. Рассчитайте ошибку эксперимента по формуле:
±ΔАБС = СН(теор) - СН(оп);
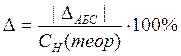
Таблица 3.1
| № | Вид определения | Данные опыта |
| Объем заданного раствора, мл | ||
| Нормальность заданного раствора, моль/л | ||
| Масса CuSO4, необходимая для приготовления раствора, г | ||
| Масса CuSO4·5Н2О, необходимая для приготовления раствора, г | ||
| Плотность приготовленного раствора, г/мл | ||
| Массовая доля CuSO4 в приготовленном растворе, % | ||
| Молярная концентрация приготовленного раствора, моль/л | ||
| Нормальная (эквивалентная) концентрация приготовленного раствора, моль/л | ||
| Относительная ошибка эксперимента, % |
10. Результаты сведите в таблицу 3.1.
 2015-04-20
2015-04-20 14427
14427
