Промежуточная степень окисления карбонильных соединений обусловливает их способность к реакциям окисления и восстановления. В качестве восстановителей в реакциях восстановления используют молекулярный водород и гидридные комплексы алюминия и бора.
- Восстановление карбонильных соединений до спиртов.
а) восстановление молекулярным водородом
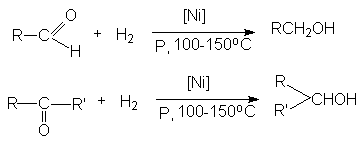
В качестве катализаторов этих реакций используют Ni, Pd, Pt,CuCrO2.
б) восстановление гидридными комплексами металлов
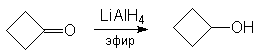
Эти методы находят применение в случае дорогостоящих или неустойчивых карбонильных соединений. В этих реакциях ключевой стадией является перенос гидрид-аниона от восстановления к карбонильному углеродному атому
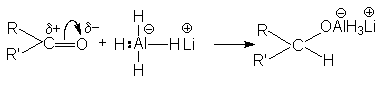
Можно полностью использовать все четыре атома водорода в литийалюминий гидриде:
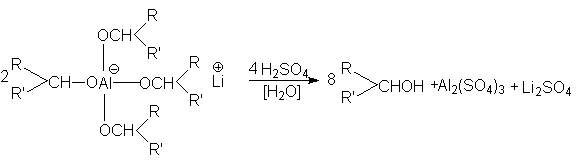
Преимущество литий алюминий гидрида состоит в том, что он селективно восстанавливает карбонильные группы, не затрагивая >C=C< связи. Он также восстанавливает карбонильные группы карбоновых кислот.
Другой восстановитель NaBH4 - более мягкий. Он восстанавливает альдегиды и кетоны, но инертен по отношению к карбоновым кислотам и сложным эфирам.
в) восстановление алкоголятами алюминия – реакция Меервейна-Понндорфа-Верлея-Оппенауэра
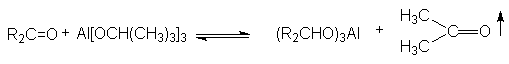
Смешение равновесия в этой реакции обеспечивается непрерывной отгонкой карбонильного продукта из реакционной массы.
- Восстановление карбонильных соединений до углеводородов.
а) восстановление по Клемменсену.
Если карбонильное соединение устойчиво к действию кислот, то используют этот тип восстановления
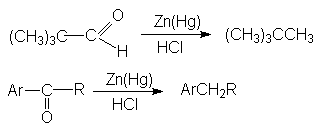
б) ион-радикальная димеризация альдегидов и кетонов.
Если восстановление амальгамированным цинком или магнием осуществлять в нейтральной водной среде, то результатом реакции является образование пинаконов. Первой стадией этой реакции является перенос электрона от металла к карбонильной группе с последующей димеризацией ион-радикалов
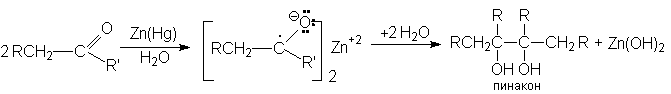
в) восстановление по Кижнеру-Вольфу
Этот вид восстановления используется в тех случаях, когда объект восстановления устойчив к основаниям
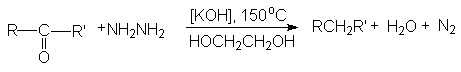
 2015-04-23
2015-04-23 1572
1572
