Все реакции солей диазония можно разделить на четыре большие группы, различающиеся по механизму взаимодействия катиона диазония с нуклеофильным агентом Х-.
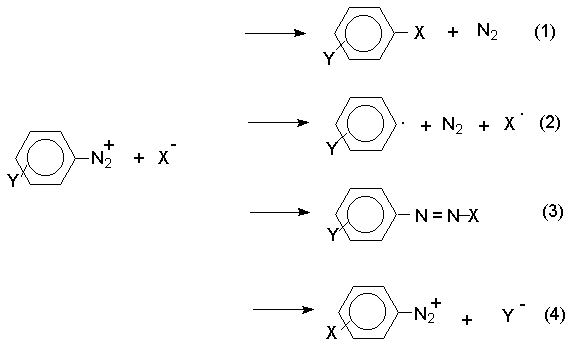
Реакции типа (1) и (4) - нуклеофильное ароматическое замещение. В реакциях группы (1) имеет место замещение самой диазогруппы. В реакциях типа (4) диазогруппа, как очень сильный акцептор, активирует нуклеофильное замещение группы Y в орто - или пара -положении к диазогруппе. В реакциях группы (2) происходит радикальный распад соли диазония. Образующийся при этом арильный радикал Ar претерпевает затем дальнейшее превращение. Третий тип реакций предполагает атаку нуклеофильным агентом крайнего атома азота диазониевого катиона.
По формальному признаку реакции солей диазония можно разделить на две большие группы: реакции идущие с выделением (1,2) и без выделения (3,4) азота.
Реакции, идущие с выделением азота
Замещение диазогруппы – один из основных методов введения заместителей в ароматическое кольцо. Замещение протекает как по гетеролитическому, так и по гомолитическому механизму. Характер разрыва связи углерод-азот в катионе арендиазония зависит прежде всего от природы нуклеофильного агента. Гетеролиз связи С-N имеет место при взаимодействии с жесткими нуклеофильными агентам - водой, фторид-ионом и при проведении реакции в растворителях с электрофильными или малонуклеофильными свойствами. Гомолитическому расщеплению связи углерод-азот благоприятствует рост нуклеофильных свойств растворителя и использование мягких нуклеофильных агентов (J-, SCN-). Все эти анионы относятся к сильным восстановителям, что облегчает перенос одного электрона от реагента к катиону диазония. Эту же функцию в отдельных случаях может выполнять и растворитель.
Для многих реакций переход от гетеролитического к гомолитическому механизму происходит очень легко при введении в раствор солей одновалентной меди.
а) Замещение диазогруппы на гидроксил.
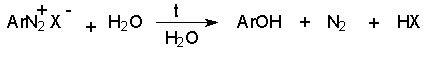
Реакцию обычно проводят путем разложения соли диазония в 40-50 %-ном растворе серной кислоты. Реакция протекает как процесс мономолекулярного ароматического нуклеофильного замещения (SN1). Для получения фенолов используют соли диазония с малонуклеофильными или комплексными анионами (X=HSO4-, BF4-), что избежать образования продуктов арилирования противоиона промежуточно образующимся арилкатионом. Образующийся из Ar+ и HSO4- эфир серной кислоты ArОSO3H в условиях реакции гидролизуется до фенола. Как во всех процессах SN1 - типа стадия, определяющая скорость реакции, и стадия, определяющая состав продуктов реакции, не совпадают.
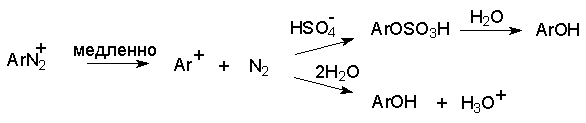
б) Замещение диазогруппы на фтор (реакция Шимана).
Замещение диазогруппы на фтор происходит при термическом разложении тетрафторборатов арендиазония.
ArN2 +BF4 - ® ArF + N2 + BF3
Реакция протекает, вероятно, через промежуточное образование арилкатиона. Выходы арилфторидов сильно колеблются в зависимости от природы заместителя в бензольном кольце арендиазокатиона. Увеличению выхода способствует наличие в бензольном кольце электронодонорных заместителей. Реакция Шимана – один из основных методов введения фтора в ароматическое кольцо.
с) Замещение диазогруппы на иод
ArN2 +X - + KI ® ArI + N2 + KX
Замещение диазогруппы на йод осуществляется по принципиально иному механизму и представляет собой ион-радикальный процесс, в котором иодид-ион выступает в роли одноэлектронного восстановителя.
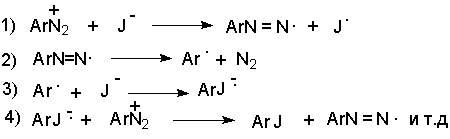
В препаративном отношении это одна из самых простых реакций ароматических диазосоединений.
д) Замещение диазогруппы на хлор-, бром-, циан- и нитрогруппу (реакция Зандмейера).
Выходы арилхлоридов, арилбромидов и арилцианидов в реакциях солей арендиазония с хлорид-, бромид- и цианид-ионами в отсутствие катализаторов невелики и редко превышают 20%. Для получения этих соединений используют реакцию Т. Зандмейера, который обнаружил, что такое замещение эффективно катализируется солями меди (I). Для введения хлора и брома используют раствор галогенида меди (I) в соответствующей галогеноводородной кислоте.
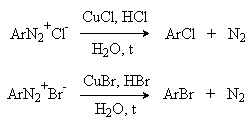
Для введения цианогруппы нейтральный раствор соли диазония смешивают с раствором комплексного цианида.
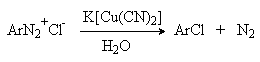
Механизм реакции Зандмейера достоверно не установлен. Считается, что катион меди (I) выступает в роли восстановителя катионов диазония, поскольку сами ионы Cl- и Br- в отличие от иодид-ионов трудно окисляются. Образующиеся при одноэлектронном восстановлении арилрадикалы Ar или арилдиазорадикалы Ar - N = N далее окисляются солью двухвалентной меди. Предполагают, что радикалы образуются и реагируют в реакционном комплексе соль диазония–соль меди и в растворе как кинетически независимые частицы не появляются.
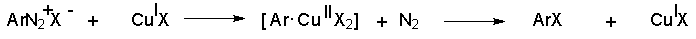
Вместо солей меди (I) может использоваться медный порошок (реакция Гаттермана). Метод дает особенно хорошие результаты при замене диазогруппы в тетрафторборатах или гексафторфосфатах арендиазония на нитрогруппу.
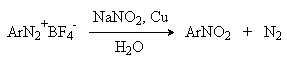
е) Замещение диазогруппы на водород (дезаминирование первичных ароматических аминов).
Замещение диазогруппы на водород происходит при действии восстановителей. В качестве восстановителей используют спирты.
ArN2+X- + RCH2OH ® ArH + R-CH=O + N2 + HX
Реакция протекает по цепному радикальному механизму.
Зарождение цепи:
ArN2+ + CH3OH ® ArN2. + CH3OH.+
ArN2. ® Ar. + N2
CH3OH. + ®.CH2OH + H+
Развитие цепи:
Ar. + CH3OH ® ArH + .CH2OH
. CH2OH + ArN2+® ArN2. + CH2OH+ т.е. (H2-C=O+H)
CH2OH+ ® H-C(H)=O + H+
ArN2. ® Ar . + N2 и т.д.
Параллельно протекает замещение диазозогруппы на алкоксильную.
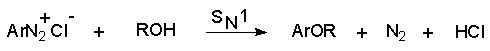
Эта реакция, также как и взаимодействие катиона диазония с водой, протекает по гетеролитическому мономолекулярному механизму. Соотношение продуктов в двух конкурирующих процессах - гетеролитическом и гомолитическом - зависит от природы заместителя в бензольном кольце катиона арендиазония и от рН среды. Протеканию гомолитического процесса восстановления способствует наличие электроноакцепторных заместителей в ароматическом кольце и среда, близкая к нейтральной, в которой доминируют гомолитические процессы разложения ковалентных форм диазосоединений. В общем же случае образуется смесь эфира фенола и углеводорода, поэтому восстановительное дезаминирование осуществляют другими методами.
Универсальным восстановителем при замещении диазогруппы на водород является фосфорноватистая кислота H3PO2.
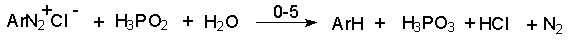
Замещение дизогруппы на водород широко применяется в органическом синтезе, так как позволяет получать арены, которые трудно или вообще невозможно синтезировать другими методами.
ж) Получение биарилов (реакция Гомберга - Бахмана).
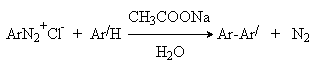
При разложении солей диазония в слабощелочной среде в присутствии аренов образуются биарилы. Процесс протекает через промежуточное образование арилрадикалов и является примером радикального ароматического замещения. Реакция используется для синтеза несимметричных биарилов.
Реакции, идущие без выделения азота
а) Реакция азосочетания
Соли диазония реагируют с фенолами и ароматическими аминами с образованием ярко окрашенных азосоединений.
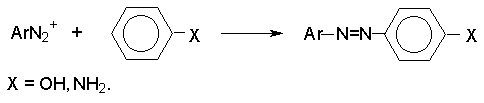
Азосочетание относится к типичным реакциям электрофильного ароматического замещения, скорость которых зависит от электрофильных свойств катиона диазония (диазосоставляющей) и от электронодонорных свойств ArX (азосоставляющей).
Катион арендиазония относится к числу слабых электрофильных агентов, так как его положительный заряд делокализован за счет сопряжения с ароматическим кольцом. Как слабый электрофильный катион диазония взаимодействует только с такими производными бензола и нафталина, которые содержат сильные электронодонорные заместители.
Реакционная способность азосоставляющей уменьшается в ряду:
X = O- > NR2 > NHR > NH2 > OH~OR >> Alk.
Реакционная способность катиона арендиазония в большой степени зависит от природы заместителей в бензольном кольце. Электроноакцепторные заместители увеличивают, а электронодонорные уменьшают электрофильные свойства катиона диазония.
Активной формой фенола в качестве азосоставляющей является фенолят – анион, поэтому сочетание с фенолами проводят в слабоосновной среде. Однако рН раствора в этом случае поддерживают в интервале 8-10, избегая более высокой основности раствора. Это объясняется тем, что при значениях рН>12 резко уменьшается концентрация единственной активной в реакциях азосочетания формы катиона диазония ArN2+ и растет концентрация нереакционноспособного диазотат-аниона
Ar – N = N – O-.
Сочетание с ароматическими аминами проводится в слабокислой среде с рН 3 – 5, где катион диазония реагирует с активированным к электрофильному замещению свободным амином.
Азосочетание отличается от других реакций электрофильного ароматического замещения чрезвычайно высокой селективностью. Азосочетание с фенолят-ионами и аминами осуществляется в пара -положение к гидроксильной группе или аминогруппе и только в том случае, если пара -положение занято, сочетание идет в орто -положение.
Реакция азосочетания имеет большое практическое значение, так как азосоединения используются как красители (азокрасители). В результате комбинации солей диазония из различных ароматических аминов с различными азосоставляющими и подбора условий могут быть получены самые разнообразные азокрасители.
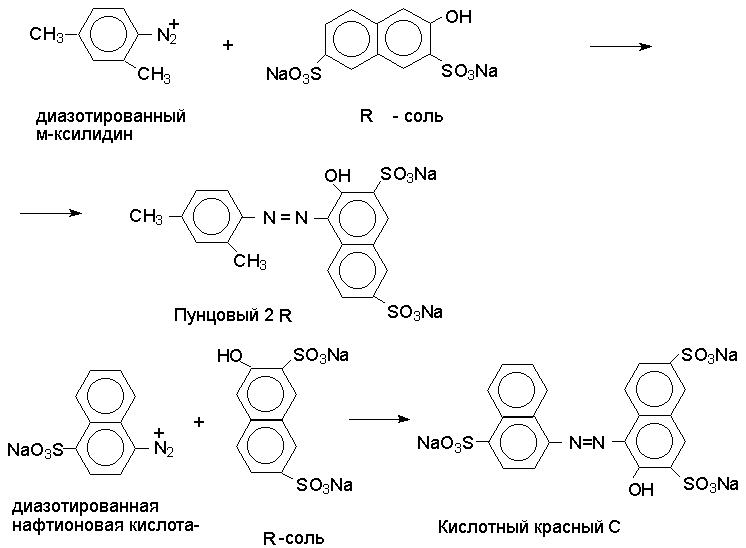
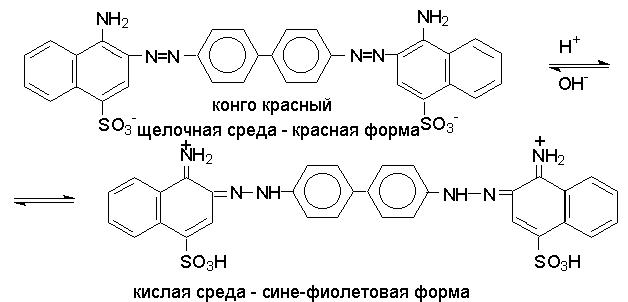
Многие азокрасители в зависимости от рН среды изменяют строение, а, следовательно, и окраску. Такие азокрасители находят применение в качестве индикаторов (метилоранж, метаниловый желтый, метиловый красный, конго красный и др.).
б) Восстановление солей арендиазония в арилгидразины.
Существует два общих метода восстановления солей диазония до арилгидразинов.
Первый способ заключается в восстановлении катиона арендиазония смесью сульфита и гидросульфита натрия. На первой стадии образуется ковалентный диазосульфонат, который далее восстанавливается до соли арилгидразин-N–N/-дисульфокислоты, гидролизующейся далее до арилгидразина.
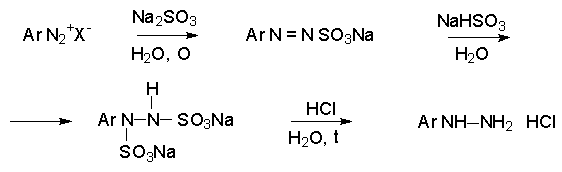
Другой способ состоит в восстановлении солей диазония двухлористым оловом в соляной кислоте.
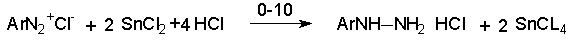
 2015-04-23
2015-04-23 3107
3107








