Нитрозоарены
Нитрозоарены легко восстанавливаются, поэтому их трудно получить восстановлением нитроаренов. Лучший метод получения нитрозоаренов состоит в окислении арилгидразинов.
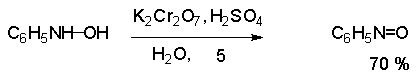
Возможно непосредственное введение нитрозогруппы в ароматическое кольцо действием азотистой кислоты на фенолы и третичные ариламины (см. лек.№29 и 42)
В кристаллическом состоянии ароматические нитрозосоединения существуют в виде бесцветных димеров. В жидком и газообразном состоянии существует равновесие между димером и мономером. Мономеры окрашены в зеленый цвет.
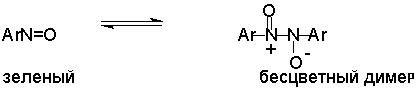
Нитрозосоединения, подобно карбонильным, соединениям вступают в реакции с нуклеофилами. Например, при конденсации с арилгидроксиламинами образуются азоксисоединения (см. выше), а с ариламинами – азосоединения.
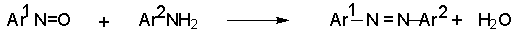
Арилгидроксиламины
Кроме описанного выше метода получения восстановлением нитроаренов в нейтральной среде арилгидроксиламины синтезируют путем нуклеофильного замещения в активированных аренах.
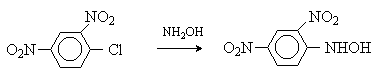
Как промежуточные продукты восстановления нитроаренов арилгидроксиламины могут быть окислены в нитрозосоединения (см. выше) и восстановлены в амины путем каталитического гидирирования или действием металла в кислой среде.
ArNHOH + Zn + 3HCl ® ArNH2 . HCl + ZnCl2 + H2O
В кислой среде арилгидроксиламины перегруппировываются аминофенолы, что используется для получения последних, например:
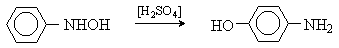
Азоксиарены
Кроме описанных выше методов – конденсации нитрозосоединений с арилгидроксиламинами и восстановления нитроаренов метилатом натрия, азоксиарены могут быть получены окислением азоаренов пероксисоединениями.
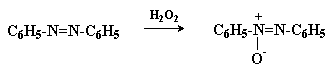
В щелочной среде азоксиарены восстанавливаются до азо- и далее гидразоаренов (см. выше).
Азоарены
Образуются при восстановлении нитроаренов, арилгидразинов и азокси- аренов в щелочной среде, например:
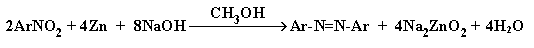
Несимметричные азосоединения получают конденсацией нитрозосоединений с аминами (см. выше). Важный метод синтеза азосоединений – реакция азосочетания будет подробно рассмотрен далее (см. лек.№43)
Азоарены существуют в виде цис - и транс - изомеров. При облучении более стабильный транс -изомер превращается в цис -изомер. Обратное превращение происходит при нагревании.
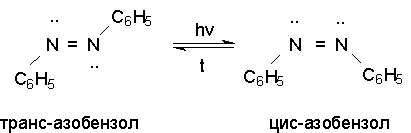
Азосоединения окрашены, многие из них используются в качестве красителей.
Гидразоарены
Это конечные продукты восстановления нитроаренов в щелочной среде. Гидразоарены – бесцветные кристаллические вещества, на воздухе окисляются в окрашенные азосоединения. В препаративных целях окисление проводят действием бромной воды
Ar-NHN-HAr + Br2 + 2NaOH ® Ar-N=N-Ar + 2NaBr + 2H2O
При восстановлении в жестких условиях гидразоарены дают ариламины.
Важным свойством гидразосоединений является перегруппировка в 4,4/-диаминобифенилы. Это превращение получило название бензидиновой перегруппировки. В настоящее время этим термином объединяют целую группу родственных перегруппировок, приводящих к образованию смеси орто - и пара -изомерных производных диаминобифенила.
При перегруппировке самого гидразобензола получается смесь диаминов, содержащая 70 % бензидина и 30 % 2,4/-диаминобифенила.
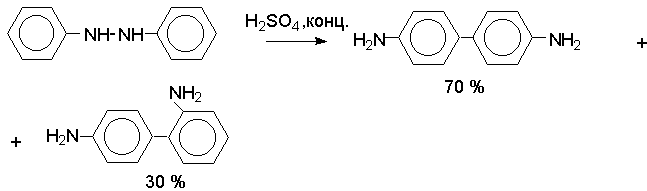
Если пара -положение в одном из бензольных ядер гидразобензола занято каким-нибудь заместителем, продуктом перегруппировки оказывается производное дифениламина (так называемая семидиновая перегруппировка).
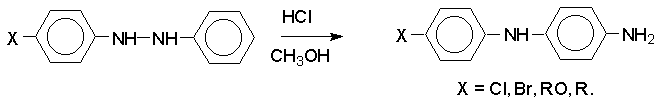
При изучении механизма бензидиновой и родственных перегруппировок было установлено, что они протекают внутримолекулярно. Если два различных гидразобензола подвергнуть совместной перегруппировке, то продукты перекрестной перегруппировки отсутствуют. Для перегруппировки самого гидразобензола было обнаружено, что скорость реакции пропорциональна концентрации гидразобензола и квадрату концентрации протона. Это означает, что перегруппировке подвергается дипротонированная форма гидразобензола. Было также показано, что монопротонированная форма гидразобензола превращается нацело в бензидин только при повторной обработке кислотой. Эти данные согласуются со следующим механизмом бензидиновой перегруппировки.
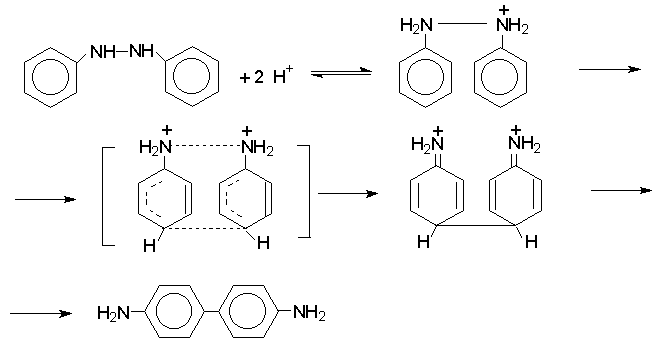
Предполагается, что переходное состояние образуется из такой конформации гидразобензола, в которой сильно сближены между собой два соответствующих атома углерода обоих бензольных колец. Образование новой углерод-углеродной связи и разрыв старой связи двух атомов азота происходит строго синхронно. Согласно современной терминологии бензидиновая перегруппировка относится к числу [5,5] - сигматропных перегруппировок.
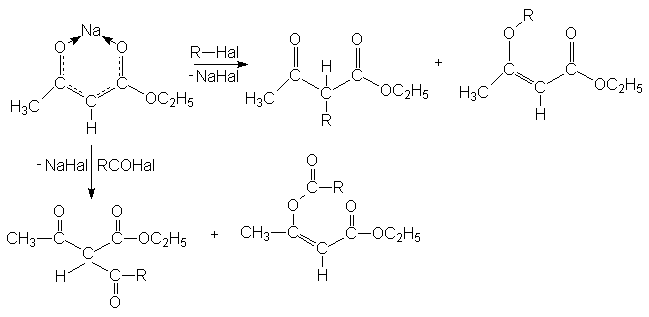
Алкилирование и ацилирование происходит главным образом у углеродного атома, т.к. атомы кислорода в значительной степени блокированы ионом металла.
Если в полученных продуктах алкилирования или ацилирования при атоме углерода в положении 2 содержится еще один кислый атом водорода открывается дополнительная возможность введения в это положение алкильных или ацильных групп, например
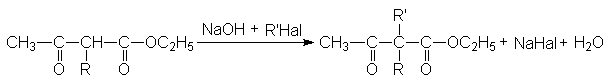
Последующий гидролиз и нагревание приводит к синтезу 1,3-кетокарбоновой кислоты и соответствующего кетона
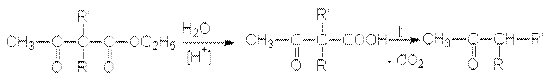
Эти реакции представляют собой важных синтетический метод получения кетонов различных структур.
 2015-04-23
2015-04-23 1545
1545
