Амиды представляют собой бесцветные кристаллические вещества или жидкости, растворяющиеся в органических растворителях. Амиды, в молекулах которых имеются связи N-H, ассоциированы вследствие образования межмолекулярных водородных связей и имеют более высокие температуры кипения.
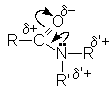
В молекулах амидов имеет место значительное сопряжение неподеленной парой электронов азота и p -электронной системой двойной связи С=О. Это приводит к образованию дополнительной поляризации связей в амидной группе и наличие электрофильных реакционных центров на ацильном и алкильных углеродных атомах и отрицательного - на карбонильном кислороде.
Химические свойства амидов.
- Реакции нуклеофильного замещения.
Примером может служить гидролиз. В нейтральной среде гидролиз протекает медленно. Поэтому реакцию ведут в присутствии минеральной кислоты либо основания, которые не только ускоряют ее, но и участвуют как реагенты.
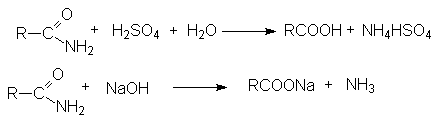
Активация молекулы амида кислотой связана с ее протонированием и увеличением положительного заряда на карбонильном углероде, который становится более восприимчивым к последующей нуклеофильной атаке:
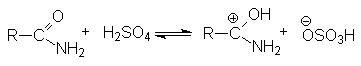
В случае щелочного гидролиза в качестве нуклеофила вместо воды выступает более реакционно способный гидроксил-анион, который эффективно осуществляет нуклеофильную атаку на кaрбонильный углерод:
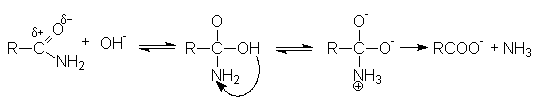
- Реакция восстановления.
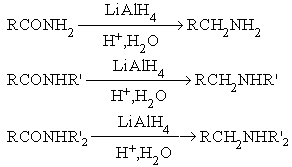
- Реакция дегидратации.
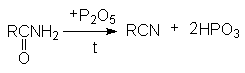
- Расщепление по Гофману.
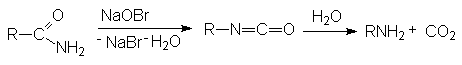
Механизм реакции
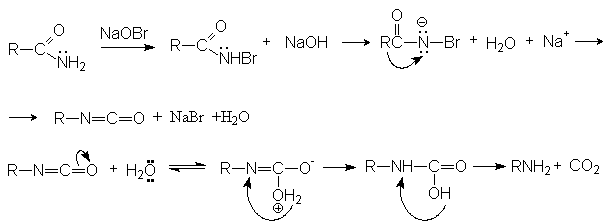
- Перегруппировка Курциуса характерна для азидов карбоновых кислот, которые ведут себя подобно амидам в расщеплении по Гофману.
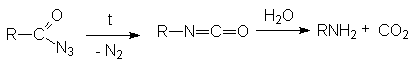
- Взаимодействие формамидов с реактивом Гриньяра (реакция Буво)
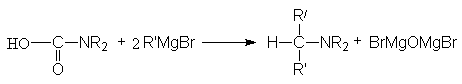
Продуктами этой реакции являются альдeгид и третичный амин.
НИТРИЛЫ КАРБОНОВЫХ КИСЛОТ
Общая формула нитрилов R-Cº N или CnH2n+1CN.
Методы получения нитрилов.
- Дегидратация амидов карбоновых кислот с помощью водоотнимающих агентов.
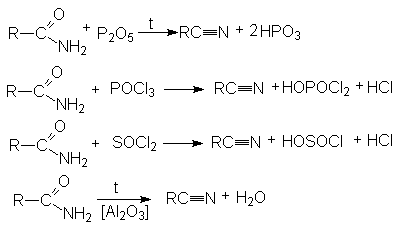
На практике в последнем случае пропускают над катализатором смесь карбоновой кислоты с аммиаком. В этом процессе совмещается образование амида и его дегидратация.
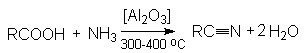
- Нуклеофильное замещение галогена в галогеналканах на циaнид-анион.
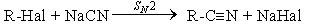
- Дегидратация альдоксимов.
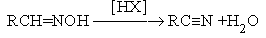
Механизм реакции:
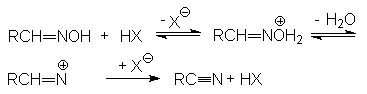
Химические свойства нитрилов.
Циано-группа характеризуется высокой степенью поляризации, следствием которой является образование частичного положительного заряда на углероде и отрицательного заряда – на азоте
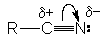
Это обусловливает, с одной стороны, восприимчивость углеродного центра к нуклеофильной атаке, с другой – основность атома азота.
o Реакции нуклеофильного присоединения.
Нитрилы легко реагируют с сильными анионными нуклеофильными реагентами (карбанионами, амидами металлов, щелочами, алкоголятами, тиоалкоголятами)
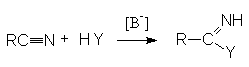
Примером может служить щелочной гидролиз нитрилов:
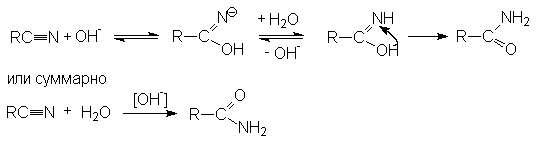
Дальнейший гидролиз амида приводит к образованию солей карбоновых кислот.
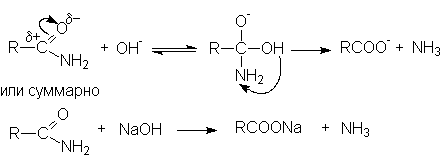
Таким образом суммарное уравнение щелочного гидролиза нитрилов можно представить как
R-Cº N + H2O + NaOH ® RCOONa + NH3
Реакции нитрилов со слабыми нуклеофилами (водой, спиртами) протекает крайне медленно. Для эффективного проведения этих реакций используют кислотный катализ. Активация молекулы нитрила в этом случае осуществляется за счет образования водородной связи между кислотой – катализатором и атомом азота и, как следствие, увеличение положительного заряда на нитрильном углеродном атоме.
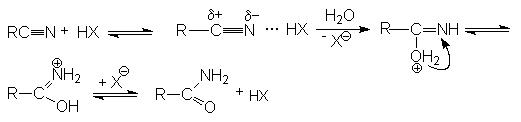
На последующей стадии гидролиза кислота НХ выступает одновременно как ускоритель реакции и реагент.
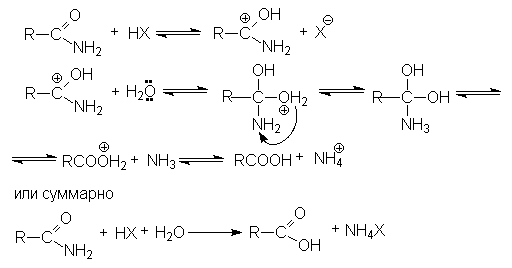
Таким образом, полный кислотный гидролиз нитрилов описывается уравнением:
R-Cº N + 2H2O + HX ® RCOOH + NH4X
Если в качестве реагента использовать водно-спиртовые среды, то можно осуществлять синтез сложных эфиров
R-Cº N + R'OH + H2O + HX ® RCOOR' + NH4X
o Гидрирование.
Реакции гидрирования нитрилов можно подразделить на две группы:
а) каталитическое гидрирование
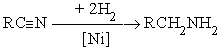
В качестве катализаторов этих реакций используют металлические Pt, Pd, Ni.
б) реагентное гидрирование
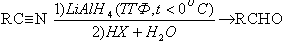
В качестве реагентов этих реакциях используют LiAlH4, NaBH4.
Механизм реакции:
RCº N + LiAlH4 ® RCH=N-Li + AlH3
RCH=N-Li + HX ® RCH=NH + LiX
Механизм второй стадии:
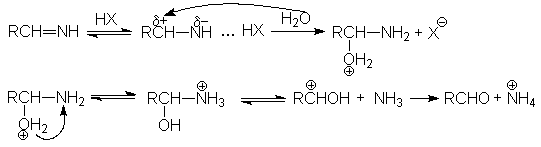
o Взаимодействие с металлоорганическими соединениями.
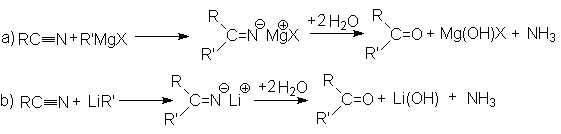
o Реакция Риттера.
Эта реакция является примером присоединения атома углерода к гетероатому (азоту).
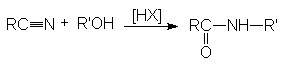
Реакция протекает по карбкатионному механизму:
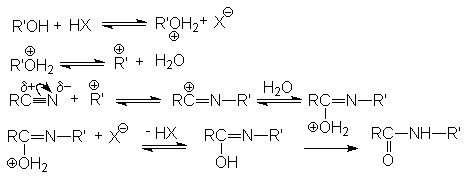
В реакцию вступают только спирты, дающие достаточно стабильные карбкатионы (вторичные, третичные, бензильные и т.п.). Первичные спирты не реагируют. Карбкатионы не обязательно следует генерировать из спирта, его можно получать протонированием алкенов.
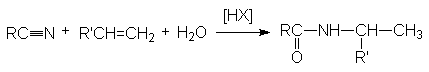
 2015-04-23
2015-04-23 6862
6862