Форма существования диазосоединений в растворе зависит от рН. Катионы диазония могут существовать в кислой среде и в средах, близких к нейтральной. При обработке растворов солей диазония щелочью образуются диазотаты.
ArN2+X- + 2NaOH ® Ar-N=N-O- Na+ + NaX + H2O
Процесс протекает в две стадии. Сначала катион диазония, как кислота Льюиса, взаимодействует с гидроксид-ионом с образованием диазогидроксида, который, будучи кислотой Бренстеда, быстро реагирует с еще одним эквивалентом щёлочи с образованием диазотат- аниона
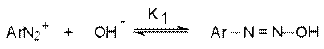
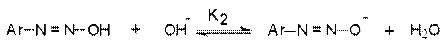
Для приведенных выше равновесий К2>К1, поэтому концентрация диазогидрата в водном растворе очень мала.
Диазотат-анионы существуют в анти - и син -формах. При взаимодействии катиона арендиазония со щелочью первоначально образуется менее стабильный син -диазотат, который медленнно изомеризуются в более стабильную анти -форму. Изомеризацию ускоряет нагревание и присутствие в бензольном кольце электроноакцепторных групп. Обратная изомеризация наблюдается только при УФ облучении.
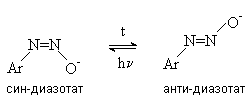
Диазотат-ионы являются амбидентными ионам с двумя нуклеофильными центрами - кислородом и азотом. анти -Диазотат протонируется исключительно по атому азота с образованием N-нитрозоамина.
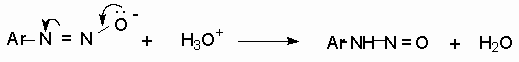
Далее N-нитрозоамин в кислой среде медленно превращается в катион арендиазония, как это было описано ранее в соответствии со стадиями (2 - 6) при обсуждении механизма диазотирования.
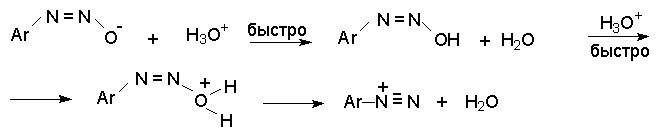
син -Диазотаты при протонировании образуют диазогидраты в результате протонирования по кислороду. Диазогидрат далее очень быстро превращается в кислой среде в катион арендиазония.
Общую схему протолитических превращений ароматических диазосоединений в водном растворе можно представить следующим образом.
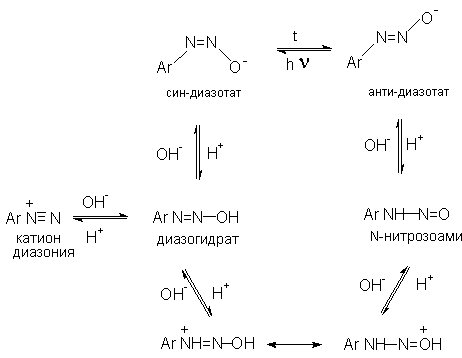
 2015-04-23
2015-04-23 577
577








