Вначале в ближайшей к отпрыску клетке, а затем и в последующих образуется канал, проходящий из клетки в клетку через соединяющие их протоплазматические связи.
Таким образом, формирование нового капилляра С, И. Щелкунов представляет в виде ряда мезенхимных клеток, обособившихся из синцития, окружающего растущий эндотелиальный отпрыск.
Описанный капилляр, названный С. И. Щелкуновым внутриклеточным, в дальнейшем претерпевает изменения, при которых утрачивается первоначальный сегментарный тип строения, а клетки, входящие в состав его, после деления превращаются в типичные эндотелиальные элементы,

Рис. 90. Образование капилляров в брыжейке (по С. И. Щелкунову). 1. а— клетки недиференцированного отдела синцития; b — прогрессивное развитие капилляров: 1 — ядро клетки, вошедшей в состав капилляра; 2 — адвен-тициальная клетка; 3 — клетка недиференцированного отдела синцития. Окраска гематоксилином, ок. 7, ob. imm. 2. Прогрессивное развитие капилляра: 1 — просвет капилляра; 2 — клетки недиференцированного отдела синцития; 3 — отростки клеток, вошедших в состав капиллярной стенки; 4 — вакуоли. Окраска гематоксилином, ок. 7, ob. imm. 3. Фрагмент интрацеллюлярного капилляра: 1 — просвет капилляра, заполненный кровяными элементами; 2 — клетки синцития, часть которых вошла в состав капилляра. Окраска гематоксилином, ок. 7, ob. imm. 4. Регрессивное развитие капилляров: а, b — фрагменты капилляров, состоящие из двух клеток; с, d — одноклеточные фрагменты капилляров; 1 — кровяные элементы, расположенные в замкнутой полости; е — клетка капиллярного фрагмента, освободившаяся от кровяных элементов: 2 — остатки гритроцитов. Окраска гематоксилином, ок. 7, ob. imm. 5. Фрагмент интрацеллюлярного капилляра: 1 — клетки фрагмента; 2 — остатки капиллярного просвета, заполненные кровяными клетками; 3 — клетки синцития; 4 — гистиоциты.
После образования из примыкающих мезенхимных клеток адвентиции капилляр принимает свой окончательный вид. С. И. Щелкунов считает его внеклеточным (рис. 90).
Следовательно, если первое из изложенных предположений об организации нового капилляра из эндотелия уже существующего капилляра отрицает всякое участие в этом процессе клеток примыкающей соединительной ткани, то второе предположение считает участие последних обязательным.
Таким образом, не существует единого мнения по такому важному вопросу, каким является вопрос о клеточном составе растущего капил-
ляра. Разногласия настолько велики, что даже в пределах одной и той
же гистологической школы уживаются совершенно противоположные в этом отношении взгляды (можно сравнить, например, точки зрения А. А. Заварзина и С. И. Щелкунова).
Существует и еще одно своеобразное представление о способе ро-
ста капилляров, впервые высказанное Ранвье (1874). Исследуя развитие капилляров в большом сальнике кролика, этот автор пришел к заключению, что в области млечных пятен рост капилляров происходит при непосредственном участии особых вазоформативных клеток.
Будучи постоянными элементами млечных пятен, вазоформативные клетки по форме своего тела отличаются от соединительнотканных и являются, таиим образом, совершенно самостоятельными элементами с особой функцией. Благодаря соединению отростков описываемых клеток между собой, образуются особые вазоформативные сети, которые превращаются в дальнейшем в сосудистую сеть независимо от собственно сосудистой сети млечньгх пятен.
Хотя Жолли (Jolly, 1906), Мартынов (1907) и другие подтвердили описание вазоформативных сетей, данное Ранвье, были высказаны также и другие мнения, согласно которым эти сети являются артефактами [Шпулер (Spuller)] или представляют собой результат обратного развития капиллярной сети [Восмер (Wosmer), 1898, и др.].
Несовершенство методов исследования и большие расхождения по принципиальным вопросам о росте капилляров сомы вызвали создаиие новой методики. Новый метод, заключающийся в прижизненном наблюдении растущих капилляров через прозрачную камеру, вставленную в ухо кролика, собаки или оторочку хвоста головастика [Сандисон (San-dison), 1924], безусловно позволяет вести уже более точные и более детальные микроскопические исследования, поскольку наблюдение производится посредством микроскопа при больших увеличениях.
Однако ряд недостатков значительно снижает преимущества работы с «прозрачной камерой». Важнейший, по нашему мнению, недостаток заключается в том, что при таком прижизненном наблюдении изучается на самом деле не естественный нормальный рост капилляров, а вызванная оперативным вмешательством регенерация сосудистой ткани ори наличии воспалительной пролиферации соединительной ткани и сосудов. Отрицательной стороной такого способа исследования является также отсутствие нормальных условий для роста регенерирующих сосудов, так как при наличии «прозрачной камеры» сосуды врастают на территорию,
лишенную нормального кровоснабжения. Кроме того, на этом участке имеются различные продукты распада веществ, в свою очередь безусловно оказывающие влияние на рост сосудов.
Мы постоянно убеждались в значительных отклонениях в развитии капилляров от нормальных форм при изменении самих условий роста. Исследования, проведенные в нашей лаборатории, показали, что состояние среды, в которой происходит рост мозгового капилляра, является решающим для определения морфологической формы строящегося капилляра. При этом особенно легко изменяющейся оказалась передняя часть растущего капилляра.
Выключение артериального снабжении или венозного оттока в ка-кой-либо области мозга, т. е. местная аноксемия или асфиксия мозговой ткани, а также общая асфиксия всего организма при дыхании животного воздухом с пониженным содержанием кислорода, в зависимости от силы их действия, вела к нарушению процесса роста и к изменению оформления строящегося капилляра (Е. Н. Космарская, 3. Н. Киселе-
|
|
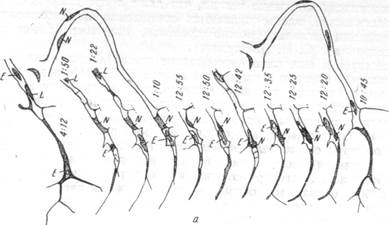
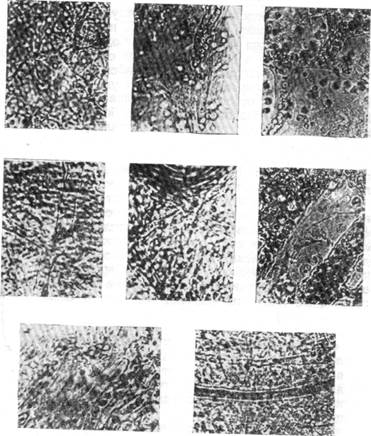
Рис. 91. Регенеративный рост капилляров, прослеженный с помощью
метода «прозрачной камеры» в ухе кролика (по Клярку). а — зарисовка последовательных стадий роста капилляров; б — микрофотографии последовательных стадий роста капилляров; Е — эритроцит; N — ядро.
ва, Н. С. Волжина). Не меньшие изменения в процессе роста иапилли-ров отмечаются в связи с наличием продуктов распада мозговой ткани в зоне размножения капилляров при травме мозга (Е. Н. Космарская). Недостаткам разбираемого метода «прозрачной камеры», использованного в многочисленных работах Кларка и его сотрудников, является также сомнение в степени правильности, с которой картины, видимые в «прозрачной камере», могут быть переданы на рисунках или микро-фотографиях. Наблюдение живой растущей ткани под микроскопом не дает все же той отчетливости деталей, которая возможна при изучении серий гистологических препаратов. Трудность изображения на рисунке картин, видимых в микроскопе, заключается в том, что клеточные элементы растущего капилляра становятся хорошо видимыми только после того, как капилляр делается проходимым для тома крови, т. е. уже после того, как капилляр окончательно сформировался.
Очевидно, этим и объясняется недостаточная четкость и убедительность иллюстративной части работ, выполненных методом «прозрачной камеры». Возможно, что благодари упомянутым трудностям микрофотографии совершенно неадэкватны приводимым рисункам (рис. 91, а и б),
Заканчивая изложение литературных данных о росте капилляров семы, нам кажется не лишним подчеркнуть слова С. И. Щелкунова, указывавшего, что до настоящих дней «развитие капилляров является одним из наиболее запутанных вопросов гистологии».
Таким образом, из литературного обзора выясняется, что не существует точно установленных и согласованных данных относительно способа роста капилляров не только в мозгу, но и в других тканях организма. Остается невыясненным вопрос, за счет каких клеток строится новый капилляр; принимают ли участие в его формировании андоте-лиальные клетки уже существующих сосудов или клетки, располагающиеся вне капилляра, или же для его формирования необходимо участие тех и других.
Еще большая неясность отмечается и при определении характера растущего капилляра. Предстоит еще установить, остается ли строящийся капилляр плотным ядерно-плазматическим недиферевцярованным тяжом вплоть до момента присоединения его к другому сосуду или параллельно с ростом происходит канализация, т. е. превращение его в подлинный капилляр с полостью, заполненной кровью, с диференциро-ванными эндотелиальными стенками.
Необходимо в дальнейшем выяснить, что представляет собой передний конец строящегося капилляра: является ли он плотным выростом протоплазмы или протоплазмой со включенным в нее ядром.
Все сказанное выше заставляет признать, что «...глава (гистологии Б. К.), посвященная эндотелию, в настоящее время еще далеко не может считаться законченной и представляет собой скорее постановку вопроса для дальнейших исследований» (Хлопин Н. Г., Общебиологические и экспериментальные основы гистологии, изд. АН СССР, 1946, стр. 313).
Столкнувшись в своих исследованиях с необходимостью выяснить совершенно не известный до сих пор способ роста капилляров в мозговой ткани, мы считали обязательным прежде всего четко разграничить во-просы, связанные с врастанием капилляров в еще не занятую сосудами область, от вопроса о размножении капилляров в области, содержащей замкнутую оформленную капиллярную сеть.
Такого рода постановки вопроса в литературе нам найти не удалось.
При изучении литературных данных мы пришли к выводу, что в боль-
163
шинстве случаев исследователи изучали именно врастание капилляров, но не их размножение.
Поэтому, приступая к изложению собственных данных, в настоящей главе, мы сосредоточили внимание лишь на описании фаз, которые проходит мозговой капилляр в процессе своего роста при наличии в мозгу уже оформленной капиллярной сети. Весь фактический материал, полученный в нашей лаборатории при изучении врастания сосудов в мозговое вещество, а также данные об организации замкнутой капиллярной сети в мозгу будут изложены ниже.
При изучении этапов роста мозгового капилляра на начальной стадии исследования наши попытки проследить их на сериях препаратов мозга, обработанных существующими гистологическими методами, не увенчались успехом.
Как уже говорилось, основные работы по изучению образования новых капилляров были произведены на тонких пластинчатых тканях. Оторочка хвоста головастика, сальник или ухо животного содержат ма-ло клиночных образований, благодаря чему сравнительно легко выделить плазматические тяжи строящихся капилляров с ядрами, входящими в их состав. Иные соотношения имеют место в медуллярной трубке. В период врастания в нее капилляров и в начальных стадиях формирования в медуллярной трубке капиллярной сети клетки основной ткани расположены очень плотно.
Обычные методы окраски, выявляющие ядра всех элементов, входящих в состав медуллярной трубки (медуллобластов, спонгиобластов, нейробластов), не дают возможности выделить среди них протоплазменные образования, представляющие на этой стадии развития строящиеся капилляры.
Таким образом, перед нами стала задача в первую очередь выработать метод, с помощью которого возможно было бы наблюдать только одну сосудисто-капиллярную сеть мозга и формирование нового капилляра в этой сети без импрегнации остальных компонентов нервной ткани. Нам казалось, что поиски нового метода гистологической обработки мозговой ткани должны опираться на особенности, отличающие капилляры мозга от таковых других тканей организма.
Как известно, эти особенности находят свое выражение даже в мор-фологическом строении мозговых капилляров. В отличие от 'Капилляров остальных органов и тканей капилляры мозга не содержат соединительнотканных элементов в стенке. Более того, в настоящее время исследователи в данной области все больше склоняются к тому, что стенка, мозгового капилляра не содержит также и эластической оболочки, наличие которой в свое время признавалось (Ранке). П. Е. Снесарез. например, считает, что молодые капилляры совершенно голы и лишь с возрастом возле них появляются разрозненные аргирофильные волокна.
Имеются указания о возникновении эластической оболочки на капиллярах мозга по мере старения организма (Д. С. Курбаганалиев, 1935). Однако появление ее может быть отмечено лишь в старших возрастах, не во всех мозгах и в различных, не совпадающих от случая к случаю, отделах мозга.
Существуют также особенности физиологической характеристики мозговых капилляров. Давно установлено, что при введении в ток крови взрослого животного какой-либо витальной краски все ткани организма окрашиваются краской, проходящей через стенку капилляров, тогда как ткань мозга оказывается совершенно неокрашенной.
Особый характер проницаемости мозговых капилляров безусловно указывает на своеобразие химического состава стенки мозгового капилляра у взрослого животного.
Несколько иной оказывается проницаемость в процессе роста капилляра.
В период формирования сосудистой сети в мозгу молодые капилляры пропускают витальную краску, но все же проницаемость их значительно меньше, чем у молодых капилляров в других тканях. Что касается проницаемости строящихся капилляров в мозгу, то подобных наблюдений пока нет.
Характерное морфологическое строение и особенности физиологических функций безусловно могут быть причиной особого отношения мозговых капилляров к реактивам, употребляющимся при гистологической обработке их. Известно, что различные элементы центральной нервной системы обладают особым сродством к серебру. Изменением способа предварительной обработки можно достичь избирательного выявления серебром любого из компонентов мозговой ткани: нервных клеток, оли-годендроглии, астроцитарной и гортеговской глии.
В выработке своего импрегнационного метода мы исходили поэтому из соображения, основанного на том, что сосудистая ткань является одной из составных частей мозгового вещества и подобно другим ее элементам должна выявляться серебром при создании для этого соответствующих условий.
Действительно, разработанный нами метод импрегнации сосудистой стенки серебром позволил получить на сериях гистологических препаратов одну только сосудисто-капиллярную сеть мозга. Серебрение сосудистой стенки оказалось эффективным не только для выявления уже оформленных, проходимых для тока крови сосудов и капилляров, но и для получения на тех же препаратах капилляров, находящихся на различных стадиях формирования их роста, а также капилляров, находящихся на различных стадиях гибели.
Таким образом, импрегнация серебром оказалась пригодной для выявления строящихся, функционирующих и атрофирующихся капилляров. В этом отношении мы пока, не могли отметить какой-либо разницы в степени импрегнации сосудистой стенки, находящейся безусловно в различных функциональных состояниях.
Факты, полученные в процессе выработки нового метода, дали возможность лишний раз убедиться в особой биохимической природе мозговых капилляров.
При обработке целых эмбрионов, когда действию серебра одновременно с тканью мозга подвергались и все остальные ткани организма, импрегнированными избирательно оказывались лишь мозговые капилляры.
Таким образом, благодаря нашей импрегна-ц и он но и методике, нам удалось в мозговой ткани
изолированно П О Л У Ч И Т Ь КАП И Л Л Я Р Н У Ю С Е Т Ь И О б-
наружить до того неизвестные фазы роста мозговых к а п и л л я р о в.
Дальнеишее и з л о ж е н и е будет представлять со-бой наши данные о росте капилляров только в мозговой ткани.
Сосудистая сеть мозга на ранних стадиях эмбриогенеза формируется при наличии в медуллярной трубке главным образом производных эктодермы.
Однако уже врастаете сосудов, первоначально располагающихся на ее поверхности в мягкой мозговой оболочке, в мозговую субстанцию сопровождается проникновением в мозг клеток мезенхимы. Последние и являются теми недиференцированными элементами, из которых впоследствии оформляется микроглия.
Таким образом, организация сосудисто-капиллярной сети в мозгу, начиная с самых ранних этапов ее построения, протекает в условиях наличия недиференцированных клеток мезенхимы и ее производных в виде клеток гортеговской глии.
Отсюда, по аналогии с другими тканями организма, служившими объектами специального исследования (сальник, оторочка хвоста головастика и др.), возможно было предположить формирование нового капилляра в мозгу двумя путями.
Можно было предполагать, что новый калилляр организуется по способу, описанному в свое время А. Голубевым, т. е. за счет слепых выростов протоплазмы материнского капилляра. Можно было также предположить, что в построении мозгового капилляра принимают участие клетки мезенхимальной природы - гортеговская глия, - присоединяющиеся к эндотелиальному протоплазменному выросту.
Приступая к изучению способа роста капилляров в мозговой ткани, мы ожидали обнаружить нечто подобное, известное по данному вопросу в отношении капилляров других тканей.
Последующее изложение покажет, что наши предположения не оправдались.
Способ построения мозгового капилляра оказался с о в в р ш е н н о о с о б ы м и х а р а к т е р н ы м, о т л и ч н ы м от всего описанного до настоящего времени в отношении роста капилляров в других тканях.
Для исследования способа формирования нового капилляра в условиях замкнутой сосудисто-капиллярной сети в мозгу, проходимой для тока крови, нами были использованы мозги эмбрионов кролика, кошки, собаки и человека разных периодов развития. Кроме того, изучались мозги новорожденных и мозги различного возраста животных и человека. На материале, включавшем более 100 серий, обработанных нашим импрегнационным методом, можно было проследить несколько; отчетливо выраженных этапов роста капилляра мозга.
Эти этапы, или фазы роста, совершенно одинаковы у различных животных и человека и поэтому приведенные описания их относятся в равной мере ко всем исследованным нами объектам. Дело будущего обнаружить возможные индивидуальные особенности роста капилляров мозга у различных животных и человека, на настоящем же этапе исследования эти различия не играют существенной роли.
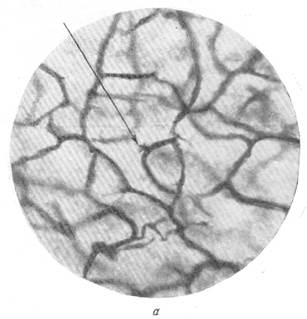
На рис. 92, а стрелкой показана начальная стадия образования нового капилляра. Как следует из рассмотрения рис. 92, а, а также рис. 93, а и б, образование нового капилляра начинается от уже существующего капилляра, входящего в состав замкнутой капиллярной сети.
На микрофотографии видно, что на начальном этапе новый капилляр представляет собой небольшое утолщение на одной из сторон стенки или накопление протоплазмы на стенке сформированного капилляра. От утолщения отходят многочисленные отростки, более подробно о которых будет сказано ниже (рис. 93, а).
Вследствие столь своеобразного вида строящегося капилляра на этой самой ранней стадии его формирования, его можно легко принять за первичную форму гортеговской глии, сползающую со стенки сосуда.
|
|
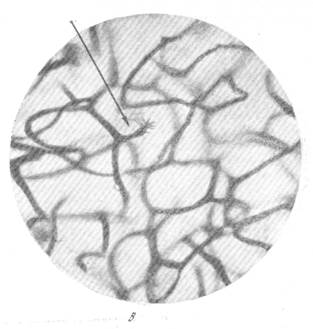
Рис. 92. Фазы роста капилляров в мозгу щенка 7 дней.
| а —растущий капилляр встадии «почки»; б — растущий капилляр в стадии «полипа». Импрегнация серебром по методу Б. Н. Клосовского. Увеличение 100. |
адии «полиг зие 100.
|
|
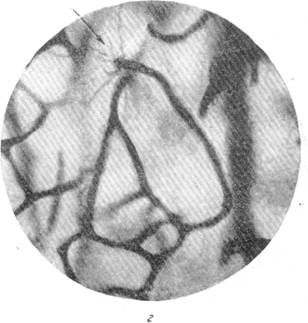
Рис. 92. Фазы роста капилляров в мозгу щенка 7 дней.
виг — растущие капилляры в стадии «гидроида». Импрегнация серебром по методу Б. Н. Клосовского. Увеличение 100.
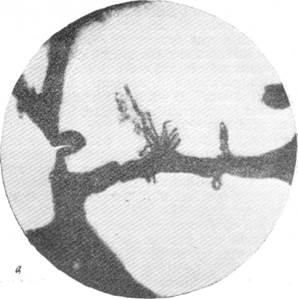
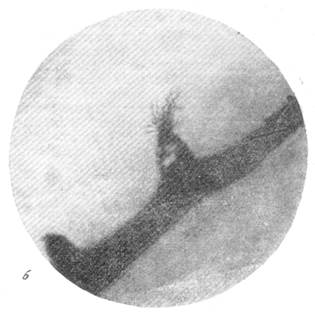
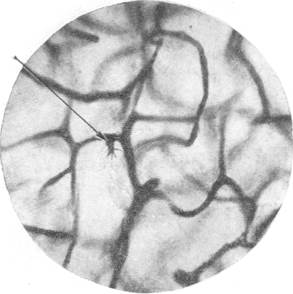
Рис. 93. Растущий капилляр в стадии «почки» в мозгу щенка 10 дней.
а— ранняя стадия; б — поздняя стадия. Импрегнация серебром по методу Б. Н. Клосовского. Увеличение 1 800.
Такое предположение тем более возможно, что гортеговская глия представляет собой компонент нервной ткани, для которого не существует еще общепризнанного способа проникновения в мозг.
Согласно современным представлениям, основным источником микро-глии является мягкая мозговая оболочка. Большинство исследователей не считает, что большая часть мезенхимных элементов проникает в мозг из мягкой мозговой оболочки непосредственно.
Вместе с тем пойти всегда приходится отмечать определенную связь проникающей в мозг микроглии с сосудистой стенкой.
Существует предположение, что связь микроглии с сосудами является только кажущейся, поскольку само продвижение ее в мозг происходит вдоль сосудов (Гоццано). В исследованиях Гоццано микроглия не вступает в какое-либо соединение с сосудистой стенкой и отделена от сосуда некоторым расстоянием.
Вместе с тем ряду авторов удалось наблюдать достаточно тесную связь микроглии с сосудами, что дало им повод предполагать происхождение микроглии от элементов сосудистой стенки или элементов крови.
Такую возможность не отрицал Гортега, считавший, что в образовании микроглии могут принимать участие мононуклеары крови, проходящие через стенку сосуда.
В. К. Белецкий в свою очередь предполагает образование микроглии из элементов крови и перицитов. Санто, Юба, Бользи относят возникновение мезоглии в мозгу за счет эмбриональных адвентициальных клеток сосудистой стенки.
Как можно видеть, большинство исследователей так или иначе отмечает определенные взаимоотношения микроглии со стенкой сосуда. Мы в свою очередь в ряде случаев могли наблюдать некоторое сходство ранней фазы формирования строящегося капилляра с первыми стадиями развития мимроглиоцитов, располагающихся еще на станке сосуда.
Это сходство могло бы дать право считать элементы сосудистой станки источником происхождения микроглии лишь в том случае, если бы удалось проследить отхождение клетки, напоминающей клетку микроглии, от материнского сосуда, переход ее в парапластическую субстанцию и дальнейшее превращение этой клетки в мозговом веществе.
Мы не можем исключить возможности «оползания» недиференциро-ванной клетки с сосуда для последующего самостоятельного существования в виде клетки гортеговской глии, поскольку в отдельных случаях подобного рода явления можно наблюдать на наших препаратах. Сравнительная редкость, с которой приходится отмечать этот факт, является результатом избирательной импрегнации сосудистой сети при использовании предлагаемой нами методики.
Лишь тогда, когда в силу тех или иных причин при импрегнации случайно выявляются и другие элементы центральной нервной системы, в том числе и клетки микроглии, можно проследить превращение адвентициальной клетки в клетку гортеговской глии при отделении ее от стенки сосуда.
Отмеченное нами сходство раннего этапа роста мозгового капилляра с микроглиоцитом может указывать на возможность диференциации адвентяциалыной клетки в двух направлениях: в сторону формирования нового капилляра и в сторону превращения в клетку микроглии.
Возвращаясь к начальной стадии строящегося капилляра, мы должны отметить, что с течением времени утолщение стенки капилляра все более увеличивается в размерах и строящийся капилляр приобретает внешнее сходство с начинающей распускаться почкой.
В этой фазе роста мозгового капилляра, названной нами стадией "почки", в плотной массе теперь уже отчетливо выраженного нароста в большинстве случаев наблюдается светлое пятно (рис. 93, б). Форма и размер пятна соответствуют форме и размеру ядра адвентициальной клетки. Сходство с последним дополняется тем, что в просветленном участке строящегося капилляра, как видно на рис. 93, б, различаются хорошо импрегнированные серебром глыбки или толстые нити хроматина, располагающиеся по длинной оси ядра. Характер расположения, а также форма глыбок полностью совпадают с характером расположения и формой таковых в адвентициальной клетке при окраске методом Гей-денгайна.
Что представляет собой описываемое светлое пятно, располагающееся, как мы увидим из дальнейшего изложения, постоянно на переднем конце строящегося капилляра? К описанной выше характеристике этого пятна следует добавить постоянство формы и размера, а также расположение этого образования в дистальной растущей части новообразующе-гоея капилляра, как бы сосредоточивающего в себе энергию роста. Все сказанное выше заставляет нас утверждать, чтоописываемое образование является не чем иным, как ядром клетки строящегося капилляра.
В наиболее дистальном отделе растущего капилляра располагается уплотненная протоплазма, всегда интенсивно импрегнированная, с отходящими от нее во все стороны отростками. При рассматривании последних под большими увеличениями можно видеть, что отростки представляют собой подлинные протоплазменные тяжи, отходящие от растущего конца капилляра во всех плоскостях.
Форма, размер, а также характер расположения отростков на конце капилляра изменчивы даже у декапитированного нормального животного. На стадии «почки» отростки имеют вид очень тонких протоплазмати-ческих тяжей с осевшими на них мельчайшими крупинками серебра. Благодаря последнему обстоятельству, отростки кажутся состоящими из отдельных члеников. По мере роста капилляра отростки становятся несколько плотнее, импрегнируются лучше и все больше увеличиваются в длине. Вместе с увеличением длины они всe больше приобретают характер протоплазматических выростов.
В пользу этого предположения говорит факт импрегнации серебром отростков наряду с растущим капилляром.
Просматривая серии препаратов мезга животных, обработанных различными гистологическими методами, мы нигде не могли обнаружить образований, которые напоминали бы растущие капилляры в том виде, в каком они обнаруживались на импрегнированных препаратах.
Неудачи поисков являются результатом того, что ни один из обычных методов гистологической обработки не выявляет характерного конца растущего капилляра с его отростками.
Избирательная импрегнация отростков одновременно с импрегнацией сосудистой стенки сама по себе является доказательством одного и того же химического состава протоплазмы сосудистой стенки и отростков.
Отростки могут иметь вид прямых тонких тяжей, чаше же всего они характерно изогнуты и напоминают коленчатые лапки паука.
Полученный в нашей лаборатории материал по развитию сосудистой сети с мозгу показал, что своеобразная иногда коленчатая форма протоплазменных отростков растущего капилляра обусловлена проникновением этих отростков в среду с особым характерным расположением основной стромы, где отростки спонгиобластов идут от внутренней к на- ружной поверхности в виде параллельных «струн» (Б. Н. Клосов-
ский, 1949). В отдельных очень редких случаях удается обнаружить раздвоение конца протоплазм этического отросгка в виде рогатки, обычно же они не ветвятся. Изредка встречается своеобразная форма отростка, имеющего на своем конце утолщение, несколько напоминающее присоску.
Сравнение фотографий, представляющих различные фазы роста моз-гового капилляра, позволяет отметить разнообразие в расположении отростков в венчике. На поздних стадиях роста отростки все более отходят друг от друга, раскидываясь во всех плоскостях на большое расстояние.
Растущий конец строящегося капилляра, а именно располагающиеся на. нем отростки, чрезвычайно чувствительны ко всяким изменениям среды, т. е. к изменениям состоянии мозгового вещества. При изменении состояния мозгового вещества отростки меняют не только свою длину, толщину, но и могут резко уменьшаться в числе. Этим обстоятельством объясняется трудность обнаружения строящихся капилляров в мозгу человеческих эмбрионов и новорожденных.
Патологическое состояние мозговой ткани имеет своим следствием ее только искажение морфологической формы отростков, но и полное исчезновение их, благодаря чему становится чрезвычайно трудно обнаружить растущие капилляры в сосудисто-капиллярной сети.
Наблюдение всех нормальных стадий роста мозгового капилляра поэтому возможно лишь в мозгу эмбрионов человека, полученных при кесаревом сечении.
Установление количества отростков на различных стадиях роста капилляра в норме и при патологических состояниях мозга, вследствие расположения их в очень многих плоскостях, чрезвычайно затруднено. Обычно в мозгу нормального животного число их колеблется от 12 до 24. Изучая характер отростков строящегося капилляра, мы вначале по аналогии с ранее изучавшимися нами клетками, сосудистых сплетений и эпендимы предположили, что отрытый являются своеобразным жгутиковым аппаратом, которым обладают эти клетки.
 2015-05-18
2015-05-18 801
801








