Равновесный потенциал водородного электрода при Р=1атм. И 298К:
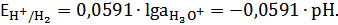 (27)
(27)
Видно, что в интервале рН от 0 до 14 значение 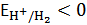 . Если в качестве электрода сравнения используется хлоридсеребряный, потенциал которого
. Если в качестве электрода сравнения используется хлоридсеребряный, потенциал которого
положителен, то напряжение химической цепи
⊖ электрод сравнения | раствор 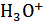 | индикаторный электрод ⊕,
| индикаторный электрод ⊕,
необходимой для потенциометрического определения рН, будет отрицательно. Поэтому правильно поменять электроды местами, составив цепь:
⊖ Ag, Pt(Pt), H2|H3O+¦KCl(нас)¦Cl-|AgCl, Ag  . (Г)
. (Г)
Здесь промежуточный раствор хлорида калия играет роль солевого мостика,
заметно снижающего диффузионный потенциал на каждой из жидкостных границ. Напряжение цепи (Е) (оно теперь положительно) дается выражением:
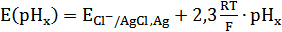 (28)
(28)
Формула (28) может быть использована для оценки рНх, если известно точное значение 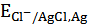 .
.
 2015-05-10
2015-05-10 426
426








