Активность осахаривающих ферментов определяют поляриметрическим методом. Метод основан на определении скорости ферментативной реакции гидролиза крахмала, которая устанавливается по уменьшению угла вращения плоскости поляризации. Это уменьшение возникает за счет образования низкомолекулярных углеводов при действии ферментов на крахмал.
За единицу активности принимают такое количество фермента, которое в строго определенных условиях (рН 4,7-4,9 и температура 50 0С, продолжительность 30 мин) гидролизует1 г крахмала до низкомолекулярных углеводов.
Приборы и оборудование: весы технические, термостат, мясорубка, поляриметр.
Посуда и материалы: стакан стеклянный для взвешивания, мерная колба вместимостью 100 см3 – 2 шт., фильтровальная бумага, воронка пипетки на 10, 1 см3, пробирки большие на 35 см3 или конические колбы на 50 см3– 2 шт; конические колбы на 50 см3– 2 шт.
Реактивы: фосфатный буфер с рН 4,8-4,9 (готовят из двух растворов: 11,876 гNa2HPO4*2H2О в 1 дм3 дистиллированной воды и 9,078 гKH2PO4 в 1 дм3 дистиллированной воды; берут 100 см3 второго раствора и добавляя около 1 см3 первого доводят на рН-метре до значения рН 4,8-4,9) – 100 см3; забуференный 2 %-ный раствор крахмала (2 г растворимого картофельного крахмала помещают в мерную колбу на 100 см3, добавляют 30-40 см3 воды, перемешивают, нагревают в кипящей водяной бане до полного растворения крахмала, охлаждают и добавляют 10 см3 фосфатного буфера и доводят водой до метки) – 40 см3; раствор HCl концентрацией 1 моль/дм3 – 5 см5; 30 %-ный раствор сульфата цинка (ZnSO4) (30 г в 100 см3) – 5 см3; 15 %-ный раствор гексационо-П-феррата калия [K4Fe(CN6)] (17,65 г в 100 см3) – 5 см3.
Расход сырья: свежепроросший солод - 10 г
Техника определения
Для анализа берут 2 пробирки. В одну наливают 20 см3 субстрата (2 %-ный раствор забуференного крахмала) и выдерживают в термостате 10 мин при температуре 50 0С. Затем в нее добавляют 10 см3 ферментного рабочего раствора, приготовленного, как при определении АС, перемешивают и выдерживают в термостате 30 мин. По истечении этого времени пробирку вынимают из термостата, добавляют в нее 1 см3 раствора соляной кислоты концентрацией 1 моль/дм3 для инактивации ферментов. После этого приливают 1 см3 30 %-ного раствора сульфата цинка и после перемешивания 1 см3 15 %-ного раствора гексациано-(П)-феррата калия.
Одновременно готовят контрольную пробу. Для этого в другую пробирку наливают последовательно 10 см3 ферментного раствора, 1 см3 раствора соляной кислоты концентрацией 1 моль/дм3, по 1 см3 30 %-ного раствора ZnSO4 и 15 %-ного раствора K4Fe(CN6) и 20 см3 субстрата.
Содержимое обеих прбирок перемешивают и фильтруют. В фильтратах (контрольном и опытном) определяют величину угла вращения плоскости поляризации при температуре 20 0С, используя поляризационную длиной 200 мм.
После измерения получают 2 значения Пк – контрольного раствора и По - опытного раствора. Разность между значениями величины угла вращения плоскости поляризации контрольного и опытного растворов (П) показывает снижение степени поляризации, которое пропорционально количеству образовавшихся в процессе ферментативной реакции низкомолекулярных углеводов. Значение П должно быть не менее 0,2 0 и не более 2,5 0.
Осахаривающую способность в ед/г (ОС) определяют по формуле 3.5
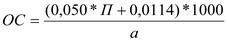 (3.5)
(3.5)
где: 0,050 и 0,0114 – постоянные коэффициенты;
а – масса солода в реакционной среде, мг
П – разность показаний поляриметра контрольного и опытного
растворов.
 2015-05-10
2015-05-10 1212
1212








