Растворы неэлектролитов и электролитов
Вариант 14
1. Какова будет массовая доля (%) HNO3 в растворе, если к 0,200 дм3 32% - ного раствора азотной кислоты (r = 1,198 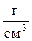 ) прибавить 1 дм3 воды?
) прибавить 1 дм3 воды?
2. При какой температуре (°С) замерзает раствор, содержащий 21,6 г глюкозы (С6Н12О6) в 100 г воды? Криоскопическая постоянная воды К = 1,86.
3. Определите концентрацию (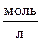 ) катионов натрия в растворе гидроксида натрия, если рН раствора 11.
) катионов натрия в растворе гидроксида натрия, если рН раствора 11.
4. Укажите слабодиссоциирующий электролит: Ba(OH)2; NH4OH; Al(OH)3; LiOH. От чего зависит степень диссоциации?
5. В каком из указанных случаев раствор электролита МХ ненасыщен:
а) [Mz+]×[Xz-] < ПР;
б) [Mz+]×[Xz-] > ПР;
в) [Mz+]×[Xz-] =ПР.
6. Какая из солей подвергается полному гидролизу: FeSO4; (NH4)2S; MgBr2; Bi2(SO4)3? Напишите ионно-молекулярные уравнения гидролиза FeSO4.
Контрольная работа 2
Растворы неэлектролитов и электролитов
Вариант 15
1. Сколько граммов SO3 надо растворить в воде, чтобы получить 400 мл 15% - ного раствор H2SO4 (r = 1,100 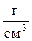 )?
)?
2. Чему равна концентрация раствора уксусной кислоты, рН которой равен 5,2?
3. К раствору H2SO4 медленно добавляют раствор, содержащий CaCl2 и SrCl2. Какой осадок начнёт выпадать раньше: SrSO4 или CaSO4? Почему?
4. Рассчитайте константу диссоциации гидроксида аммония, если степень диссоциации в 2×10-3М растворе NH4OH равна 10%.
5. Какое значение рН (<, > или» 7) имеют растворы солей: K3PO4; ZnCl2; K2SO3; NiCl2; FeCl3? Напишите ионно-молекулярные уравнения гидролиза соли NiCl2.
6. Какие пары ионов можно использовать при составлении молекулярного уравнения, которому соответствует ионно-молекулярное уравнение: Н+ + ОН- ® Н2О:
а) Br- и K+;
б) SO42- и Mg2+;
в) CN- и K+;
г) NO3- и Ba2+?
 2015-05-26
2015-05-26 586
586








