Выбор сборника типа СИ для аптек зависит от объема работы и расхода воды очищенной. Сборники должны иметь четкую надпись: «Вода для инъекций». Если используется одновременно несколько сборников, они нумеруются.
В порядке исключения вода для инъекций может храниться в стерильных стеклянных сборниках (бутылях), которые плотно закрываются пробками (крышками) с двумя отверстиями: одно — для трубки, по которой поступает вода, другое — для стеклянной трубки, в которую вставляется тампон из стерильной ваты для фильтрования воздуха (меняется ежедневно). Приемник в целях защиты от пыли должен быть обязательно заключен в герметический стеклянный бокс. Необходимо тщательно следить за чистотой баллонов, соединительных трубок, по которым поступает вода в сборник.
Обычные стеклянные бутыли с корковыми или притертыми пробками непригодны для хранения воды для инъекций.
Воду для инъекций используют свежеприготовленной или хранят при температуре от 5 до 10 °С. При подготовке запаса воды для инъекций ее необходимо стерилизовать сразу же после перегонки в плотно закрытых сосудах при 120 °С в течение 20 минут или при 100 °С — в течение 30 минут, либо подогревать в сборнике до температуры 80—95 °С в процессе перегонки, сбора и затем сохранять в асептических условиях не более 24 часов.
Проверка качества воды для инъекций. В аптеках качество воды для инъекций проверяется химическими методами ежедневно из каждого баллона в соответствии с требованиями ГФ на отсутствие хлоридов, сульфатов, солей кальция, восстанавливающих веществ, аммиака и угольного ангидрида. Ежеквартально вода для инъекций направляется в контрольно-аналитическую лабораторию для полного химического анализа. В этом случае, кроме вышеупомянутых испытаний, в воде определяют рН, кислотность или щелочность, наличие сухого остатка, нитратов, нитритов, тяжелых металлов.
Бактериологический контроль проводится не реже двух раз в квартал. В 1 мл воды очищенной, используемой для приготовления растворов для инъекций сразу же после перегонки, предельно допустимое содержание микроорганизмов не должно превышать 10—15 колоний.
Ежеквартально вода для инъекций контролируется на пиро-генность, так как исследование на восстанавливающие вещества с калия перманганатом не может указывать на отсутствие пироген-ных веществ.
В соответствии с ФС 42-2620—89 вода для инъекций проверяется на отсутствие видимых механических включений. Испытание проводят в соответствии с РД 42У-001—93.
Вода деминерализованная (обессоленная) — Aqua deminiralisata (см. главу 13).
Жирные масла (Olea pinguid). Для приготовления инъекционных растворов используют абрикосовое, миндальное и персиковое масла, которые имеют незначительную вязкость, что особенно важно для прохождения их через узкий канал иглы. Обычно масла используют в тех случаях, когда лекарственное вещество не растворимо в воде или для пролонгированного действия лекарственных веществ.
Масло персиковое (Oleum Persicorum) — прозрачная жидкость светло-желтого цвета, без запаха или со слабым своеобразным запахом приятного маслянистого вкуса. На воздухе не высыхает, растворимо в абсолютном спирте этиловом, легкорастворимо в эфире, хлороформе. При температуре -10 °С масло не должно застывать, оставаясь жидким и прозрачным; допускается лишь появление тонкой пленки на поверхности. Применяется для приготовления инъекционных растворов камфоры, дезоксикортикостерона ацетата, диэтилстиль-бестрола пропионата, ретинола ацетата, синэстрола.
Масло оливковое (Oleum Olivarum) — прозрачная маслянистая жидкость светло-желтого или золотистого цвета, без запаха или со слабым своеобразным запахом, непрогорклого вкуса. На воздухе не высыхает, не дает осадка даже при продолжительном отстаивании при 15 °С, образуя прозрачные растворы. Применяется для приготовления 20 %-ного раствора камфоры, 2 %-ного раствора синэстрола и др.
Масло миндальное (Oleum Amygdalarum) — прозрачная жидкость желтоватого цвета без запаха, приятного маслянистого вкуса. На воздухе не высыхает. При температуре -10 °С не должно застывать, оставаясь жидким и прозрачным. Растворимо в 60 частях абсолютного спирта, легкорастворимо в эфире и хлороформе.
Этилолеат (Aethylii oleas) — это сложный эфир ненасыщенных кислот с этанолом: СН3...(СН2)7...СН=СН..{СН2) r..CO...O...C 2Н5. Обладает большей растворяющей способностью, чем растительные масла, меньшей вязкостью, имеет постоянный химический состав, легко проникает в ткани, хорошо рассасывается, сохраняет однородность при пониженной температуре. В этилолеате хорошо растворяются витамины, гормональные вещества. Он также применяется как добавка к масляным растворам для увеличения растворимости лекарственных веществ и понижения вязкости раствора.
Комплексные растворители. Для приготовления инъекционных растворов применяют неводные растворители как индивидуальные, так и смешанные. В качестве комплексных растворителей могут быть использованы спирт этиловый, глицерин, пропиленгликоль, спирт бензиловый, бензилбензоат и другие, разрешенные к медицинскому применению. Они позволяют приготовить инъекционные растворы нерастворимых или нестабильных в воде лекарственных веществ. При приготовлении инъекционных растворов на неводном растворителе необходимо учитывать свойства растворителя, его способность смешиваться с водной средой, высвобождать лекарственные вещества, резорбцию его организмом, фармакологическое действие и ряд других факторов. Если неводный растворитель не смешивается с водой, то после введения в результате контакта с тканями организма происходит выделение лекарственного вещества, которое более или менее быстро резорбируется организмом. В этом случае неводный растворитель является «носителем» лекарственного вещества. Если же неводный раствор смешивается с водной средой, то после введения лекарственное вещество, оставаясь в растворе, постепенно диффундируют в ткани организма.
Для приготовления инъекционных растворов применяют смешанные неводные растворители, такие, как водно-глицериновые, спир-то-водно-глицериновые, смеси растительных масел с бензилбензоа-том, этилолеатом и др., которые обладают большей растворяющей способностью, чем каждый растворитель в отдельности. Сораствори-тели используются для растворения таких веществ, как гормоны, витамины, антибиотики, барбитураты и др.
ОРГАНИЗАЦИЯ РАБОТЫ В АСЕПТИЧЕСКИХ УСЛОВИЯХ
Источниками загрязнения стерильных растворов могут быть исходные вещества, окружающая среда, оборудование, тара, укупорочный материал, работающий персонал.
> Асептика — это определенные условия работы, комплекс организационных мероприятий, позволяющих в максимальной степени предохранить лекарства от попадания в них микроорганизмов.
Асептика включает в себя ряд последовательных мероприятий, дополняющих друг друга, и ошибка, допущенная в одном звене этого ряда, сводит на нет всю проведенную и последующую работу.
Асептические условия предусматривают наличие в аптеке особого помещения для приготовления стерильных и асептических лекарств — асептического блока, который должен иметь не менее трех комнат:
1. Предасептическая (шлюз) — предназначена для подготовки персонала к работе.
2. Асептическая — предназначена для приготовления лекарственных форм.
3. Аппаратная — в ней устанавливаются автоклавы, стерилизаторы, аппараты, позволяющие получать воду для инъекций.
Требования к помещению. Производство лекарств в асептических условиях осуществляется в «чистых» помещениях, в которых нормируется чистота воздуха по содержанию микробных и механических частиц.
Асептический блок обычно располагается вдали от источников загрязнения микроорганизмами (зала обслуживания больных, моечной, фасовочной, санитарного узла).
В помещениях для приготовления лекарств в асептических условиях стены должны быть окрашены масляной краской или выложены светлой кафельной плиткой, при этом не должно быть выступов, карнизов, трещин. Потолки окрашиваются клеевой или водоэмульсионной краской. Полы покрываются линолеумом или релином с обязательной сваркой швов. Двери и окна должны быть плотно подогнаны и не иметь щелей.
Асептический блок оборудуется приточно-вытяжной вентиляцией с преобладанием притока воздуха над вытяжкой. Для снижения микробной обсемененности рекомендуется установка воздухоочистителей, которые обеспечивают эффективную очистку воздуха фильтрацией через фильтры из ультратонких волокон и ультрафиолетовое облучение.
Для обеззараживания воздуха в асептическом блоке устанавливаются неэкранированные бактерицидные облучатели: настенные (ОБН-150), потолочные (ОБП-300), передвижные маячного типа (ОБПЕ-450); бактерицидные лампы БУВ-25, БУВ-30, БУВ-60 из расчета мощности 2—2,5 Вт на 1 м3 объема помещения, которые включают на 1—2 часа до начала работы в отсутствие людей. Включатель для этих облучателей должен находиться перед входом в помещение и сблокирован со световым табло «Не входить, включен бактерицидный облучатель». Вход в помещение, где включена неэкранированная бактерицидная лампа, разрешается только после ее выключения, а длительное пребывание в указанном помещении — только через 1 5 минут после отключения неэкранированной бактерицидной лампы.
В присутствии персонала могут эксплуатироваться экранированные бактерицидные облучатели, которые устанавливаются на высоте 1,8—2 м, из расчета 1 Вт на 1 м3 помещения при условии исключения направленного излучения на находящихся в помещении людей.
Поскольку ультрафиолетовые облучатели образуют в воздухе токсические продукты (озон и оксиды азота), при их работе вентиляция должна быть включена.
Все оборудование и мебель, вносимые в асептический блок, предварительно обрабатываются салфетками, смоченными дезинфицирующим раствором (раствор хлорамина Б 1 %-ный, раствор хлорамина Б 0,75 %-ный с 0,5% моющего средства, раствор перекиси водорода 3 %-ный с 0,5% моющего средства). Хранение в асептическом блоке неиспользуемого оборудования категорически запрещается. Уборка асептического блока проводится не реже одного раза в смену с использованием дезинфицирующих средств.
Один раз в неделю проводится генеральная уборка асептического блока. При этом помещения по возможности освобождают от оборудования, моют и дезинфицируют стены, двери, полы. После дезинфекции облучают ультрафиолетовым светом.
Перед входом в помещение асептического блока должны быть резиновые коврики, которые один раз в смену смачиваются дезинфицирующим раствором. Асептический блок отделяется от других помещений аптеки воздушными шлюзами.
Требования к персоналу. Лица, участвующие в приготовлении лекарств в асептических условиях, должны соблюдать строгим образом правила личной гигиены. При входе в шлюз они должны обуть специальную обувь, вымыть руки с мылом и щеткой, надеть стерильный халат, 4-слойную марлевую повязку, шапочку (при этом волосы тщательно убрать), бахилы. Оптимальным является применение шлема и комбинезона. Марлевая повязка должна меняться каждые 4 часа. После надевания стерильной технологической одежды персонал должен ополоснуть руки водой для инъекций и обработать их дезинфицирующим раствором спирта этилового 80 %, раствором хлоргексидина биглюконата в 70 % спирте этиловом или 0,5 %-ным раствором хлорамина Б (при отсутствии других веществ). Вход из шлюза в помещение для приготовления и фасовки лекарств в асептических условиях в нестерильной санитарной одежде запрещен. Запрещается также выходить за пределы асептического блока в стерильной санитарной одежде.
Санитарная одежда, халаты, марля, изделия из текстиля, вата стерилизуются в биксах в паровых стерилизаторах при температуре 132 °С в течение 20 минут или при 120 °С в течение 45 минут и хранятся в закрытых биксах не более 3 суток. Обувь перед началом и после окончания работы дезинфицируют снаружи и хранят в шлюзах. Лица с инфекционными заболеваниями, открытыми ранами на коже, носители патогенной микрофлоры до полного их выздоровления не должны допускаться к работе.
Требования к исходным веществам и материалам. Лекарственные вещества, необходимые для приготовления лекарств в асептических условиях, хранятся в шкафах в плотно закрывающихся штан-гласах в условиях, исключающих их загрязнение. Штангласы перед каждым заполнением моются и стерилизуются.
Для приготовления инъекционных лекарственных форм используют лекарственные вещества квалификации «химически чистый», «чистый для анализа» или «годен для инъекций», отвечающие требованиям нормативно-технической документации и ГФУ.
Однако к некоторым препаратам сорта «годен для инъекций» предъявляются дополнительные требования по качеству (табл. 29).
Вспомогательные вещества (стабилизаторы, солюбили-заторы, консерванты) по качеству также должны соответствовать требованиям нормативно-технической документации.
В качестве стабилизаторов инъекционных лекарственных форм используются следующие вещества:
Глицерин высший сорт ГОСТ 6824—76.
Трилон Б ч.д.а., ГОСТ 10652—75.
Калия метабисульфит ч.д.а., ГОСТ 5713—75.
| Перечень лекарственных веществ, к которым предъявляются дополнительные требования |

Кислота хлористоводородная х.ч., ч.д.а., ГОСТ 3118—77, ГФ X, ст. 17. Кислота лимонная х.ч., ч.д.а., ГОСТ 3652—69.
Натрия ацетат х.ч., ч.д.а., ГОСТ 199—78. Натрия гидроксид х.ч., ч.д.а., ГОСТ 4328—77.
Натрия йодид двуводный х.ч., ч.д.а., ГОСТ 8422—76, ГФ X, ст. 133. Натрия хлорид х.ч., ГОСТ 4233—77, ГФ X, ст. 426. Натрия метабисульфит ч.д.а., ГОСТ 10575—76. Натрия сульфит безводный ч.д.а., ГОСТ 195—66.
Спирт этиловый высшей очистки, ГОСТ 5962—67, первый сорт, ГФ X,
ст. 631.
Натрия гидрокарбонат х.ч., ч.д.а., ГОСТ 4201—79, ГФ X, ст. 430.
Вспомогательный материал (вата, марля, пергаментная бумага, фильтры и т. п.) стерилизуется в биксах или банках с притертыми пробками при температуре 132 °С в течение 20 минут или при 120 °С в течение 45 минут и хранится в закрытом виде не более 3 суток. Вскрытые материалы должны использоваться в течение 24 часов. После каждого забора материала бикс плотно закрывается. Забор производится стерильным пинцетом. При этом следует иметь в виду, что вспомогательный материал должен укладываться для стерилизации в биксы в готовом к применению виде.
Упаковка. Загрязнение растворов механическими частицами и микроорганизмами можно снизить путем качественной подготовки тары и укупорочных средств, а также соблюдением условий их хранения и транспортировки непосредственно на место разлива раствора. Аптечная посуда моется (посуда, бывшая в употреблении, предварительно дезинфицируется, затем моется) и стерилизуется, укупоривается и хранится в плотно закрывающихся шкафах, выкрашенных изнутри светлой масляной краской или покрытых пластиком (см. с. 100).
При мытье посуды, кроме удаления механических примесей, необходимо возможно полнее удалить растворимые щелочные соединения, которых особенно много в щелочном стекле. Мытье посуды с применением мыла мало пригодно, так как при этом может быть образование нерастворимого кальциевого мыла, загрязняющего стекло. Моющие и дезинфицирующие средства представлены в главе 8. Посуду моют вручную с помощью ерша или моечных машин, описание которых приведено в главе 10. Чистота вымытой посуды и полнота смывае-мости моющих средств должна контролироваться (см. главу 8, с. 104).
Инъекционные растворы, приготовляемые в аптеках, необходимо отпускать во флаконах из нейтрального стекла марки НС-1 (для медпрепаратов, антибиотиков) и НС-2 (сосуды для крови). В порядке исключения после освобождения от щелочности используют флаконы из стекла марки АВ-1 и МТО, учитывая, что срок хранения растворов в них не должен превышать 2 суток, так как возможно выщелачивание стекла (см. главу 8, с. 96).
Для укупорки флаконов с инъекционными растворами используют пробки специальных сортов резины (с. 99—100): ИР-21 (силиконовая), 25П (натуральный каучук), 52-369, 52-369/I, 52-369/II (бутиловый каучук), ИР-119, ИР-119А (бутиловый каучук). В зарубежной литературе имеются сообщения о применении для укупорки инъекционных растворов пробок из поливинилхлорида.
Обработка, мытье и стерилизация пробок и алюминиевых колпачков представлены в главе 8, с. 103—104.
Требования к производственному оборудованию. Применение средств малой механизации при приготовлении растворов для инъекций допускается при условии возможности их обеззараживания или стерилизации (см. главу 10). Оборудование должно быть сконструировано и размещено так, чтобы обеспечивалась его подготовка к работе, эксплуатации и обслуживанию. Материал, из которого сделано оборудование, не должен вступать в реакцию с компонентами лекарства, а конструкция оборудования должна исключать возможность попадания в лекарство веществ, используемых для его эксплуатации (смазочные вещества, охлаждающие жидкости и т. п.).
Оборудование и инструменты необходимо регулярно подвергать профилактическим осмотрам, мыть, обрабатывать дезсредствами или стерилизовать. Оборудование должно эксплуатироваться таким образом, чтобы свести к минимуму возможность загрязнения микроорганизмами готовых лекарств. Стерилизаторы должны быть снабжены устройствами, автоматически регистрирующими время и температуру стерилизации.
СТЕРИЛИЗАЦИЯ
> Стерилизация (или обеспложивание) — это процесс полного уничтожения микроорганизмов и их спор в лекарственных веществах, лекарственных формах, на посуде, вспомогательных материалах, инструментах и аппаратах.
Термин «стерилизация» происходит от лат. sterilis, что означает бесплодный. Стерильность достигается соблюдением асептики и применением методов стерилизации в соответствии с требованиями ГФУ «Методы и условия стерилизации», ранее в ГФ XI — статья «Стерилизация».
При выборе метода и продолжительности стерилизации необходимо учитывать свойства, объем или массу стерилизуемых материалов.
Методы стерилизации можно разделить на: физические, механические, химические.
Физические методы стерилизации. К ним относятся: термическая, или тепловая, стерилизация, стерилизация ультрафиолетовыми лучами, радиационная стерилизация, стерилизация токами высокой частоты.
Из перечисленных методов в условиях аптек применяются термическая стерилизация, а также стерилизация ультрафиолетовыми лучами. Остальные методы стерилизации в условиях аптек пока не нашли применения.
Термическая стерилизация. При этом методе стерилизации происходит гибель микроорганизмов под влиянием высокой температуры за счет коагуляции белков и разрушения ферментов микроорганизмов. Наиболее широко в аптечной практике применяется стерилизация сухим жаром и паром.
Стерилизация сухим жаром осуществляется сухим горячим воздухом в воздушных стерилизаторах при температуре 180—200 °С. Эффективность стерилизации зависит от температуры и времени. Равномерность прогрева объектов обусловливается степенью их теплопроводности и правильностью расположения внутри стерилиза-ционной камеры для обеспечения свободной циркуляции горячего воздуха. Стерилизуемые объекты должны быть расфасованы в соответствующую тару, плотно укупорены и свободно размещены в сушильных шкафах, чтобы обеспечить быстрое и равномерное проникновение к ним горячего воздуха. Загрузка должна производиться в ненагретые сушильные шкафы или когда температура внутри шкафа не превышает 60 °С. В связи с тем, что горячий воздух обладает невысокой теплопроводностью, прогрев стерилизуемых объектов происходит довольно медленно. Время, рекомендуемое для стерилизации, должно отсчитываться с момента нагрева воздуха в сушильном шкафу до температуры 180—200 °С.
Воздушный метод используется для стерилизации термостойких порошкообразных лекарственных веществ (натрия хлорид, цинка оксид, тальк, глина белая и др.). Порошки массой более 200,0 г стерилизуют при 180 °С в течение 60 минут или при 200 °С — 30 минут. При этом толщина слоя порошка должна быть не более 6—7 см. Время стерилизационной выдержки порошков массой менее 200,0 г соответственно уменьшают до 30—40 минут при 180 °С и до 10— 20 минут — при 200 °С.
Минеральные и растительные масла, жиры, ланолин безводный, вазелин, воск стерилизуют горячим воздухом при 180 °С в течение 30—40 минут или при 200 °С — 15—20 минут с учетом количества вещества.
Изделия из стекла, металла, силиконовой резины, фарфора, установки для стерилизующего фильтрования с фильтрами и приемники фильтрата стерилизуют при 180 °С в течение 60 минут.
Мелкие стеклянные и металлические предметы (воронки, пипетки и др.) помещают в сушильные шкафы в специальных биксах.
Для сохранения стерильности посуды, если она не используется сразу же после обеспложивания, ее перед стерилизацией плотно закрывают стеклянными или ватными пробками, обернутыми в марлю. В порядке исключения простерилизованную посуду можно закрывать пробками в асептических условиях сразу же после стерилизации, пока флаконы и колбы горячие.
Растворы лекарственных веществ нельзя стерилизовать в сушильных шкафах, так как из-за плохой теплопроводности воздух, имеющий температуру 100—120 °С, не обеспечивает быстрый нагрев растворов до температуры стерилизации. Так, например, раствор натрия хлорида (объем 200 мл), помещенный в сушильный шкаф с температурой 120 °С, через час прогревается всего лишь до 60 °С. Горячий воздух более высокой температуры может вызвать разложение лекарственных веществ и разрыв склянок вследствие разницы давлений внутри и снаружи флаконов.
Для стерилизации сухим горячим воздухом в аптеках целесообразно использовать шкафы сушильно-стерилизационные марки ШСС-250П, стерилизатор сухожаровой СС-200, а также воздушные стерилизаторы с небольшим объемом стерилизационной камеры марок ВП-10, ГП-20 и ГП-40. В крупных больничных аптеках имеются сушильно-стерилизационные шкафы ШСС-500П и ШСС-1000П.
Таблица 30
Стерилизационное оборудование для воздушной стерилизации
Тип
Техническая характеристика
 |
Шкаф сушильный электрический круглый АВ-151
Шкаф сушильно-стерили-зационный ШСС-80П
Шкаф сушильно-стерили-зационный ШСС-250П
Шкаф сушильно-стерили-зационный проходной ШСС-250ПР
Шкаф сушильно-стерили-
зационный ШСС-500П
Шкаф сушильно-стерили-зационный проходной
ШСС-500ПР
Шкаф сушильно-стерили-
зационный ШСС-1000П
Шкаф сушильно-стерили-зационный проходной
ШСС-1000ПР
Технические характеристики рекомендуемых шкафов приведены в табл. 30.
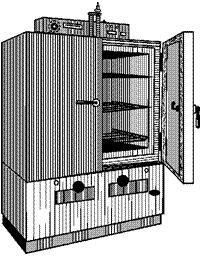
На рис. 136 изображен наиболее широко применяемый в больничных аптеках шкаф сушильно-стерилизационный ШСС-500П.
 |
Стерилизация паром основана на сочетании высокой температуры и влаги. Коагуляция белковых веществ в этих условиях начинается при температуре 56 °С. В фармацевтической практике применяют несколько методов стерилизации паром, из которых наиболее надежный, быстрый и экономичный — стерилизация насыщенным водяным паром под давлением 0,11 МПа (1,1 кгс/см2) и температуре 120 °С; 0,20 МПа (2 кгс/см2) и температуре 132 °С. В этих условиях погибают не только веге-
тативные, но и споровые формы Рис. 136. Шкаф сушильно-
микроорганизмов. стерилизационный ШСС-500П
Паровой метод стерилизации при 120 °С рекомендуется для воды и водных растворов лекарственных веществ. Время стерилизацион-ной выдержки не более 30 минут в зависимости от физико-химических свойств препарата и объема раствора. Растворы объемом до 100 мл стерилизуют в течение 8 минут, объемом 101—500 мл — 8—12 минут и объемом от 501 до 1000 мл — 12—15 минут.
Стерилизация воды и водных растворов производится в герметично укупоренных и предварительно простерилизованных флаконах или ампулах. Жиры и масла в герметично укупоренных сосудах стерилизуют при 120 °С в течение 2 часов. Этим методом стерилизуют также изделия из стекла, фарфора, металла, резины, перевязочные и вспомогательные материалы (вату, марлю, бинты, халаты, фильтровальную бумагу, резиновые пробки, пергамент и др.). Время стерилизационной выдержки 45 минут.
Установки для стерилизующего фильтрования с фильтрами стерилизуют 15 минут (для фильтров диаметром 13 и 25 мм), 30 минут (для фильтров диаметром 47, 50, 90 и 142 мм) и 45 минут (для фильтров диаметром 293 мм).
Для стерилизации хирургических инструментов, перевязочных материалов, белья и спецодежды также может быть рекомендован метод стерилизации паром при 132 °С в течение 20 минут. Стерилизация указанных объектов должна производиться в стерилизацион-ных коробках или двухслойной мягкой упаковке из бязи либо в пергаментной бумаге.
Стерилизацию паром под давлением проводят в паровых стерилизаторах (автоклавах) различной конструкции. Наиболее удобны те паровые стерилизаторы, в которых автоматически поддерживаются заданные давление и температура, а также предусмотрена
|
возможность просушивать вспомогательный материал (вату, фильтровальную бумагу, марлю и др.) после стерилизации (табл. 31).
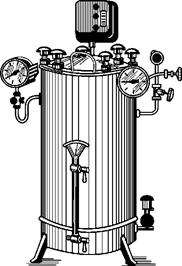
В настоящее время широкое распространение получили стерилизаторы типа ВК-15, ВК-30
(рис. 137), ГП-280 и др. В практике больничных аптек могут быть использованы также стерилизаторы типа ГП-400, ГПД-280
и ГПС-500, которые по устройству и принципу действия аналогичны стерилизатору ГП-280.
Вертикальные паровые стерилизато-
ры ВК-30 и ВК-75 отличаются емкостью
стерилизационной камеры. Состоят они
из корпуса со стерилизационной и водо-
паровой камерами, крышки, кожуха,
электронагревательных элементов, элект-
Рис. 137. Стерилизатор вертикальный рощита, электроконтактного манометра,
круглый электрический ВК-30 мановакуумметра, эжектора, предохра-
Таблица 31
Стерилизаторы паровые
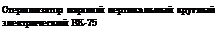

Стерилизатор паровой горизонтальный прямоугольный электрический шкафного типа ГП-400
Стерилизатор паровой с автоматическим управлением ГП-560
Стерилизатор паровой электрический горизонтальный прямоугольный двусторонний с автоматическим управлением ГПД-400
Стерилизатор паровой полуавтоматический двухсторонний ГПД-560
Установка стерилизационная ЦСУ-1000-0. По требованию заказчика может быть укомплектована шкафом сушильно-стерилизационным марки ШСС-500ПР и различным количеством паровых стерилизаторов и загрузочных тележек
Объем камеры 560 л. Габаритные размеры 1620x420x1800 мм. Имеет три режима стерилизации.
Представляет собой комплекс паровых стерилизаторов с двусхторонним обслуживанием, автоматическим управлением и загрузочно-выгрузоч-ным устройством. Пароснабжение от собственного электрического парогенератора. Три паровых стерилизатора каждый объемом 750 л, 6 загрузочных тележек, 8 контейнеров. Оснащена программным устройством по контролю экспозиции и температуры стерилизации.
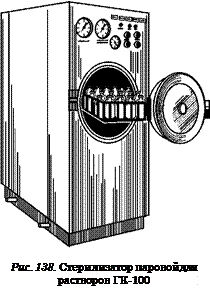
нительного клапана, водоуказательной колонки и трубопровода с вентилями. Стерилизационная и водопаровая камеры объединены в единую сварную конструкцию, но разобщены функционально, в результате чего можно перекрывать поступление пара в стерилизационную камеру во время загрузки, эжекции и разгрузки автоклава, а также автоматически поддерживать рабочее давление в во-допаровой камере для выполнения последующей стерилизации. Обе камеры выполнены из нержавеющей стали. Максимальное давление пара в стерилиза-ционной камере 0,25 МПа. Оба стерилизатора работают от сети трехфазного переменного тока напряжением 220/380 В. Паровые стерилизаторы ВКО-50 и ВКО-75 отличаются размерами стерилизационной камеры, рабочее давление в которых не должно превышать 0,2 МПа. Стерилизацию можно проводить как под давлением, так и текучим паром. Паровой стерилизатор ВКО-16 переносного типа предназначен для стерилизации текучим паром.Горизонтальный паровой стерилизатор ГК-100 рассчитан на работу при максимальном давлении пара 0,2 МПа. Основные части его — стерилизационная и водопаровая камеры, парообразователь с электронагревательными элементами, крышка, кожух и электрощит. Внутри водопаровой камеры расположена стерилизационная. Пар из парообразователя поступает в паровую камеру, а затем в стерилизационную. Образующийся в процессе работы конденсат стекает в парообразователь, который снабжен предохранительным клапаном, манометром и водоуказательной колонкой с воронкой для залива воды. Заполнение парообразователя водой может осуществляться как вручную через воронку, так и от водопроводной магистрали через специальный патрубок, снабженный вентилем. Работает стерилизатор от сети трехфазного переменного тока напряжением 220/380 В (рис. 138).
Паровой стерилизатор ГП-280 работает в автоматическом цикле и имеет четыре режима стерилизации, отличающихся различной продолжительностью (от 20 до 30 минут) и давлением пара в стерилизационной камере (от 0,1 до 0,2 МПа). Стерилизатор состоит из стерилизационной камеры с дверцей, парогенератора, электронасоса и электрощита. Дверца камеры снабжена центральным затвором и имеет блокировку мембранного типа, которая предотвращает возможность ее открывания при избыточном давлении пара внутри камеры. На панели управления стерилизатора имеются манометр, вакуумметр, водомерное стекло и кнопки управления. Парогенератор выполнен в виде котла с теплоизолирующим кожухом, снабженного предохранительным клапаном, термис-тором, манометром, датчиком уровня и водоуказательной колонкой.
 2014-02-17
2014-02-17 618
618








