Мольная доля NА вещества в растворе равна отношению числа молей данного вещества к общему числу молей всех веществ, содержащихся в растворе:
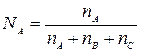 ,
, 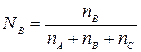 ,
,
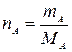 ;
; 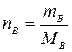 и т.д.
и т.д.
Сумма молярных долей всех компонентов должна быть равна единице:
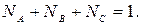
И, наконец, рассмотрим пример смешивания раствора разных концентраций и расчеты, связанные с этим.
Пример. Сколько граммов 20 %-ного раствора КОН надо прибавить к 250 г 90 %-ного раствора, чтобы получить 50 %-ный раствор КОН?
Решение.
Эта задача решается с помощью правила смешения. Массу 20 %-ного раствора КОН обозначим через X; тогда
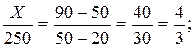

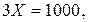
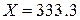 г.
г.
Для получения 50 %-ного раствора КОН к 250 г 90 %-ного раствора надо прибавить 333,3 г 20 %-ного раствора КОН.
Задачи такого типа легко решаются при помощи «диагональной схемы» или «правила креста».
Диагональная схема строится так: точкой пересечения двух отрезков прямой обозначают свойства смеси. У концов обоих отрезков, расположенных по одну сторону от точки пересечения, обозначают свойства компонентов смеси, а у других концов отрезков – разности между свойствами смеси и свойствами ее компонентов. «Диагональная схема» для этого примера имеет вид:
20 40



 |  |
Х 30
Количества исходных растворов, необходимые для приготовления смеси, обратно пропорциональны разностям между концентрациями заданного и менее концентрированного растворов и более концентрированного и заданного раствора:
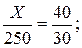
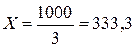 г.
г.
 2015-01-07
2015-01-07 1433
1433
