Одна тонна черновой меди содержит 300-1000 г серебра, 30-100 г золота. Затраты на рафинирование окупают все расходы и дают значительный экономический эффект, поэтому рафинируют более 90% черновой меди. Везде применяют сернокислотные электролиты близкого состава: Сu2+ - 30-50 г/л, Н2SJ4 - 120-200 г/л с добавками активатора (Cl- - 0,01-0,04 г/л) и ПАВ (желатин 50-100 г/т, либо столярный клей 40-45 г/т, либо тиомочевина 50-90 г/т).
Серная кислота повышает электропроводность электролита, снижает энергозатраты. Однако при больших концентрациях возможна пассивация анода, приводящая к его значительной поляризации, ионизации серебра и его потерям с катодной медью. На аноде имеют место 2 процесса:
Сu - 2е = Сu2+ (ЕoCu2+/Cu = 0,344 В) (4.1)
Сu - е = Сu+ (ЕoCu+/Cu = 0,522 В) (4.2)
Превалирующим является процесс (4.1). В равновесных условиях соотношение концентраций ионов Сu2+ и Сu+ близко к 1000. Однако при анодном растворении оно значительно смещается в сторону образования Cu+ из-за стадийного протекания реакции (4.1). Одновалентная медь взаимодействует в объеме электролита с серной кислотой по реакции:
Cu2SO4 + 1/2О2 +H2SО4 = 2CuSО4 +H2О (4.3)
Это приводит к уменьшению концентрации H2SО4 и электропроводности электролита, его перегреву, к еще большему превышению убыли анода над привесом катода (Dm,%).
Зависимость Dm,%,от температуры
t,°C 20 50 70
Dm% 1,0 2,3 5,3
Для того чтобы избежать этого нежелательного явления, в серии электролизеров делают несколько регенеративных ванн (1,5-2,5%). Их назначение - регенерировать (восстановить) первоначальный состав электролита. Анодом в регенеративных ваннах являются свинец или его сплав с 1% серебра. Анод должен работать в режиме нерастворимого анода с выделением на нем кислорода по реакции
Н2О - 2е = 2Н+ + 1/2О2 (4.4)
На катоде происходит разряд ионов меди:
Cu2+ + 2e = Cu (4.5)
Сложив уравнения (4.4) и (4.5), получаем суммарную реакцию, реализующуюся в регенеративных ваннах:
CuSО4 + Н2О = Сu + 1/2О2 + H2SО4 (4.6)
Выделяющийся газообразный кислород ухудшает атмосферу в цехе за счет образования аэрозолей серной кислоты при схлопывании пузырьков.
Для предотвращения образования аэрозолей поверхность электролита покрывают маслами либо полиэтиленовыми шариками.
Ниже показано распределение примесей, содержащихся в анодной меди, между шламом, электролитом и катодной медью, % мас.
_________________________________________________
Ag Au Se,Te Pb Ni As Sb
_________________________________________________
В шламе 97,7 98,6 97,6 98,3 3,7 24,7 68,4
В электролите - - - - 94,9 73,8 30,4
В катодной
меди 2,3 1,4 2,4 1,7 1,4 1,5 2,0
_________________________________________________
Содержание Se, Те, Pb, Ni, As, Sb в анодной меди находится на уровне (0,01-0,05) мас.%.
Условия электрорафинирования меди следующие:
Ток серии - 10000 A
Катодная плотность тока 240-280 А/м2
Катодный выход по току 92-95%
Напряжение на ванне 0,2-0,4 В
Расход электроэнергии 200-380 кВт×ч/т
Температура электролита 55-60°С
При интенсивной циркуляции электролита удается повысить плотность тока до 500-700 А/м2.
В результате получают рафинированную медь и шлам. На медь существует ГОСТ 859-66, регламентирующий содержание основного металла:
Марка меди по ГОСТ 859-66 М-4 М-3 М-2 М-1 М-0
Содержание меди,% 99,0 99,5 99,7 99,9 99,95
Средний состав шлама Элемент
Сu Ag Au Sb Pb Se Те
Содержание в шламе, % 20-50 9-35 0,3-4 5-12 1-10 2-20 0,5-5
Шлам представляет собой ценнейшее сырье для получения серебра, золота, селена и теллура. Для этого шлам вначале подвергают сульфатизирующему отжигу:
Cu + H2SО4 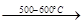 CuSО4 + H2 (4.7)
CuSО4 + H2 (4.7)
Содержание меди в шламе при этом снижается до 0,5-4,5%.
Далее шлам плавят под флюсом (SiО2, Na2CO3, селитра) в отражательной печи с получением сплава, %: 80-90Ag, 2-12 Au, 1-4 Сu (так называемый металл Дорэ). Металл Дорэ отливается в аноды размером 250х150х15 мм и направляется на афинажные заводы для электрорафинирования серебра, если проба золота меньше 300 (проба 1000 соответствует 100%), или электрорафинирования золота, если содержание серебра меньше 200 проб.
Шихтовкой стремятся уменьшить пробу второго металла.
 2015-05-22
2015-05-22 1709
1709








