степень свободы.
18. При очистке воздуха активированным углем при 40°С протекают реакции: 2H2S(г) + О2(г) = 2H2O(г) + S2(г)
СS(г) + О2(г) = CO2(г) + 2S(г)
Применить к этой системе правило фаз.
19. Приведите примеры однокомпонентных систем состоящих из одной, двух, трех фаз.
20. Приведенные равновесия при 500°С смещены вправо
COS(г) + H2O(г) = CO2(г) + H2S(г)
CS2(г) + 2H2O(г) = CO2(г) + 2H2S(г)
Примените здесь правило фаз.
21. Возможно ли существование однокомпонентной системы, состоящей из четырех фаз?
22. Приведите примеры двухкомпонентных систем, состоящих из одной, двух, трех и четырех фаз.
23. Возможно ли существование пяти фаз в двухкомпонентной и трехкомпонентной системе?
24. Определить фазовый состав и степень свободы системы при 500°С и 1500°С.

 2FeS(тв) 2Fe(тв) + S2(г)
2FeS(тв) 2Fe(тв) + S2(г)
25. При 500-600°С в системе, состоящей из железа, его окислов и кислорода, возможно существование равновесий:
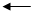
 2Fe3O4(тв) 6FeO(тв) + О2(г)
2Fe3O4(тв) 6FeO(тв) + О2(г)
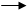 Fe3O4(тв) 3Fe(тв) + 2О2(г)
Fe3O4(тв) 3Fe(тв) + 2О2(г)


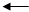 2FeO(тв) 2Fe(тв) + О2(г)
2FeO(тв) 2Fe(тв) + О2(г)
Применить к данной системе правило фаз.
26. В процессах водоочистки большую роль играет коагулирование коллоидных примесей, при этом протекает реакция
Al2(SO4)3(aq) + 3Ca(HCO3)2(aq) = 3CaSO4(тв) + 6CO2(г) + 2Al(OH)3(тв)
Определить фазовый состав и степень свободы системы.
27. Применить правило фаз к системе
NaCl(aq) + CO2(г) + NH3(г) + H2O(ж) = NH4Cl(aq) +NaHCO3(TB)
28. Фосфор получают восстановлением и возгонкой его в электрической печи из шихты, содержащей фосфорнокислый кальций (апатит или фосфорит), кокс и песок. Процесс протекает по уравнению
2Ca3(PO4)2(тв) + 10C(тв) + 6SiO2(тв) = P4(г) + 10СО(г) + 6СaSiO3(тв)
Определить число фаз, число независимых компонентов и степень свободы этой системы; какие из параметров можно изменять произвольно, не изменяя фазового состава системы?
29. Временная жесткость воды связана с наличием в ней растворимых солей
Сa(HCO3)2 и Mg(HCO3)2. При кипячении воды эти соли выпадают в осадок, при этом протекают реакции:
Сa(HCO3)2 = СaCO3(тв) + CO2(г) + H2О(ж)
2Mg(HCO3)2 = (MgOH)2CO3 (тв) + 3CO2(г) + H2О(ж)
Определить фазовый состав системы, число независимых компонентов и степень свободы.
30. В стеклоплавильных печах протекают реакции:
MgCO3(тв) + SiO2(тв) = MgSiO3(тв) +CO2(г) (450 - 700°C)
Na2CO3(тв) + SiO2(тв) = Na2SiO3(тв) +CO2(г) (800 - 900°C)
MgO(тв) + SiO2(тв) = MgSiO3(тв) (980 - 1150°C)
Примените правило фаз к каждой реакции в отдельности.
31. В керамическом производстве при разных температурах протекают реакции:
MgCO3(тв) = MgO(тв) +CO2(г) (400 - 600°C)
2CaSO4(тв) = 2CaO(тв) + 2SO2(г) + O2(г) (850 - 1100°C)
CaCO3(тв) = CaO(тв) + CO2(г) (850 - 920°C)
Na2SO4(тв) +C(тв) + CaCO3(тв) = Na2CO3(тв) + CaS(тв) + 2CO2(г) (1000°C)
Fe2O3(тв) + C(тв) = 2FeO(тв) + CO(г)(1100°C)
Примените правило фаз к каждой реакции в отдельности.
32. Кремний получают разложением силанов при 400-500°С:
SiH4(тв) = Si(тв) + 2H2(г)
Si2H6(тв) = 2Si(тв) + 3H2(г)
 |
SiH4(тв) + Si2H6(тв) = 3Si(тв) + 5H2(г)
Определить фазовый состав суммарной реакции в указанном интервале температур.
33. Аммиак и хлористый водород реагируют по уравнению
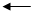
 NH3 + HCl NH4Cl
NH3 + HCl NH4Cl
Смешано 2 моль NH3 и 1 моль HCl. Cколько степеней свободы будет иметь система после наступления равновесия?
 2015-06-04
2015-06-04 1431
1431
