Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито по ТУ 23.2. 2068-89 с отверстиями диаметром 2 мм. Около 1,0 г (точная навеска) помещают в колбу вместимостью 100 мл, прибавляют 50 мл воды. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 2 ч. Извлечение фильтруют через бумажный фильтр в плоскодонную колбу вместимостью 50 мл и доводят объем раствора водой до метки 10 мл полученного извлечения с помощью пипетки переносят в мерную колбу вместимостью 25 мл и доводят объем раствора водой до метки (раствор А). 1 мл раствора А переносят в центрифужную пробирку, добавляют 2 мл 95% этанола, перемешивают и нагревают на водяной бане в течении 5 мин. Через 1 час содержимое пробирки центрифугируют в течение 10 мин в центрифуге со скоростью вращения 3000 об/мин. Осадок промывают 5 мл 50% этанола. Центрифугируют 5 мин в центрифуге со скоростью вращения 3000 об/мин. Спиртовой слой сливают в колбу объемом 100 мл. К осадку приливают 10 мл воды и помещают на кипящую водяную баню, где выдерживают до его полного растворения. Полученный раствор выливают в мерную колбу вместимостью 100 мл, доводят водой объем до метки (раствор Б). К 1 мл раствора Б прибавляют 2 мл 0,2% раствора антрона в серной кислоте концентрированной, охлаждают на водяной бане при температуре 10-15˚С в течение 5 мин, нагревают на кипящей водяной бане в течение 16 мин, затем снова охлаждают на водяной бане при температуре 10-15˚С в течение 5 мин. Для охлажденного раствора измеряют оптическую плотность на спектрофотометре при длине волны 625 нм в кювете с толщиной слоя 10 мм.
В качестве раствора сравнения используется смесь следующего состава: 1 мл воды очищенной и 2 мл 0,2% раствора антрона, выдержанная в тех же условиях, что и опытная смесь.
Количество полисахаридов в цветках липы вычисляют с помощью калибровочного графика по формуле:
Контрольная работа 3 Билет 4 с.5
Х (%) = а ∙ 50 ∙ 25 ∙ 100 ∙ 100,
1 ∙ b ∙ 10 ∙ 1000000 ∙ (100-W)
где а – количество глюкозы, найденное по калибровочному графику, мкг/мл;
b – навеска сырья в г; 50 - объем извлечения, мл; 25,100 – объемы мерных колб, мл; 1,10 – аликвоты, мл; 1000000 – пересчет микрограммов в граммы; W- потеря в массе при высушивании, %.
Для указанных видов лекарственных растений заполните таблицы и составьте схемы (п. 9-12):
1. Чистотел большой
2. Перец однолетний
3. Термопсис очередноцветковый
4. Липа сердцевидная
5. Алтей лекарственный (корни)
6. Тыква обыкновенная
9. Для указанных видов заполните таблицу:
| Вид | В РФ заготав-ливается ди-корастущее | В РФ введено в промыш-ленную куль-туру | Произрастаетв Татарстане | Охраняется в Татарстане |
10. Для видов, заготовка которых возможна в Татарстане, составьте схему заготовки сырья:
1. В каких местообитаниях встречаются?
2. В какие сроки нужно заготавливать сырье?
3. Правила сбора (отличие от возможных примесей) и условия сушки.
4. Особенности хранения сырья.
11. Для указанных видов сырья заполните таблицу:
| Сырье | Стандартизуется НД по содержанию | По содержа-нию дейст-вующих ве-ществ не стандарти-зуется | ||
| индивиду-ального вещества | суммы дейст-вующих ве-ществ | экстрактив-ных веществ | ||
В столбцах 2 и 3 укажите, соответственно, название соединения или природу действующих веществ и метод определения; в столбце 4 - природу экстрагента.
12. Для указанных видов сырья заполните таблицу:
Контрольная работа 3 Билет 4 с.6
| Сырье | Поступает в аптеки для использова-ния в форме настоев (от-варов) | Поступает на предприятия для произ-водства сум-марных не-очищенных препаратов (настоек, экс-трактов, со-ков, масел) | Поступает на предприятия для произ-водства сум-марных очи-щенных (но-вогаленовых) препаратов | Поступает на предприятия для выделе-ния и исполь-зования в ка-честве лекар-ственных средств инди-видуальных веществ |
В таблице укажите названия препаратов и основное терапевтическое назначение.
13. Используя рисунок микроскопических признаков листа термопсиса ланцетного с поверхности, нарисуйте картину его поперечного среза и отметьте на нем диагностические признаки.
Контрольная работа 3 Билет 5 с.1
Билет 5
1. Корни раувольфии змеиной, клубни с корнями стефании гладкой, побеги эфедры хвощевой содержат алкалоиды. К каким классам алкалоидов по классификации А.П.Орехова относятся алкалоиды этих видов сырья?
2. Физико-химические свойства алкалоидов. Объясните исходя из этих свойств, схему получения «Раунатина» из корней раувольфии змеиной:
1. Измельченные корни экстрагируют 10% водным раствором уксусной кислоты методом противоточной экстракции.
2. Водное извлечение подщелачивают 25% водным раствором аммиака до рН=10-11. После чего многократно экстрагируют хлористым метиленом.
3. Хлорметиленовое извлечение упаривают до 1/5 объема и обрабатывают 5% водным раствором уксусной кислоты.
4. Водное извлечение снова подщелачивают 25% раствором аммиака до рН=10-11 и снова обрабатывают хлористым метиленом.
5. Хлорметиленовую вытяжку промывают водой и обрабатывают прокаленным сульфатом натрия, после чего упаривают до 1/8 первоначального объема и добавляют семикратное количество петролейного эфира. Полученный осадок отфильтровывают и высушивают.
3. Качественное определение алкалоидов в лекарственном растительном сырье.
4. Методы количественного определения алкалоидов в растительном сырье. Приведите примеры. Объясните методику количественного определения гиндарина в клубнях с корнями стефании гладкой. Гиндарин является наиболее слабым основанием среди других алкалоидов стефании (стефаглабрина, циклеанина и др.). На каком этапе методики происходит их отделение от гиндарина?
Количественное определение. Аналитическую пробу сырья измельчают как указано в разделе «Качественные реакции». 10 г (точная навеска) измельченного сырья помешают в колбу с притертой пробкой емкостью 500 мл, смачивают 5 мл раствора аммиака, заливают 200 мл хлороформа и оставляют стоять на сутки при периодическом помешивании. Полученное извлечение фильтруют через бумажный фильтр. 100 мл фильтрата переносят в делительную воронку вместимостью 250 мл и обрабатывают 3 раза по 40 мл 10% раствором серной кислоты, взбалтывая каждый раз в течение 5 минут. Объединенные кислотные извлечения доводят раствором аммиака до pН=5, и обрабатывают 3 раза по 50 мл хлороформом, взбалтывая каждый раз в течение 5 минут. Объединенные хлороформные извлечения сушат свежепрокаленным безводным сульфатом натрия и фильтруют в колбу для отгонки емкостью 250 мл. Колбу и фильтр дважды промывают безводным хлороформом порциями по 20 мл и хлороформ полностью отгоняют. Сухой остаток растворяют в 25 мл безводного хлоро-
Контрольная работа 3 Билет 5 с.2
форма. Отсутствие других алкалоидов в хлороформном растворе контролируют хроматографически. На хроматографическую пластинку с незакрепленным слоем окиси алюминия (активированного по Брокману) наносят полученный выше хлороформный раствор. Хроматографируют в системе растворителей эфир-метанол (98:2), после высушивания проявляют парами иода. 1-тетрагидропальматин имеет Rf 0,8.
5 мл хлороформного раствора переносят в коническую колбу вместимостью 50 мл и последовательно приливают 10 мл диэтиленгликоля, 1,5 мл раствора ацетата окисной ртути в ледяной уксусной кислоте и 3 капли 0,07% спиртового раствора метилового оранжевого.
Раствор титруют из бюретки с ценой деления 0,02 мл 0,1 н раствором хлорной кислоты в смеси 1 объема безводного хлороформа и 2 объемов диэтиленгликоля до появления оранжевой окраски.
Параллельно проводят контрольный опыт. 1 мл 0,1 н раствора хлорной кислоты соответствует 0,03919 г гидрохлорида 1-тетрагидропальматина. Содержание гиндарина (1-тетрагидропальматина гидрохлорид) в процентах (Х) вычисляют по формуле:
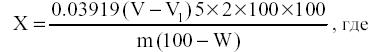 |
V – объем раствора хлорной кислоты, израсходованный на титрование пробы в миллилитрах; V1 – объем раствора хлорной кислоты, израcходованное в контрольном опыте, в миллилитрах; m – масса сырья в граммах; W – влажность сырья в процентах.
5. Напишите структуру глюкоманнана, который имеет линейное строение с β 1-4 связями при соотношении D-маннозы и D-глюкозы 3:1.
6. Дайте сравнительную характеристику предполагаемых физико-химических свойств указанного полисахарида (м.м.= 200 000 – 250 000 у.е.) и пектина сахарной свеклы, исходя из разницы в их химическом строении.
Пектин в промышленности получают из жома сахарной свеклы по
следующей схеме:
1. Экстрагируют измельченный жом 1,3% HCl при температуре 70 оС в течение 2,5 часов.
2. Отфильтровывают экстракт и охлаждают его до 30 – 40 оС.
3. К полученному экстракту добавляют 25% раствор NH4OH до рН= 6,0 –6,5 и раствор AlCl3.
4. Выпавший осадок отфильтровывают и многократно промывают сначала этиловым спиртом крепостью 94-96о, содержащим 7,2% HCl, затем чистым спиртом.
5. Отмытый осадок высушивают и измельчают.
Объясните эту схему исходя из строения и физико-химических свойств пектина.
Контрольная работа 3 Билет 5 с.3
7. В ГФ ХI для качественной идентификации полисахаридов в ЛРС используются реакции осаждения этанолом, с тушью, со щелочью, с α-нафтолом, карбазолом, реактивом Феллинга. Для каких видов ЛРС предусмотрены эти реакции, приведите их химизмы.
8. Объясните методику количественного определения полисахаридов в сухом экстракте алтейного корня (ФС 42-2248-84) и приведите химизмы реакций, имеющих место при ее проведении.
 2015-06-14
2015-06-14 1203
1203
