Около 5 г (точная навеска) препарата помещают в коническую колбу вместимостью 100 мл, прибавляют 50 мл 10 % раствора кали едкого спиртового, 0,1 г аскорбиновой кислоты и нагревают с обратным холодильником при температуре кипения смеси на водяной бане в течение 30 мин. Содержимое колбы охлаждают до комнатной температуры, количественно переносят 50 мл воды в делительную воронку и извлекают эфиром один раз 50 мл и два раза по 30 мл. Объединенные эфирные извлечения промывают водой по 30 мл до отсутствия щелочной реакции промывных вод (проба с фенолфталеином). Раствор фильтруют через бумажный фильтр, на который помещено 8 г безводного сульфата натрия в колбу для отгона. Сульфат натрия промывают три раза эфиром, порциями по 10 мл, которые сливают в ту же колбу. Эфир отгоняют в вакууме или в токе азота на водяной бане при температуре не выше 40°С. Сухой остаток тотчас же растворяют в спирте этиловом 96 % и количественно переносят в мерную колбу вместимостью 25 мл, доводят объем раствора тем же спиртом до метки и перемешивают. 20 мкл полученного раствора вводят в хроматограф с помощью инжектора с дозирующей петлей.
Хроматографирование проводят на приборе типа «Shimadzu» с УФ-детектором с длиной волны 292 нм на колонке «Nova-Pak C18» 3,9 х 150 мм (фирма "Waters") или на другой аналогичной. Элюент - этанол:вода в соотношении 90:10, скорость потока 1,5 мл/мин. Используют метод внешнего стандарта. Время записи хроматограммы 15 минут.
Параллельно хроматографируют 20 мкл раствора государственного стандартного образца (ГСО) α-токоферола ацетата, обработанного аналогично препарату. Содержание α-токоферола в мг% (X) вычисляют по формуле:
Sпp. ∙ Аст. ∙ 25 ∙ 1 ∙ 100 ∙ 1000 Sпp. ∙ Аст. ∙ 500
X = ------------------------------------------ = -------------------------
Sст. ∙ Апp. ∙50 ∙ 100 Scт. ∙ Апр.
где Sпp.- площадь пика α - токоферола в испытуемом растворе препарата;
Scт.- площадь пика α -токоферола в растворе ГСО α -токоферола ацетата;
Контрольная работа 3 Билет 2 с.4
Апр.- навеска препарата;
Аст.- навеска ГСО α –токоферола ацетата.
Содержание α -токоферола в препарате должно быть не менее 4 мг %.
Примечание. Приготовление раствора ГСО α -токоферола ацетата.
Около 0,05 г (точная навеска) ГСО α-токоферола ацетата (ФС 42-1522-88) омыляют как указано выше. Остаток, полученный после отгонки эфира растворяют в этиловом спирте 96 %, количественно переносят в мерную колбу вместимостью 50 мл, доводят объем раствора тем же спиртом до метки и перемешивают. 1 мл полученного раствора помещают в мерную колбу вместимостью 100 мл, доводят объем раствора тем же спиртом до метки и перемешивают.
Раствор годен в день приготовления.
Для указанных видов лекарственных растений заполните таблицы и составьте схемы (п. 9-12):
1. Крестовник плосколистный
2. Чемерица Лобеля
3. Мачек желтый
4. Смородина черная
5. Лен обыкновенный
6. Тыква обыкновенная
9. Для указанных видов заполните таблицу:
| Вид | В РФ заготав-ливается ди-корастущее | В РФ введено в промыш-ленную куль-туру | Произрастаетв Татарстане | Охраняется в Татарстане |
10. Для видов, заготовка которых возможна в Татарстане, составьте схему заготовки сырья:
1. В каких местообитаниях встречаются?
2. В какие сроки нужно заготавливать сырье?
3. Правила сбора (отличие от возможных примесей) и условия сушки.
4. Особенности хранения сырья.
11. Для указанных видов сырья заполните таблицу:
| Сырье | Стандартизуется НД по содержанию | По содержа-нию дейст-вующих ве-ществ не стандарти-зуется | ||
| индивиду-ального вещества | суммы дейст-вующих ве-ществ | экстрактив-ных веществ | ||
Контрольная работа 3 Билет 2 с.5
В столбцах 2 и 3 укажите, соответственно, название соединения или природу действующих веществ и метод определения; в столбце 4 - природу экстрагента.
12. Для указанных видов сырья заполните таблицу:
| Сырье | Поступает в аптеки для использова-ния в форме настоев (от-варов) | Поступает на предприятия для произ-водства сум-марных не-очищенных препаратов (настоек, экс-трактов, со-ков, масел) | Поступает на предприятия для произ-водства сум-марных очи-щенных (но-вогаленовых) препаратов | Поступает на предприятия для выделе-ния и исполь-зования в ка-честве лекар-ственных средств инди-видуальных веществ |
В таблице укажите названия препаратов и основное терапевтическое назначение.
13. Используя рисунок микроскопических признаков корня чемерицы на поперечном срезе, нарисуйте картину его продольного среза и отметьте на нем диагностические признаки.
Контрольная работа 3 Билет 3 с.1
Билет 3
1. Корни барбариса обыкновенного, листья белены, трава пассифлоры содержат алкалоиды. К каким классам алкалоидов по классификации А.П.Орехова относятся алкалоиды этих видов сырья?
2. Физико-химические свойства алкалоидов. Объясните исходя из этих свойств, схему получения очищенной суммы алкалоидов в методике количественного определения суммы алкалоидов в листьях белены.
Количественное определение. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. Около 10 г измельченного сырья помещают в колбу вместимостью 250 мл, приливают 150 мл эфира, 7 мл раствора аммиака и взбалтывают смесь в течение 1 ч. Эфирное извлечение быстро фильтруют через вату в колбу вместимостью 200 мл, прикрывая воронку часовым стеклом. К фильтрату приливают 5 мл воды, энергично взбалтывают и оставляют до просветления эфирного слоя, после чего отмеривают с помощью мерного цилиндра 90 мл эфирного извлечения в делительную воронку вместимостью 200 мл. Цилиндр дважды ополаскивают эфиром порциями по 10 мл, которые присоединяют к отмеренному эфирному извлечению. Эфирное извлечение обрабатывают 1% раствором хлористоводородной кислоты порциями по 20, 15, 10 мл (проба с реактивом Майера), каждый раз фильтруя через смоченный водой бумажный фильтр диаметром 5 см во вторую делительную воронку такой же вместимости. Фильтр промывают дважды 1% раствором хлористоводородной кислоты по 5 мл, присоединяя промывную жидкость к общему кислотному извлечению. Кислотное извлечение подщелачивают раствором аммиака до щелочной реакции по фенолфталеину и обрабатывают последовательно 20, 15, 10 мл хлороформа, взбалтывая по 3 мин. Хлороформные извлечения фильтруют в колбу для отгонки вместимостью 100 мл через бумажный фильтр, на который предварительно помещают 4—5 г свежепрокаленного безводного натрия сульфата, смоченного хлороформом. Фильтр дважды промывают хлороформом по 5 мл. Хлороформ отгоняют на водяной бане до объема 1—2 мл, остаток хлороформа в колбе удаляют продуванием воздуха до полного исчезновения запаха растворителя. Сухой остаток растворяют в 15 мл раствора хлористоводородной кислоты (0,02 моль/л) при подогревании на водяной бане, прибавляют 2 капли спиртового раствора метилового красного и 1 каплю раствора метиленового синего и избыток хлористоводородной кислоты оттитровывают раствором натра едкого (0,02 моль/л) до появления зеленой окраски.
Содержание суммы алкалоидов в пересчете на гиосциамин в абсолютно сухом сырье в процентах (X) вычисляют по формуле:
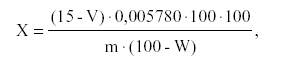 |
где 0,005780 — количество алкалоидов в пересчете на гиосциамин, соответствующее 1 мл раствора хлористоводородной кислоты (0,02 моль/л), в граммах; V — объем раствора натра едкого (0,02 моль/л), израсходованного на титрование, в миллилитрах; m — масса сырья, соответствующая отмеренному объему эфирного извлечения, в граммах; W — потеря в массе при высушивании сырья в процентах.
Контрольная работа 3 Билет 3 с.2
3. Качественное определение алкалоидов в лекарственном растительном сырье.
4. Методы количественного определения алкалоидов в растительном сырье. Приведите примеры. Объясните методику количественного определения берберина бисульфата в корнях барбариса обыкновенного. В корнях барбариса берберин может находиться в аммонийной и карбинольной формах. В данной методике он экстрагируется в карбинольной форме. Почему? Помимо берберина в корнях барбариса присутствуют и другие алкалоиды (пальматин, ятроризин, колумбанин и др.) фенольной и нефенольной природы. На каком этапе происходит отделение берберина от сопутствующих алкалоидов фенольной природы? Почему, в конечном счете, в данной методике определяется только содержание берберина?
Количественное определение. Для определения содержания берберина от средней пробы цельного сырья отделяют не менее 1кг и измельчают до частиц, проходящих сквозь сито с диаметром отверстий 7 мм, тщательно перемешивают, отбирают не менее 250 г сырья, которые измельчают до частиц, проходящих сквозь сито с диаметром отверстий 3 мм. Затем отделяют около 25 г сырья и доводят его измельчение до размера частиц, проходящих сквозь сито с диаметром отверстий 1 мм. Около 0,5 г (точная навеска) сырья помещают в коническую плоскодонную колбу емкостью 100 мл (с притертой пробкой), прибавляют 0,5% мл 25% раствора едкого натра, тщательно перемешивают стеклянной палочкой до получения однородной увлажненной массы, закрывают пробкой и оставляют при комнатной температуре на 2 часа. Затем в колбу прибавляют 50 мл эфира, закрывают пробкой и взвешивают. Содержимое колбы осторожно взбалтывают круговыми движениями в течение 10 минут и оставляют на 12 часов, затем вновь взбалтывают 10 минут, взвешивают и потерю массы восполняют эфиром. Содержимое колбы вновь осторожно перемешивают, дают отстояться, затем берут осторожно, не взмучивая, пипеткой 15 мл эфирного извлечения, помещают в делительную воронку емкостью 100 мл и обрабатывают 2% раствором серной кислоты порциями 20,10 и 10 мл (до отрицательной реакции с кремневольфрамовой кислотой). Объединенные кислотные извлечения помещают в мерную колбу вместимостью 50 мл и доводят объем раствора до метки 2% раствором серной кислоты. После тщательного перемешивания определяют оптическую плотность раствора на спектрофотометре при длине волны 420 нм в кювете с толщиной слоя 1 см.
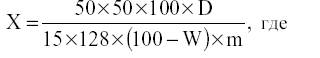 |
Содержание берберина бисульфата в процентах (X) в пересчете на абсолютно сухое сырье вычисляют по формуле:
50 – объем эфирного извлечения; в миллилитрах;50 – объем сернокислого извлечения в миллилитрах;15 – объем эфирного извлечения в миллилитрах;128 – удельный показатель поглощения Е1см 1% берберин-бисульфата при длине волны 420 нм; D – оптическая плотность сернокислотного извлечения; m – масса сырья в граммах;W – влажность сырья в процентах.
Контрольная работа 3 Билет 3 с.3
5. Приведите формулы витаминов К и С, пронумеруйте атомы углерода в их структурах и назовите лекарственные растения в которых предусмотрено их качественное или количественное определение.
6. Охарактеризуйте физико-химические свойства этих соединений. Покажите связь таких свойств этих соединений как растворимость, оптическая активность, антиоксидантная активность с особенностями их химического строения.
7. В приведенной ниже схеме комплексной переработки плодов шиповника (см. приложение) получают следующие продукты и лекарственные препараты: «Сироп из плодов шиповника», «Холосас» (сгущенный сироп шиповника), «Концентрат витаминов группы Р», «Каратолин», «Масло шиповника». Укажите по каким схемам будут получены эти препараты? Какие из этих препаратов являются лекарственными препаратами Государственного реестра лекарственных средств? Какие из этих препаратов будет содержать аскорбиновую кислоту? Какие витамины будут доминировать в других препаратах, полученных по этой схеме?
8. Какими методами проводится качественное и количественное определение витаминов К и С в лекарственном растительном сырье, приведите примеры, напишите химизмы соответствующих реакций.
Для указанных видов лекарственных растений заполните таблицы и составьте схемы (п. 9-12):
1. Барбарис обыкновенный (корни)
2. Белена черная
3. Пассифлора инкарнатная
4. Крапива двудомная
5. Подорожник блошный (трава)
6. Шиповник морщинистый
9. Для указанных видов заполните таблицу:
| Вид | В РФ заготав-ливается ди-корастущее | В РФ введено в промыш-ленную куль-туру | Произрастаетв Татарстане | Охраняется в Татарстане |
10. Для видов, заготовка которых возможна в Татарстане, составьте схему заготовки сырья:
1. В каких местообитаниях встречаются?
2. В какие сроки нужно заготавливать сырье?
Контрольная работа 3 Билет 3 с.4
3. Правила сбора (отличие от возможных примесей) и условия сушки.
4. Особенности хранения сырья.
11. Для указанных видов сырья заполните таблицу:
| Сырье | Стандартизуется НД по содержанию | По содержа-нию дейст-вующих ве-ществ не стандарти-зуется | ||
| индивиду-ального вещества | суммы дейст-вующих ве-ществ | экстрактив-ных веществ | ||
В столбцах 2 и 3 укажите, соответственно, название соединения или природу действующих веществ и метод определения; в столбце 4 - природу экстрагента.
12. Для указанных видов сырья заполните таблицу:
| Сырье | Поступает в аптеки для использова-ния в форме настоев (от-варов) | Поступает на предприятия для произ-водства сум-марных не-очищенных препаратов (настоек, экс-трактов, со-ков, масел) | Поступает на предприятия для произ-водства сум-марных очи-щенных (но-вогаленовых) препаратов | Поступает на предприятия для выделе-ния и исполь-зования в ка-честве лекар-ственных средств инди-видуальных веществ |
В таблице укажите названия препаратов и основное терапевтическое назначение.
13. Используя рисунок микроскопических признаков листа белены с поверхности, нарисуйте картину его поперечного среза и отметьте на нем диагностические признаки.
Контрольная работа 3 Билет 4 с.1
Билет 4
1. Трава чистотела, плоды перца стручкового, трава термопсиса очередноцветкового содержат алкалоиды. К каким классам алкалоидов по классификации А.П.Орехова относятся алкалоиды этих видов сырья?
2. Физико-химические свойства алкалоидов. Объясните исходя из этих свойств, схему выделения алкалоида цитизина в методике количественного определения этого алкалоида в траве термопсиса очередноцветкового.
Количественное определение. Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с диаметром отверстий 1 мм. 10 г (точная навеска) измельченного сырья помещают в плоскодонную колбу вместимостью 250 мл, приливают 100 мл хлороформа, подщелачивают 5 мл концентрированного раствора аммиака, закрывают пробкой и встряхивают на вибрационном аппарате в течение 2 часов или оставляют при комнатной температуре на 12-15 часов, после чего встряхивают 30 минут. Хлороформное извлечение фильтруют, через вату в мерный цилиндр; 50 мл фильтрата переносят в коническую колбу вместимостью 100 мл и хлороформ отгоняют до объема 1-2 мл. Остатки хлороформа удаляют продуванием воздуха. К остатку приливают пипеткой 2 мл 0,1 н. раствора едкого натра и растирают стеклянной палочкой до полного удаления комочков, затем прибавляют пипеткой 3 мл воды и перемешивают. К содержимому приливают пипеткой 10 мл 0,2 н. раствора соляной кислоты, перемешивают 5-6 минут и фильтруют через тройной бумажный складчатый фильтр диаметром 7 см. По 0,04 мл фильтрата (70-90 мкг) наносят калиброванной микропипеткой на линию старта (на 4 средние полосы) хроматографической пластинки; первую полосу оставляют контрольной; на шестую полосу наносят в качестве свидетеля 0,04 мл (80 мкг) 0,2% спиртового раствора цитизина основания. Раствор наносят полосами длиной 1-1,2 см каждая, шириной 0,5 см. Во время нанесения проб пластинку подсушивают теплым воздухом. Пластинку с нанесенной пробой высушивают на воздухе, затем помещают в предварительно насыщенную (не менее 2 часов) вертикальную камеру со смесью растворителей 95% этанол - хлороформ - аммиак (40:80:0,05) и хроматографируют восходящим способом при комнатной температуре.
Через 1,5-2 часа, когда фронт растворителей пройдет около 16 см пластинку вынимают из камеры, сушат на воздухе в течение 3 минут и просматривают в УФ-свете при длине волны 360 нм. Участки с зонами адсорбции на уровне свидетеля отмечают. Цитизин просматривается на синем фоне пластинки в виде фиолетовых пятен. Для проверки полосу со свидетелем и одну полосу с испытуемым раствором проявляют реактивом Драгендорфа.
Участки сорбента с пятнами, находящимися на уровне проявленного пятна цитизина испытуемого раствора (и пятна свидетеля) и такой же участок сорбента с контрольной полосы количественно переносят в колбы со шлифами, заливают 10 мл 35% этанола и встряхивают на вибрационном аппарате в течение 1 часа. Затем растворы переносят в центрифужные пробирки и центрифугируют 15 минут при скорости вращения 4000 об/мин или фильтруют через двойной бумажный складчатый фильтр.
Оптическую плотность полученного элюата измеряют на спектрофотометре СФ-4а или СФ-1б в кювете с толщиной слоя 10 мм при длине волны 311 нм, используя в качестве раствора сравнения элюат с контрольной полосы.
Контрольная работа 3 Билет 4 с.2
Содержание цитизина в.процентах (X) в пересчете на абсолютно сухое сырье вычисляют по формуле:
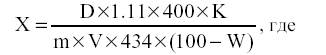 |
V – объем солянокислого раствора суммы алкалоидов, нанесенный на хроматографическую пластинку, в миллилитрах; 434 – удельный показатель поглощения цитизина (Е1% 1см) при длине волны 311 нм, полученный на приборе, использованном при разработке метода; m – масса сырья взятого на анализов в граммах; W – влажность сырья, в процентах; D – оптическая плотность элюата при длине волны 311 нм; 1,11 – поправочный коэффициент на неполное элюирование цитизина с хроматограммы; К – инструментальная поправка на используемые кюветы и спектрофотометр.
3. Качественное определение алкалоидов в лекарственном растительном сырье.
4. Методы количественного определения алкалоидов в растительном сырье. Приведите примеры. Объясните методику количественного определения пахикарпина в траве софоры толстоплодной. В траве софоры толстоплодной наряду с пахикарпином, содержатся и другие алкалоиды (матрин, софокарпин, софорамин). Почему в данной методике определяется только содержание пахикарпина?
Количественное определение. Аналитическую пробу сырья измельчают до частиц, проходящих сквозь сито с отверстиями диаметром 2 мм. 50 г (точная навеска) измельченного сырья перемешивают с 20 мл 10% раствора аммиака, заливают 300 мл дихлорэтана и встряхивают в течение 5 часов. Дихлорэтановое извлечение фильтруют через складчатый фильтр. 150 мл фильтрата помещают в делительную воронку вместимостью 500 мл, прибавляют 100 мл 20% раствора серной кислоты и встряхивают в течение 10 минут, отстаивают и отделяют серно-кислотное извлечение, фильтруя его через маленький фильтр; при этом первые 3-5 мл фильтрата отбрасывают. 40 мл серно-кислотного извлечения нейтрализуют (при охлаждении льдом), 30 мл 40% раствора едкого натра и исчерпывающе экстрагируют хлороформом, порциями 50, 25, 25 мл и т.д. (проба с кремне-вольфрамовой кислотой). Объединенное хлороформное извлечение сушат безводным сульфатом натрия в течение 30 минут при периодическом перемешивании, фильтруют и сульфат натрия промывают на фильтре 2-3 раза хлороформом по 10 мл. Хлороформ отгоняют на водяной бане, сухой остаток растворяют в 20 мл 20% серной кислоты и количественно переносят в колбу Кьельдаля вместимостью 250 мл, прибавляя туда же воду, которой промывали колбу с осадком. В колбу Кьельдаля прибавляют 30 мл 40% раствора едкого натра и отгоняют с водяным паром в приемник, содержащий 15 мл 0,1 н раствора серной кислоты. Собирают 400 мл отгона, после чего меняют приемник. Отгон титруют 0,1 н. раствором едкого натра до четкого розового окрашивания (по фенолфталеину). Отгонку продолжают, собирая в отдельные приемники каждый раз по 400 мл отгона до тех пор, пока на титрование отгона будет расходоваться столько же мл 0,1 н. раствора едкого натра, сколько на контрольный опыт. Для контрольного опыта в колбу Кьельдаля помещают 40 мл 20% раствора серной кислоты, 30 мл 40% раствора едкого натра и производят отгонку с паром, собирая в приемник с 15 мл 0,1 н.
Контрольная работа 3 Билет 4 с.3
раствора серной кислоты 400 мл отгона. Отгон титруют 0.1 н. раствором едкого натра до четкого розового окрашивания (по фенолфталеину). Из объема (в мл) 0,1 н. раствора едкого натра, пошедшего на титрование контрольного опыта, вычитают объем (в мл) 0,1 н. раствора едкого натра, пошедшего на титрование каждого объема пахикарпина, и суммируют объем мл 0,1 н. раствора серной кислоты, прореагировавшей с пахикарпином. 1 мл 0,1 н. раствора серной кислоты соответствует 0,0234 г пахикарпина.
Содержание пахикарпина в процентах (X) рассчитывают по формуле:
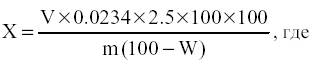 |
V – суммарный объем раствора 0,1 н. серной кислоты, прореагировавший с пахикарпином, в миллилитрах; m – масса сырья в граммах, соответствующая объему дихлорэтана, взятого на анализ; W – влажность в процентах.
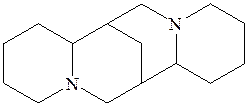

пахикарпин матрин
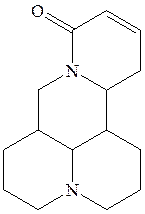
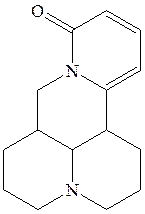
софокарпин софорамин
Контрольная работа 3 Билет 4 с.4
5. Напишите структуру арабиноксилана, которая содержит главную цепь из остатков D-ксилопиранозы, связанных 1-4 связями, причем в среднем к каждому второму моносахариду этой цепи в положении 3 присоединены остатки L-арабинофуранозы.
6. Опишите предполагаемые физико-химические свойства (агрегатное состояние, окраска, растворимость, оптическая активность устойчивость к кислотам и щелочам и др.) указанного полисахарида (м.м = 200 000 -250 000 у.е.) и предложите схему его выделения и очистки (от низкомолекулярных и высокомолекулярных примесей, других полисахаридов) из растительного материала.
7. В каких видах ЛРС по ГФ ХI предусмотрено качественное обнаружение полисахаридов? Приведите химизмы соответствующих реакций.
8. Приведенную в приложении методику количественного определения полисахаридов в цветках липы, предлагается включить в новый вариант фармакопейной статьи на это сырье. Объясните эту методику, исходя из физико-химических свойств определяемых соединений и приведите химизмы соответствующих реакций.
 2015-06-14
2015-06-14 2849
2849
