Процессы поглощения газов или растворенных веществ твердыми материалами или жидкостями носят общее название сорбции. Если сорбция идет только на поверхности, то её называют адсорбцией. Она приводит к увеличению концентрации вещества на границе раздела фаз. Если поглощаемое вещество диффундирует вглубь поглотителя, то явление называется абсорбцией. То вещество, на поверхности которого идет адсорбция, называется адсорбентом, а которое адсорбируется - адсорбатом (адсорбтивом). Адсорбцию Г обычно выражают соотношением количества адсорбата X, приходящегося на единицу площади адсорбента S (кмоль/м2)
Г = X / S
Если адсорбентом является твердое пористое тело, общую поверхность которого определить невозможно, то величину адсорбции Г относят к единице массы адсорбента m (кмоль/кг)
Г = X / m
Между адсорбентом и адсорбатом возникают адсорбционные силы. В зависимости от их природы рассматривают два крайних случая: физическую и химическую адсорбцию.
Физическая адсорбция возникает за счет Ван-дер-Ваальсовых взаимодействий. Она характеризуется
1) Обратимостью, т.е. может протекать обратный процесс - десорбция. Скорость адсорбции с течением времени уменьшается, а скорость десорбции увеличивается, что приводит к адсорбционному равновесию
адсорбция ↔ десорбция,
при котором скорости двух противоположных процессов становятся одинаковыми.
2) При повышении температуры величина адсорбции уменьшается, так как увеличивается скорость десорбции.
3) Малой специфичностью.
4) При физической адсорбции могут иметь место как нелокализованная адсорбция, когда молекулы адсорбата способны передвигаться по поверхности адсорбента, так и локализованная адсорбция.
С физической адсорбцией связаны стабилизация дисперсных систем, стирка, ощущение вкуса, запаха и др.
Химическая адсорбция (хемосорбция) является химическим процессом, поэтому
1) Необратима.
2) С повышением температуры увеличивается.
3) Специфична. Адсорбция происходит, если возможна химическая реакция.
4) Молекулы адсорбата связаны с адсорбентом прочными химическими силами и не могут перемещаться по поверхности последнего, поэтому химическая адсорбция - локализованная.
Примером является адсорбция кислорода на алюминии, приводящая к образованию поверхностной оксидной пленки.
Уравнение адсорбции устанавливает функциональную связь величины адсорбции с равновесной концентрацией и температурой Г = f (С, Т), если адсорбция идет из растворов, и равновесным давлением и температурой Г = f (Р, Т), если адсорбируется газ.
При постоянной температуре адсорбированное количество вещества есть функция равновесной концентрации Г = f (С)т или равновесного давления Г = f (Р)т.
Графическая зависимость называется изотермой адсорбции и имеет вид кривой, на которой можно выделить три участка: I и III - прямолинейные, II - криволинейный.
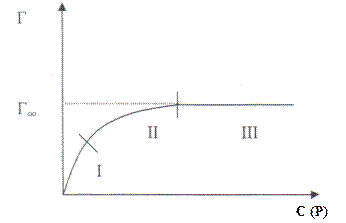
Рис. 2 Изотерма мономолекулярной адсорбции
 2015-06-14
2015-06-14 1190
1190
