Большое значение в практической деятельности судомеханика имеет представление о гетерогенном равновесии в растворах электролитов, которое лежит в основе механизма накипеобразования при эксплуатации энергетических установок.
Подавляющее большинство электролитов обладает ограниченной растворимостью в воде. На практике часто встречаются гетерогенные системы, в которых осадок малорастворимого электролита находится в равновесии с насыщенным раствором этого электролита:
растворение


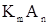 mK
mK 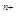 + nA
+ nA 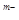


осадок кристаллизация раствор 
CaCl2 + H2SO4 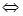 CaSO4↓ + 2HCl
CaSO4↓ + 2HCl
Ca2+ + SO42- 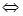 CaSO4↓
CaSO4↓
раствор осадок
Произведение активностей ионов в насыщенном растворе малорастворимого электролита при заданной температуре есть величина постоянная и называется произведением растворимости ПР:
K = ПРK 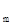 A
A 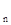 = а
= а 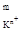 а
а 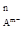
Произведение растворимости как и константа равновесия зависит от природы электролита и от температуры, но не зависит от активности ионов в растворе.
Поскольку раствор малорастворимого соединения получается очень разбавленным, и взаимодействие ионов из-за их удаленности друг от друга практически отсутствует, коэффициент активности близок к единице, то активности ионов в растворе можно приравнять к их концентрациям, и произведение растворимости может быть записано в следующей форме:
ПРK 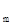 A
A 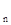 =[K
=[K 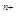 ]
] 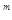 ·[A
·[A 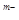 ]
] 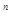
Произведение растворимости характеризует растворимость вещества: чем больше ПР, тем больше растворимость.
Часто вместо значений ПР применяют показатель растворимости рПР - отрицательный логарифм произведения растворимости, рПР= - lgПР.
Если произведение концентраций ионов электролита в растворе равно ПР, то раствор находится в равновесии с твердой фазой (осадком).
Когда [K 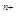 ]
] 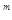 ·[A
·[A 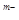 ]
] 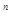 >ПР, равновесия нет при этих концентрациях, и из раствора будет выделятся твердая фаза (осадок).
>ПР, равновесия нет при этих концентрациях, и из раствора будет выделятся твердая фаза (осадок).
Если же [K 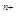 ]
] 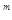 ·[A
·[A 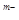 ]
] 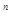 <ПР, то снова нет равновесия, но раствор в этом случае ненасыщен относительно твердой фазы, и она будет переходить в раствор.
<ПР, то снова нет равновесия, но раствор в этом случае ненасыщен относительно твердой фазы, и она будет переходить в раствор.
Под действием одноименного иона равновесие смещается по принципу Ле-Шателье в сторону образования осадка. Например:
CaSO4<=>Ca 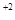 + SO4
+ SO4 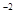
осадок раствор
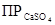 =
= 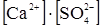
при введении дополнительного иона Ca 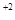 в раствор, равновесие будет смещаться влево.
в раствор, равновесие будет смещаться влево.
Этим объясняется повышенное накипеобразование при наличии, например, в котловой воде даже следов одноименных ионов, содержащихся в качестве примесей при различного рода нарушениях воднохимических режимов.
 2015-06-14
2015-06-14 950
950








