К сильным электролитам условно относят вещества, кажущаяся степень диссоциации которых в растворе превышает 30% ( > 0,3). При < 3% ( < 0,03) электролиты считают слабыми, в других случаях о них говорят как об электролитах средней силы.
Силу электролитов количественно характеризуют степенью диссоциации. Степень диссоциации () - это отношение числа распавшихся на ионы молекул (Nдис.) к общему числу молекул растворенного вещества (Nобщ.):
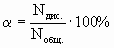
Степень диссоциации выражают в долях единицы или в процентах. Поскольку общее число молекул вещества в растворе пропорционально количеству его вещества и его молярной концентрации, то можно записать:
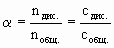 ,
,
где nдис. и cдис. - соответственно, количество и молярная концентрация растворенного вещества, подвергшегося электролитической диссоциации;
nобщ. и cобщ. - количество и молярная концентрация вещества в растворе в момент его приготовления.
Электролиты, у которых = 1, относят к сильным, у слабых электролитов < 1.
Степень диссоциации обычно определяют по данным измерения электропроводности растворов, которая прямо пропорциональна концентрации свободно движущихся ионов. При этом получают не истинные , а кажущиеся значения. Они всегда меньше истинных значений , т.к. ионы при движении к электродам сталкиваются и частично уменьшают свою подвижность, особенно при высокой их концентрации в растворе, когда возникает электростатическое притяжение между ионами. Например, истинное значение степени электролитической диссоциации HCl в разбавленном растворе равно 1, в 1 М растворе = 0,78 (78%) при 18 С, однако, в этом растворе не содержится 22% недиссоциированных молекул HCl, практически все молекулы диссоциированы.
Электролиты, которые в разбавленном водном растворе диссоциируют практически полностью, называют сильными электролитами.
К сильным электролитам в водных растворах принадлежат почти все соли, многие неорганические кислоты (H2SO4, HNO3, HClO4, галогеноводородные, кроме HF и др.), гидроксиды s-элементов (исключение - Be(OH)2 и Mg(OH)2). Кажущиеся значения a этих электролитов находятся в пределах от 70 до 100%. Диссоциация сильных электролитов - это практически необратимый процесс:
HCl H+ + Cl- или HCl = H+ + Cl-
Электролиты, которые в разбавленном водном растворе диссоциируют частично, называют слабыми. Диссоциация слабых электролитов - обратимый процесс, например:
| (при 25 С) | |
| HCN H+ + CN- | 7·10-5 (или 0,007)) |
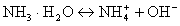 | 0,013 (или 1,3%) |
Степень электролитической диссоциации зависит от:
- природы электролита и растворителя;
- концентрации раствора;
- температуры
и возрастает при увеличении разбавления раствора:
| C(CH3COOH), моль/л | 0,2 | 0,1 | 0,05 | 0,01 | 0,005 | 0,001 |
| , % (при 25° С) | 0,05 | 1,4 | 1,9 | 4,2 | 6,0 | 12,4 |
| слабый электролит | электролит средней силы |
Степень диссоциации возрастает при увеличении температуры раствора. Увеличение кинетической энергии растворенных частиц способствует распаду молекул на ионы, что приводит к возрастанию степени диссоциации при нагревании растворов.
Если в растворе слабой кислоты или слабого основания увеличить концентрацию одноименного иона введением соответствующей соли, то наблюдается резкое изменение степени диссоциации слабого электролита. Рассмотрим, например, как изменится уксусной кислоты (CH3COOH) при введении в раствор ацетата натрия (введение одноименных ионов CH3COO-).
 2015-06-14
2015-06-14 960
960








