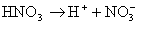
Двухосновная H2SO4 диссоциирует ступенчато, причем первый ион H+ отрывается от молекулы легче, чем второй. Вторая ступень диссоциации является обратимым процессом и характеризуется значением константы диссоциации:
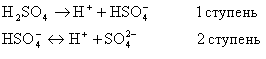
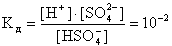
К кислотам - слабым электролитам относят HF, H2CO3, HCN, H2S, CH3COOH и др. В водном растворе они частично распадаются на ионы. Например,
HF H+ + F-
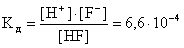
Слабые многоосновные кислоты диссоциируют ступенчато. Каждую ступень характеризуют своим значением константы диссоциации, например:
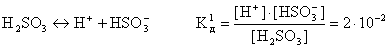
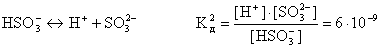
Первый ион водорода H+ отрывается от молекулы легче, чем последующие от положительно заряженных анионов, поэтому
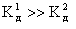 .
.
В связи со ступенчатой диссоциацией многоосновные кислоты способны образовывать кислые соли, NaHSO4, NaHCO3, K2HPO4 и т.д.
С точки зрения теории электролитической диссоциации основания - это вещества, диссоциирующие в водном растворе с образованием гидроксид-ионов OH- и катионов металла.
В общем виде уравнение электролитической диссоциации основания имеет вид:
основание гидроксид-ион + катион металла
Сильные основания (щелочи) в водном растворе практически полностью распадаются на ионы, например:
KOH OH- + K+
Ba(OH)2 OH- + BaOH+
BaOH+ OH- + Ba2+
Слабые многокислотные основания диссоциируют ступенчато:
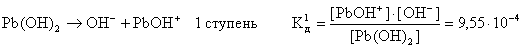
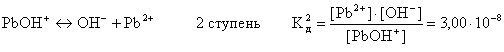
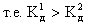
Этим объясняют способность многокислотных оснований образовывать основные соли: CuOHCl, (ZnOH)2SO4 и др.
С точки зрения теории электролитической диссоциации амфотерные гидроксиды (амфолиты) - это вещества, диссоциирующие в водном растворе как по типу кислот, так и по типу оснований. К ним относят Be(OH)2, Zn(OH)2, Pb(OH)2, Sn(OH)2, Al(OH)3, Cr(OH)3, и др. Например, уравнения электролитической диссоциации Be(OH)2:
1) диссоциация по типу основания:
Be(OH)2 + 3H2O OH- + [BeOH(H2O)3]
[BeOH(H2O)3] + H2O OH- + [Be(H2O)4]
2) диссоциация по типу кислоты:
Be(OH)2 + 2H2O H+ + [Be(OH)3H2O]
[Be(OH)2H2O] H+ + [Be(OH)3]
Рассмотрим некоторые общие закономерности в изменении свойств гидроксидов. Диссоциация кислородсодержащих гидроксидов зависит от сравнительной прочности и полярности связей Э-О и О-Н. Чем менее прочна или более полярна связь, тем легче происходит электролитическая ионизация по этой связи в водных растворах. Таким образом, диссоциация гидроксидов может протекать по двум направлениям:
Э ------ О ------ Н
1) ЭОН ОН- + Э+ (по типу основания)
2) ЭОН Н+ + ЭО- (по типу кислоты)
Чем больше степень окисления и меньше радиус центрального иона (Э), тем менее полярна связь Э-О и выше ее прочность сравнительно со связью О-Н. В данном случае диссоциация идет по типу кислоты, т.е. с отщеплением иона водорода. И наоборот, чем меньше степень окисления и больше радиус центрального иона, тем более полярна связь Э-О и меньше ее прочность, чем связи О-Н. В этом случае диссоциация идет, преимущественно, по типу основания, т.е. с отщеплением гидроксид-ионов. Если полярности связей Э-О и О-Н близки, то диссоциация гидроксида ЭОН может протекать как по типу основания, так и по типу кислоты, т.е. гидроксид является амфотерным.
В периодах с увеличением заряда ядер элементов радиусы ионов уменьшаются, а максимальная степень окисления в соединениях типа ЭОm(ОН)n возрастает от 1 до 7. В связи с этим уменьшается полярность и увеличивается прочность связи Э-О, т.е. основные свойства
 2015-06-14
2015-06-14 1765
1765








