1. Вычислить стандартную энтальпию растворения NaOH в воде, если при растворении 10 г NaOH в 250 мл воды температура раствора повысилась от 200С до 29,70С. Удельная теплоемкость раствора равна 3,99 Дж/(г·К).
Дано: 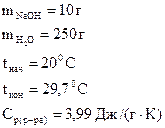 |
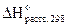 (NaOH) -? (NaOH) -? |
РЕШЕНИЕ:
Стандартную энтальпию растворения рассчитываем по уравнению:
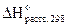 (NaOH) =
(NaOH) =
= 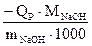 , (кДж/моль)
, (кДж/моль)
где МNaOH - молярная масса NaOH, г/моль,
Qp = mр-ра·Ср(р-ра)·(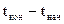 ), -количество выделившейся теплоты при растворении NaOH, Дж
), -количество выделившейся теплоты при растворении NaOH, Дж
mр-ра - масса раствора, г;
Ср(р-ра) – теплоемкость раствора, кДж/(г×К)
1000 - пересчет Дж в кДж.
Для рассматриваемой задачи 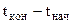 = 29,7-20 = + 9,70. При этом знак "+" указывает на повышение температуры при растворении, а знак "-" - на понижение температуры.
= 29,7-20 = + 9,70. При этом знак "+" указывает на повышение температуры при растворении, а знак "-" - на понижение температуры.
mр-ра = m 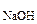 + m
+ m 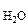 = 10+250 = 260 г.
= 10+250 = 260 г.
Тогда: QР = (10 + 250)·3,99·9,7 = 10062,8 Дж,
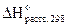 (NaOH) =
(NaOH) = 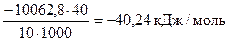 ,
,
Ответ: 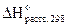 (NaOH) = - 40,24 кДж/моль.
(NaOH) = - 40,24 кДж/моль.
2. Найти массу метана, при полном сгорании, которого выделяется теплота, достаточная для нагревания 30 л воды от 20 до 90оС. Мольная теплоемкость воды равна 75,3 Дж/мольК. КПД теплового агрегата составляет 40%.
Дано: 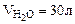 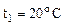 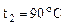 Ср = 75,3 Дж/мольК КПД = 40% Ср = 75,3 Дж/мольК КПД = 40% |
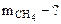 |
РЕШЕНИЕ:
Определяем количество теплоты, необходимое для нагревания 30 л воды от 20 до 90оС.
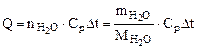
т.к. 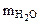 =
= 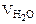
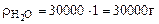
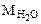 = 18 г/моль ∆t = 90 – 30 = 60К
= 18 г/моль ∆t = 90 – 30 = 60К

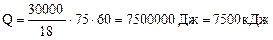
Учитывая КПД теплового агрегата потребуется
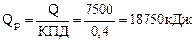 теплоты
теплоты
Такую теплоту необходимо получить при сжигании метана. Тепловой эффект реакции горения метана получим используя I следствие из закона Гесса
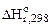 = Σni
= Σni 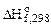 (В) - Σ nj
(В) - Σ nj 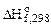
продуктов исходных
реакции веществ
Уравнение горения метана
СН4(г) + О2(г) = СО2(г) + 2Н2О(г)
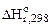 -74,9 0 -393,5 2(-241,84)
-74,9 0 -393,5 2(-241,84)
кДж/моль
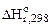 = (-393,5) + 2(-241,84) –(-74,9) = - 802,28 кДж
= (-393,5) + 2(-241,84) –(-74,9) = - 802,28 кДж
Так как при сгорании одного моль метана выделяется 802,28кДж, то определяем количество моль метана, которое необходимо для получения 18750 кДж теплоты.
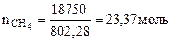
Определяем массу метана
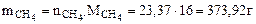
Ответ: 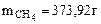
3. Испльзуя следующие термохимические уравнения:
2CO(г) + О2(г) = 2CO2(г) 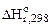 = - 566 кДж (4.10)
= - 566 кДж (4.10)
2Fe(к) + O2(г) = 2FeO(к) 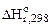 = - 529,6 кДж (4.11)
= - 529,6 кДж (4.11)
4FeO(к) + О2(г) = 2Fe2O3(к) 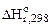 =- 585,2 кДж (4.12)
=- 585,2 кДж (4.12)
 2015-06-05
2015-06-05 1896
1896








