По химической природе ферменты делятся на:
- Однокомпонентные
- Двухкомпонентные
Белковая часть называется апоферментом, небелковая – простетической группой.
Простетическая группа, легко отделяющаяся от белковой части, называется коферментом или кофактором.
Примеры
1. Ферменты, состоящие из остатков аминокислот:
Трипсин, липаза
2. Двухкомпонентные ферменты:
2.1 Роль кофактора выполняют ионы неорганической природы: Zn+2, Mg+2, Mn+2, Fe+2, Cu+2, K+, Na+;
2.2 Вещества сложной органической природы-производные витаминов (коферменты):
Примеры коферментов
| Кофактор | Функция | Витамин |
| NAD+, NADF+ | Перенос водорода (протонов и электронов) | Никотиновая кислота – витамин PP |
| FAD | Перенос водорода (протонов и электронов) | Рибофлавин – витамин B2 |
| Коэнзим А | Активация и перенос ацильных групп | Пантотеновая кислота – витамин B3 |
| Пиридоксальфосфат | Перенос аминогрупп | Пиридоксин – витамин B6 |
| Тиаминпирофосфат | Декарбоксилирование кетокислот | Тиамин – витамин B1 |
МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ
Реакция А ↔ В протекает через переходное состояние с более высокой энергией, чем энергия А. Переходное состояние имеет более высокое значение свободной энергии, чем у А на величину ∆ G+ - cвободную энергию активации Гиббса.
∆ G+ = G перех. состояние – G субстрата
Фермент повышает скорость реакции путем снижения активационного барьера ∆ G+. При взаимодействии фермента с субстратом реакция протекает по иному механизму, характеризующемуся более низкой энергией переходного состояния, чем реакции в отсутствии фермента.
АВ ®А+В
К
АВ ®АК+В Обходной путь, требует АК ®А+ К меньше энергии активации в переходном состоянии
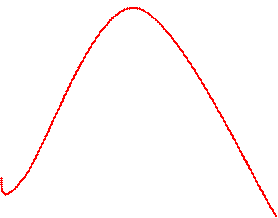
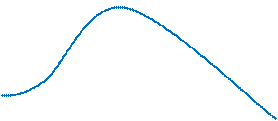
В графическом изображении энергия активации есть высота энергетического барьера, которая должна быть преодолена для осуществления химической реакции превращения субстрата - С в продукты реакции - П
В случае неферментативной реакции молекула субстрата должна для активирования перейти на более высокий уровень – переходное состояние - С*, в котором субстрат претерпевает изменение, образуя продукт - П. Энергия активации Еa1 определяется как разность уровней молекул С и С*.
В ферментативной реакции энергия активации Еa2 фермент-субстратного комплекса: ФС ٭ меньше. Это позволит фермент-субстратному комплексу превращаться в продукт реакции – П при умеренных температурах – 37оC.
 . Еа
. Еа
 С ٭
С ٭
 Еa1
Еa1
 Неферментативная
Неферментативная
реакция
 Еa2 ФС ٭
Еa2 ФС ٭
 Ферментативная
Ферментативная
реакция
С
 П
П
 2015-06-26
2015-06-26 334
334








