Так як кожна поправка p, d, f … має два близьких значення, то відповідно, енергія в цих станах буде відповідати виразам:
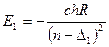
 і
і 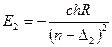 (3.5)
(3.5)
Але у Е1 і Е2 головне квантове число n і азімутальні квантові числа nj=k однакові, це означає, що різниця в енергії може бути викликана тільки різницею в якомусь третьому квантовому числі. Що це за число?
Пояснення було дано Гаудсмітом і Уленбеком (амер. вчені) у 1925 р., які висунули гіпотезу про обертання електрона навколо власної вісі. Тоді він повинен мати власний механічний момент, кількість руху Ps, але так як це заряджена частинка,то і деякий магнітний момент ms - “спін” (обертання). За квантовою теорією
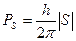 , а ms=mБ ® ms=ms·mБ. (3.6)
, а ms=mБ ® ms=ms·mБ. (3.6)
Магнітне поле орбітального руху електрона Норб створює переважний напрямок, по відношенню до якого вектор момента кількості руху спіна електрона може розташовуватися під (2|S|+1) дискретними кутами.
Маємо аналог магнітного диполя в неоднорідному магнітноиу полі (електрон з магнітним дипольним моментом в магнітному полі орбітального руху). Тоді електрон повинен мати магнітну енергію msНсosQ. Різні значення цієї енергії викликає розщеплення ліній на (2|S|+1) рівнів. Експериментально визначено, якщо розщеплення =2, тоді величині спінового квантового числа треба приписати значення ½, тобто прийняти, що
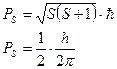 (3.7)
(3.7)
і припустити можливість лише двоякої орієнтації спіна відносно нормалі до площини орбіти: паралельна і антипаралельна.
Але S-рівні не розщеплюються, тому Уленбек і Гаудсміт припустили, що механічний і магнітний моменти орбітального руху пропорційні не азімутальному числу k, а числу l на одиницю менше k: l=0,1,2…- орбітальне квантове число. Тоді у S-рівня k=1, відповідно l=0 і pl і ml нема, додаткової магнітної енергії нема, розщеплення нема.
Як наслідок, гіпотеза Гаудсміта і Улембека, що пояснює дублети в спектрах лужних металів складається з трьох гіпотез:
1. Припущення про наявность у електрона власних механічного і магнітного моментів pS, mS (спін електрона).
2. Припущення, що величина механічного момента 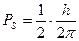 , тобто половина елементарного момента руху.
, тобто половина елементарного момента руху.
3. Припущення про заміну азимутального квантового числа k, як міри механічного і магнітного моментів орбіт руху електрона, на орбітальне квантове число l= k-1.
Тоді магнітне квантове число m, що характеризує проекцію орбітального механічного момента на переважний напрямок дії зовнішньої сили може приймати значення від l до –l, тобто 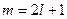 .
.
Таким чином, враховуючи спін електрона, стан атомів лужних металів необхілно хатактеризувати 3-ма квантовими числами: n, l, s(±1/2) (при відсутності зовнішньої дії).
 2015-06-28
2015-06-28 1060
1060
