Однією з найважливіших характеристик атомного ядра є зарядове число Z, яке дорівнює числу протонів, що входять до складу атомного ядра, і визначає його заряд + Zе. Число Z визначає порядковий номер хімічного елемента в таблиці Менделєєва, тому його називають атомним номером ядра.
Число нуклонів у ядрі (сума нейтронів і протонів) позначається буквою А і називається масовим числом ядра. Тоді число нейтронів в ядрі буде
N=A-Z (5.2)
Для позначення ядер застосовується символ 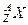 , де Х – хімічний символ якого-небудь елемента. Ядра з однаковим зарядовим числом Z, але з різними масовими числами А – називаються ізотопами. Більшість хімічних елементів мають по декілька стабільних ізотопів: у кисня три (
, де Х – хімічний символ якого-небудь елемента. Ядра з однаковим зарядовим числом Z, але з різними масовими числами А – називаються ізотопами. Більшість хімічних елементів мають по декілька стабільних ізотопів: у кисня три (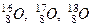 ), у олова десять, у водня є три ізотопа (
), у олова десять, у водня є три ізотопа (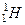 - водень,
- водень, 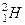 - важкий водень або дейтерій,
- важкий водень або дейтерій, 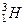 - тритій, який радіоактивний (тобто нестабільний).
- тритій, який радіоактивний (тобто нестабільний).
Розмір ядра, яке можна рахувати у першому наближенні шаром з радіусом r, визначається масовим числом:
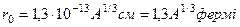 .
.
Якщо об’єм ядра пропорційний числу нуклонів у ньому. То густина речовини в усіх ядрах приблизно однакова.
Спіни нуклонів складаються в результуючий спін ядра. Так як спін нуклона ½, то квантове число спіна ядра буде напівцілим при непарному числі нуклонів А, і цілим або нульовим при парному А. Спіни ядер І не перевищують зазвичай декількох одиниць, тобто спіни більшої частини нуклонів у ядрі компенсуються, розташовуючись антипаралельно.
Механічний момент Мі ядра складається з моментів електронної оболонки Мj а повний момент імпульса атома позначається МF і визначається квантовим числом F.
Взаємодією магнітних моментів електронів у ядрі пояснюється наявність тонкої та надтонкої структури атомних спектрів.
 2015-06-28
2015-06-28 434
434








