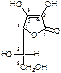
Главные природные источники: плоды шиповника, салат, капуста, картофель, томаты, черная смородина, цитрусовые, крапива, хвоя.
Описание: белый кристаллический порошок без запаха, кислого вкуса.
Растворимость: ЛР в воде, спирте. ПНР в эфире, хлороформе.
Подлинность:
ГФ:
1. С AgNO3 2%
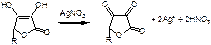
НеГФ:
3. С KMnO4/H+ à MnSO4 обесцвечивание
4. Обесцвечивание раствора I2
5. Обесцвечивание метиленового синего.
6. Получение берлинской лазури:
Аск. кислота + 2K3[Fe(CN)6] + 6HCl à Окисленная кислота + 2H4[Fe(CN)6] + 6KCl
3H4[Fe(CN)6] + 4FeCl3 à ↓Fe4[Fe(CN)6]3 + 12HCl
7. С реактивом феллинга.
CuOH à Cu2O кирпично-красный.
9. Реакция солеобразования с Fe2+
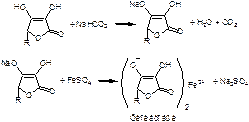
Использовать NaOH нельзя, т.к. Fe(OH)2↓ выпадет в красный осадок.
1. Йодатометрия. Титрант KIO3 0,1М. К раствору добавляют KI, HCl. Индикатор – крахмал.
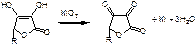
ТЭ: KIO3 + KI + HCl à I2
f=1/2
НеГФ:
2. Йодометрия с крахмалом или без него.
I2 à 2HI
4. Алкалиметрия. Индикатор ФФ. Титран – NaOH.
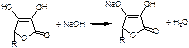
f=1
5. ФЭК с 2,6-дихлорфенолиндофенолятом.
glucosum-Д-(+)-глюкопираноза
Описание: Б.цв. кристаллы или белый мелко кристаллический порошок без запаха. Легко растворим в воде, мало растворим в спирте, практ. нераств. в эфире. Лек. формы: р-ры для инъекций и инфузий, таб.
Требования НД к качеству глюкозы как лекарственному средcтву
Подлинность: с реактивом Феллинга.
R-CHO + 2[Ag(NH3)2]NO3 + H2O 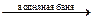 Ag¯ + RCOONH4 + NH3 + NH4NO3
Ag¯ + RCOONH4 + NH3 + NH4NO3
б) с реактивом Фелинга
Реактив – смесь равных объемов раствора Фелинга 1 (CuSO4 + следов. H2SO4 – прозрачная жидкость голубоватого цвета) и раствора Фелинга 2 (сеньетова соль – тартрат калия натрия в растворе щелочи).
При добавлении альдегида и кипячении на водяной бане, выпадает осадок красно-бурого цвета.
в) с реактивом Несслера.
RCHO + K2[HgI4] + 3KOH à Hg¯ + RCOOK + 4KI + 2H2O
2) С резорцином (+HCl / H2SO4) à(t) розовое, красное окрашивание.
КО: не проводится. Для инъекций – рефрактометрия., поляриметрия.C=(n-n0)/F*100
Обратная йодометрия в щелочной среде.
Аликвота + избыток титрованного раствора I2 + щелочь. I2 в щелочной среде диспропорционирует с образованием NaIO, который окисляет HCHO до HCOONa.
I2 + 2NaOH à NaIO + NaI + H2O
побочно: 3NaIO à NaIO3 + 2NaI
Ставим в темное место, подкисляя H2SO4
HCHO + NaIO + NaOH à HCOONa + NaI + H2O
NaI + NaIO + H2SO4 à I2 + Na2SO4 + H2O
Титруем 0,1М Na2S2O3
I2 + Na2S2O3 à 2NaI + Na2S4O6
f(HCHO) = ½
*******
Таблетки – твердая дозированная ЛФ, получаемая прессованием лекарственных веществ, смеси лекарственных и вспомогательных веществ или формованием специальных масс и предназначенная для внутреннего, наружного, сублингвального или парентерального применения.
 2015-06-28
2015-06-28 1142
1142








