Осмолиты образуют сравнительно небольшую группу химически разнообразных низко молекулярных органических соединений. Они хорошо растворимы в воде, нетоксичны и в отличие от неорганических ионов не вызывают изменений в метаболизме, отчего и получили свое второе название совместимых веществ (compatible solutes). Синтез и накопление осмолитов органической природы в цитоплазме клеток — широко распространенное явление в растительном мире, однако в распределении разных осмолитов по видам растений наблюдаются значительные вариации. У совместимых веществ существует тенденция быть нейтральными при физиологических значениях рН. В цитоплазме они находятся в недиссоциированной форме либо в форме цвиттерионов, т. е. молекул, несущих положительный и отрицательный заряды, которые пространственно разделены. Некоторые осмолиты являются амфифильными соединениями. Молекулы амфифильных веществ несут как неполярные (гидрофобные), так и полярные (гидрофильные) группы. К осмолитам относятся также некоторые полигидроксильные соединения. Химическая структура наиболее широко распространенных осмолитов показана на рис. 8.2.
Общая функция осмолитов — участие в процессе осморегуляции. Многие неорганические ионы, такие, например, как Na+ и Сl 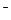 , в высоких концентрациях токсичны, поэтому не могут быть использованы растительной клеткой в регуляции осмотического давления цитоплазмы. В то же время совместимые с биополимерами осмолиты могут аккумулироваться в цитоплазме до концентраций в несколько сот микромоль на грамм без видимых токсических эффектов. Вследствие этого именно осмолиты, а не неорганические ионы клетка использует для регуляции осмотического давления цитоплазмы. Роль осмолитов особенно важна в условиях засухи и засоления, когда необходимо сконцентрировать в клетках осмотически активные вещества. Различия растений по устойчивости к дегидратации связаны со степенью эффективности у них систем биосинтеза осмолитов. Ксерофиты и галофиты — растения, обитающие соответственно при низком содержании влаги в среде и на засоленных почвах, синтезируют осмолиты с более высокой скоростью и аккумулируют их в клетках до более высоких концентраций по сравнению с растениями, обитающими в условиях нелимитированного водоснабжения и при отсутствии почвенного засоления.
, в высоких концентрациях токсичны, поэтому не могут быть использованы растительной клеткой в регуляции осмотического давления цитоплазмы. В то же время совместимые с биополимерами осмолиты могут аккумулироваться в цитоплазме до концентраций в несколько сот микромоль на грамм без видимых токсических эффектов. Вследствие этого именно осмолиты, а не неорганические ионы клетка использует для регуляции осмотического давления цитоплазмы. Роль осмолитов особенно важна в условиях засухи и засоления, когда необходимо сконцентрировать в клетках осмотически активные вещества. Различия растений по устойчивости к дегидратации связаны со степенью эффективности у них систем биосинтеза осмолитов. Ксерофиты и галофиты — растения, обитающие соответственно при низком содержании влаги в среде и на засоленных почвах, синтезируют осмолиты с более высокой скоростью и аккумулируют их в клетках до более высоких концентраций по сравнению с растениями, обитающими в условиях нелимитированного водоснабжения и при отсутствии почвенного засоления.
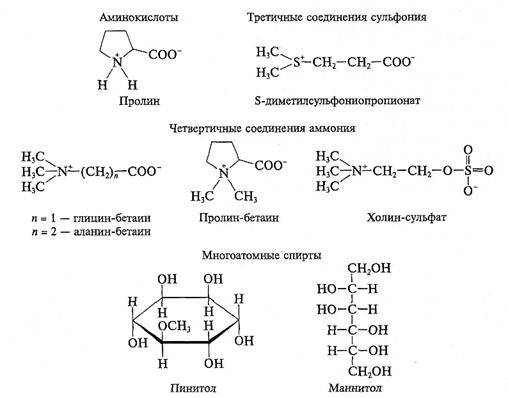
Рис. 8.2. Химические структуры некоторых наиболее распространенных осмолитов
В вакуолях, которые занимают приблизительно 90 % объема созревших клеток, осморегуляция осуществляется в основном путем аккумуляции неорганических ионов — К+, Na+ и Сl 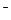 . За счет осмолитов достигается осмотическое равновесие цитозоля с вакуолями и всеми остальными органеллами клетки.
. За счет осмолитов достигается осмотическое равновесие цитозоля с вакуолями и всеми остальными органеллами клетки.
Наряду с осморегуляцией совместимые вещества выполняют еще одну, очень важную при дегидратации функцию. Эта функция может быть определена как защитная (протекторная) по отношению к цитоплазматическим биополимерам. Подчеркивая двойную функциональную роль осмолитов, их часто называют осмопротекторами. К настоящему времени накопилось много экспериментальных фактов, свидетельствующих об их защитных свойствах. Следует, однако, отметить, что доказательства защитного действия совместимых веществ получены в основном в экспериментах in vitro. Например, на препаратах из листьев растений показано, что глицин-бетаин предотвращает NaCl-индуцированную инактивацию рибулозобисфосфаткарбоксилазы и дестабилизацию выделяющего О2 комплекса фотосистемы II.
Считается, что осмолиты не разрушают гидратные оболочки биополимеров. На рис. 8.3 показана гидратная оболочка белка, состоящая из упорядоченных молекул воды. Ионы, например Na+ и Сl 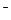 , могут проникать через гидратную оболочку и влиять на нековалентные связи, которые поддерживают структуру белковой молекулы. В отличие от Na+ и Сl
, могут проникать через гидратную оболочку и влиять на нековалентные связи, которые поддерживают структуру белковой молекулы. В отличие от Na+ и Сl 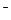 осмолиты, такие, как пролин и глицин-бетаин, не проникают через гидратную оболочку и не вступают в прямой контакт с белком, но создают препятствие для разрушения ионами гид-ратной оболочки белка и его денатурации.
осмолиты, такие, как пролин и глицин-бетаин, не проникают через гидратную оболочку и не вступают в прямой контакт с белком, но создают препятствие для разрушения ионами гид-ратной оболочки белка и его денатурации.
Некоторые низкомолекулярныё органические соединения, синтез которых индуцируется стрессорным воздействием, образуются в клетках в количествах, явно недостаточных для выполнения осморегуляторной функции. Тем не менее они играют важную роль при стрессах как протекторы биополимеров. К таким соединениям относятся диамин путресцин и образующиеся из него полиамины спермидин и спермин (см. далее рис. 8.8). Полиамины широко распространены в растениях. Они стимулируют реакции, вовлеченные в синтез ДНК, РНК и белков. Как поликатионы, полиамины обладают высоким сродством к биомолекулам, несущим отрицательные заряды, в частности к ДНК, РНК, фосфолипидам и кислым белкам, а также к анионным группам компонентов мембран и клеточных стенок. В растениях полиамины вовлечены во многие физиологические процессы, включая клеточное деление, формирование цитоскелета, инициацию роста корней, эмбриогенез и созревание плодов.
Полиамины предотвращают повреждения биомолекул, вызываемые засухой, засолением, низкими температурами и озоном. Структуры ДНК, РНК, рибосом, а также мембран, находящихся в комплексе с полиаминами, стабилизируются. Снижая активности РНКаз и протеаз, увеличенные в стрессовых условиях, полиамины повышают точность считывания информации при синтезе белков и тормозят лизис клеточных структур.
Механизм стабилизирующего действия полиаминов может быть рассмотрен на примере ДНК, являющейся сильной многоосновной кислотой. Она полностью ионизирована при рН выше 4. При цитоплазматических значениях рН отрицательно заряженные фосфатные группы, расположенные на периферии двойной спирали, образуют ионные связи с положительно заряженными аминогруппами спермидина и спермина, что предохраняет ДНК от повреждений.
Рис. 8.3. Протекторная функция пролина (Про). Пролин препятствует денатурации белка, вызываемой ионами Na+ и Сl  (Е. Bray et al., 2000)
(Е. Bray et al., 2000)
 2015-06-26
2015-06-26 6561
6561








