14. Привести условия термодинамической конъюгации двух процессов
Пусть в системе одновременно протекают две стехиометрические брутто-реакции, реализуемые за счет некоторой совокупности элементарных химических реакций. Обозначим эти брутто-реакции индексами Σ1 и Σ2. Очевидно, что при условии стехиометричности брутто-превращений выражение для diS / dt можно записать без привлечения к рассмотрению элементарных реакций:
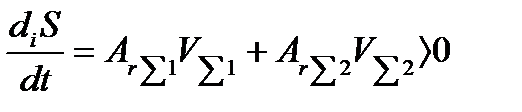 (1.9)
(1.9)
При этом неравенство (1.9) может выполняться не только при ArΣ1vΣ1 > 0 и ArΣ2vΣ2 > 0, но и, вообще говоря, при ArΣ1vΣ1 > 0, но ArΣ2vΣ2 < 0. Однако в последнем случае обе брутто-реакции обязаны быть взаимозависимыми. В рассматриваемом случае первую реакцию, способную в соответствии с требованиями термодинамики протекать самопроизвольно, называют сопрягающей, а вторую – сопряженной к первой. В гл. 2 показано, что сопряжение реакций возникает обычно только в ситуации, когда брутто-процессы состоят из набора элементарных стадий с общими для брутто-реакций интермедиатами, не входящими непосредственно в запись стехиометрических брутто-превращений.
Именно термодинамическое сопряжение двух процессов позволяет сопряженной реакции протекать, в принципе, даже в таком направлении, когда величины ArΣ2 и vΣ2 для брутто-
процесса обладают разными знаками, т. е. когда осуществление брутто-реакции Σ2 формально приводит к уменьшению энтропии.
Типичными примерами сопрягающей и сопряженной реакций являются соответственно реакция, катализируемая некоторым катализатором, и замкнутая цепь химических превра-
щений собственно катализатора в ходе его промежуточных химических взаимодействий с реагентами. Простейшую совокупность таких реакций для катализируемой брутто-реакции
R↔ P (1.10)
можно изобразить схемой Михаэлиса–Ментен
R + K ↔K1, (1.11)
K1↔ K + P
с наглядной графической иллюстрацией циклических превращений катализатора:
Здесь R и Р – исходный реагент и продукт каталитической реакции соответственно, а K и K1 – «свободная» форма активного центра катализатора и каталитический интермедиат. При этом сопрягающей реакцией является непосредственно катализируемая реакция (1.10) со сродством ArΣ1 = μR – μP, а сопряженной – циклические превращения (1.11) с участием активного центра катализатора. Сопряжение процессов происходит за счет наличия общих интермедиатов K и K1.
В данном конкретном случае в силу цикличности каталитических превращений их результирующее сродство ArΣ2 = 0.
Реальные каталитические процессы описываются схемами, намного более сложными, чем последовательность реакций (1.10). Еще более сложным примером сопряжения химических систем является жизнедеятельность живых организмов за счет реакций клеточного метаболизма.
Когда в системе с двумя стехиометрическими брутто-реакциями протекание сопряженной реакции уменьшает энтропию, условие (1.9) определяет верхний допустимый предел скорости сопряженной реакции: |VΣ2|≤ |ArΣ1VΣ1/ ArΣ2|.
Это позволяет связать чисто термодинамический параметр сопряженного процесса – химическое сродство – с важнейшей кинетической характеристикой процесса – скоростью реакции. При этом величину отношения |VΣ2ArΣ2/ VΣ1ArΣ1| можно рассматривать как энергетическую эффективность сопряжения, которая показывает, какая доля потенциала Гиббса сопрягающей реакции «вкладывается» в термодинамически запрещенную сопряженную. Термодинамическое сопряжение возможно не только для химических реакций, но и для других термодинамических
процессов, например переноса вещества, теплоты и т. п. Наличие верхнего допустимого предела энергетической эффективности сопряжения не является, естественно, свидетельством того, что сопряжение в системе реально имеет место. Как уже отмечалось, необходимым условием сопряжения химических брутто-реакций является наличие как минимум одного общего промежуточного компонента (интермедиата) в этих реакциях. Нахождение истинной величины сопряжения – отдельная и обычно очень конкретная задача
 2015-07-02
2015-07-02 322
322








