18. Дать понятие абсолютной скорости химической реакции
В химических реакционноспособных системах термодинамические потоки параметров, описывающих превращения, непосредственно связаны со скоростью химических реакций. Взаимосвязь между скоростью химической реакции и физико-химическими параметрами системы (концентрацией реагентов, температурой и т. п.) является предметом специального раздела физической химии – химической кинетики.
Традиционно в химической кинетике главными параметрами являются константы скорости реакций и концентрации реагентов. Для термодинамического анализа наиболее эффективными оказываются параметры типа химического потенциала. Поэтому для рассмотрения химических превращений в термодинамике неравновесных процессов наиболее удобной является «термодинамическая» форма записи кинетических уравнений. Ниже приведены основные элементы использования этой записи.
Рассмотрим термически инициированную (спонтанно протекающую) элементарную химическую реакцию ij
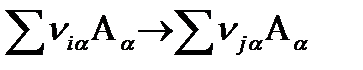
где Аα – компоненты реакции с концентрацией Cα (α = 1, 2,...,k), а Viα-стехиометрический коэффициент, с которыми этой компоненты входят в реакционную группу i.В химической кинетике скорость W ij рассматриваемой реакции «слева направо», т. е. число актов превращений реакционной группы i в реакционную группу j в единице объема и в единицу времени при протекании реакции при заданных температуре и давлении и сохранении распределения Больцмана в заселенности энергетических уровней переходного состояния (активированного комплекса) описывают законом действующих масс
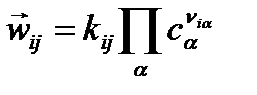
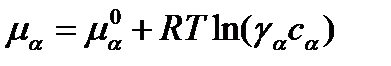 где kij – константа скорости реакции превращения i в j.
где kij – константа скорости реакции превращения i в j.
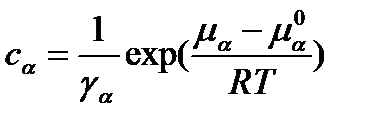 В общем случае где γα – коэффициент активности вещества Аα. Поэтому
В общем случае где γα – коэффициент активности вещества Аα. Поэтому
и выражение для скорости элементарной химической реакции любого порядка можно записать в следующем виде:
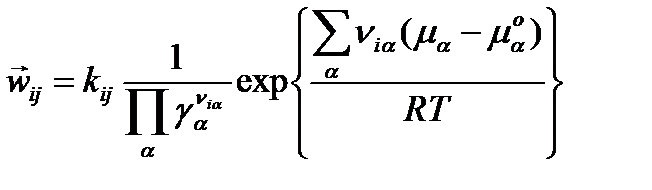
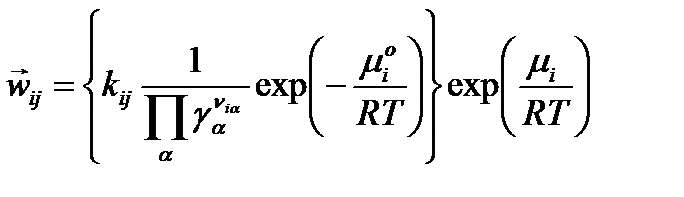
=
Здесь 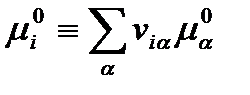 и
и 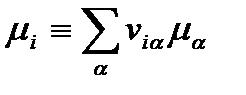 соответствуют стандартному и текущему значениям «химического потенциала» реакционной группы i в целом.
соответствуют стандартному и текущему значениям «химического потенциала» реакционной группы i в целом.
Введем обозначения
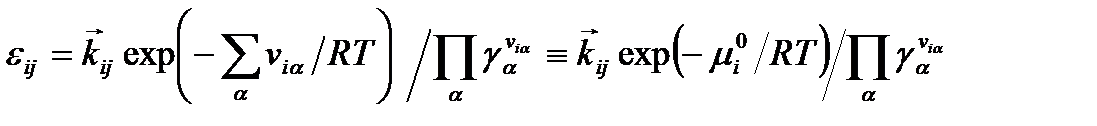 (1.14)
(1.14)
И
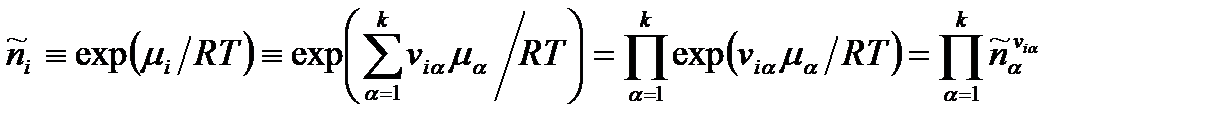 (1.15)
(1.15)
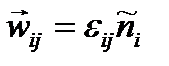 При этом, очевидно
При этом, очевидно
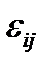
- усеченные константы скорости реакции (пропорциональны «вероятности» осуществления реакции по данному пути, не зависят от стандартных термодинамических характеристик реагентов, зависят только от термодинамических характеристик переходного состояния)
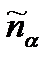 - Абсолютная активность компонентов
- Абсолютная активность компонентов
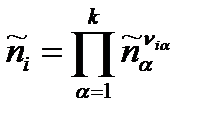
 2015-07-02
2015-07-02 523
523








