Кислоты, обладающие сильными окислительными свойствами HNO3 (концентрированная и разбавленная), H2SO4 (концентрированная) взаимодействуют как с металлами, стоящими в ряду напряжений до водорода, так и с металлами, стоящими после Н2. Характер продукта восстановления кислоты определяется концентрацией кислоты, активностью металла и температурой.
Cu + 2H2SO4 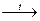 CuSO4 + SO2↑+ H2O
CuSO4 + SO2↑+ H2O
конц.
4Ca + 5H2SO4→4CaSO4+ H2S↑ + 4 H2O
конц.
4Ba +10HNO3→4Ba(NO3)2+N2O↑+ 5H2O 
конц.
Ag + 2HNO3→AgNO3 + NO2↑ + H2O
разб.
4Ca+10HNO3→4Ca(NO3)2+NH4NO3+3H2O
разб.
Соли
Солями называют соединения, состоящие из положительно заряженных ионов (катионов) и отрицательно заряженных ионов (анионов).
 2015-07-14
2015-07-14 629
629








