Длительное время в науке существовало представление, что моносахариды являются соединениями только с открытой углеродной цепью.
Однако при более глубоком изучении их строения было установлено, что цепные формулы не объясняют некоторых химических свойств и не объясняют таких фактов:
1. Почему моносахариды не присоединяют бисульфит натрия?
2. Не дают окрашивания с фуксинсернистой кислотой.
3. Чем обусловлены превращения маннозы, глюкозы и фруктозы друг в друга под действием щелочей?
4. Почему у моносахаридов появляется мутаротация, которая связана с изменением угла вращения при стоянии свежеприготовленных растворов? Если приготовить раствор глюкозы и поместить в поляриметр, то угол вращения равен 112°. Глюкоза отклоняет плоскость поляризованного луча света на 112°, через 2 часа на 90°, через 3 часа — на 60° и окончательно на 52,5°.
5. Почему при рассмотрении формулы глюкозы в ней можно насчитать 5 гидроксильных групп и только одна отличается своей реакционной способностью?
Чтобы ответить на эти вопросы, надо познакомиться с двумя видами таутомерии: карбонильно-ендиольной и цикло-оксо-таутомерией.
Углеродный скелет молекулы моносахаридов может изгибаться, приобретая форму «ухвата» (клешни). При этом альдегидная группа и гидроксильные группы при С4 или С5 находятся на расстоянии, равном примерно одной ковалентной связи, и между ними происходит химическое взаимодействие, подобно реакции между альдегидами и спиртами:
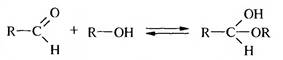
Продуктами реакции являются полуацетали.
В соответствии с теорией напряжения циклов наиболее выгодно взаимодействие, приводящее к образованию пяти- или шестичленных циклов.
Шестичленный цикл образуется при взаимодействии альдегидной группы с гидроксильной группой при С5 альдогексоз или С6 кетогексоз. Такой цикл называется пиранозным.
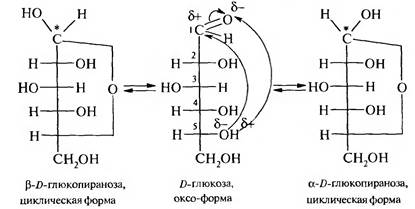
При взаимодействии альдегидной группы с гидроксильной группой при С4 альдогексоз или С, кетогексоз образуется пятичленный цикл, который называется фуранозным.
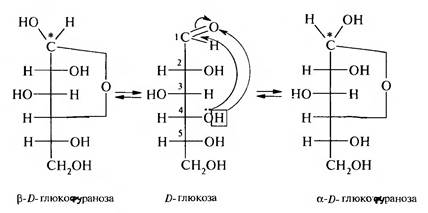
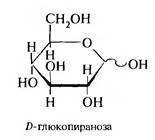
Так образуются полуацетальные циклические формы глюкозы. Приведенные циклические формы моносахаридов называются формулами Колли — Толленса.
Внутримолекулярное образование полуацеталя приводит к тому, что атом углерода карбонильной группы превращается в асимметрический. Этот новый хиральный центр называется аномерным. При этом образуется два новых стереоизомера, которые получили названия α- и β-аномеров.
Гидроксильная группа при аномерном центре называется полуаце- тальной, или гликозидной.
Поскольку формулы Колли — Толленса неудобны для изображения циклических структур, более удобны для написания и понимания проекционные формулы Хеуорса. В этом случае циклические формы моносахаридов изображаются в виде плоских многоугольников с атомом кислорода в цикле.
Для того, чтобы перейти от формул Колли — Толленса к формулам Хеуорса, необходимо учитывать такие правила:
1. Заместители, расположенные в формуле Колли — Толленса слева, в формуле Хеуорса изображаются над плоскостью, а заместители, расположенные справа, — под плоскостью цикла.
2. У альдоз D-ряда в пиранозной форме группа —СН2ОН, а в фуранозной — группа —СН(ОН)СН2ОН всегда расположены вверху, над плоскостью цикла.
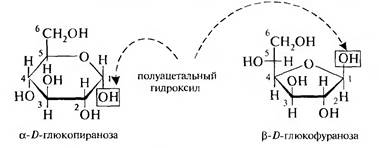
Аналогично изображаются с помощью формул Хеуорса пиранозные и фуранозные формы кетогексоз.

Для изображения смеси α- и β-аномеров в формуле Хеуорса расположение полуацетального гидроксила показывают волнистой линией.
 2015-08-12
2015-08-12 1157
1157








