Ситуация существенно изменяется при включении ферментов в концентрированные полимерные гели. Здесь в силу стерических препятствий, вносимых частой пространственной сеткой полимера, поступательное и, возможно, вращательное движение белковых молекул существенно заторможено. В результате в таких системах образование комплекса белок — матрица становится термодинамически гораздо более выгодным, поскольку здесь уже не требуется затрат свободной энергии для погашения потерь поступательной и вращательной энтропии ферментной глобулы при ее сорбции на полимерной матрице. Благодаря этому в концентрированных полимерных гелях становится возможным многоточечное взаимодействие (за счет слабых нековалентных сил) фермента с носителем^ поскольку в таких гелнх^полимерные цепи со всех сторон окружают ферментную глобулу. Такое многоточечное взаимодействие в гелевых системах действительно имеет место; оно приводит к существенной стабилизации ферментов. Так, а-химотрипсин, иековалентно включенный в заряженный гель по-лиметакриловой кислоты, в Ю5 раз более термостабилен, чем натнвный фермент, если концентрация полимерных цепей в геле составляет 50%.
Говоря о практическом применении гелевых систем, необходимо отметить один их существенный недостаток. Частички геля склонны к набуханию в воде, что приводит к снижению концентрации полимерных цепей в геле. В результате эффект стабилизации включенного в гель фермента может уменьшаться и даже вовсе исчезать, поскольку, как обсуждалось, для реали аза ции многоточечного не ко валентно го взаимодействия фермента с носителем необходимо, чтобы гель был достаточно концентрированным. Поэтому практическую ценность с точки зрения повышенной стабильности препарата биокатализатора в суспензии имеют только те системы, в которых молекулы фермента включены в «сильное шитые»» не набухающие в воде гелевые частицы.
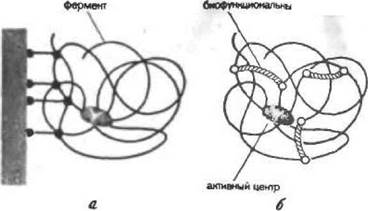
Многоточечное ко валентное присоединение фермента к поверхности носителя (рис. 24, а). Другой путь у жестчения структуры фермента заключается в его иммобилизации на носителе с образованием большого числа ковалентных связей. Для реализации многоточечного взаимодействия необходимо, чтобы размеры ферментной глобулы и поры носителя соответствовали друг другу. Если проводить иммобилизацию белка на произвольно взятом носителе, то такое соответствие можно получить лишь случайно, поскольку поверхность носителя и поверхность белка имеют свои индивидуальные рельефы, в общем случае не комплементарные друг другу.
Этого недостатка лишен сополимеризационный метод иммобилизации, позволяющий создать полимерный носитель, комплементарный молекуле фермента. Фермент химически модифицируют (например, по аминогруппам) аналогом мономера, т.е.
|
|
| и р#агвкт |
Рис. 24. Схематическое изображение иммоби-лнэационных подходов к стабилизации ферментов
соединением, содержащим ненасыщенные связи (например, хло-рангидридом акриловой кислоты или акролеином). При последующей сополимеризации с мономером (например, с акрила-мидом кли метакрилатом натрия) белковая глобула формирует вокруг себя поверхность носителя, комплементарную собственной, ковалентно к ней присоединяясь. Сополимеризационный метод дает уникальную возможность получать препараты ферментов, пришитых различным числом ковалентных связей к поверхности носителя, за счет варьирования степени модификации на стадии обработки фермента аналогом мономера.
Ферменты, иммобилизованные по сополимеризационной методике, обладают гораздо более высокой устойчивостью против инактивации при повышенных температурах, чем соответствующие нативные ферменты. Эффект стабилизации, определяемый как отношение констант скоростей необратимой инактивации нативного и иммобилизованного препаратов, возрастает с увеличением числа связей между ферментом и носителем и достигает больших величин. Например, для а-химотрипсина, пришитого к носителю 15 связями, стабилизационный эффект составляет более 1000 раз. Такие ферментные препараты сохраняют каталитическую активность при существенно более высоких температурах. Так, например, оптимум эстеразной активности трипсина, ковалентно вшитого в полиакриламндный гель 15 связями, наблюдается при температуре 75°С, что на 25° выше оптимума активности нативного фермента. Это указывает на резкое подавление быстрых обратимых денатурационных процессов в иммобилизованном препарате.
Следует отметить, что эффект стабилизации для иммобилизованного по сополимеризациониой методике фермента зависит только от числа ковалентных связей с носителем, но не зависит ни от плотности гелевого носителя (т.е. от концентрации полимера в геле), ни от степени его набухания. Более того, проводя сополимериза цнонную иммобилизацию в отсутствие бифункцио* нального сшивающего агента, удается получить водорастворимые
ферментные препараты, также обладающие повышенной термостабильностью.
Внутримолекулярное сшивание фермента бифункциональными реагентами (рис. 24,6). Модификация фгрмента бифункциональными агентами в принципе может принести к наложению на белковую глобулу внутримолекулярных ковалентных сшивок. Следует ожидать, что сшивание увеличит конформацнонную жесткость белка и, следовательно, его стабильность. Этот подход (внутримолекулярное сшивание белка) активно используется в природе для увеличения стабильности белковых структур. К числу «природных сшивок» относятся как ковалентные S—S-связи, так и нековалентные «солевые мостики», ионы Сай+ и других металлов, связанные с молекулой белка, и т. п.
Успех или неудача при попытке повысить стабильность фермента обработкой бифункциональными реагентами в основном определяется соответствием длины реагента расстоянии") между возможными центрами пришивки на белковой глобуле. Очевидно, что для каждого конкретного белка существует оптимальный размер сшивающих агентов. Единственно надежный путь определения размера подходящего реагента — эмпирический поиск. Для этого изучаемый фермент модифицируют соединениями гомологического ряда бифункциональных реагентов, например алифатических диаминов или имидоэфиров алифатических ди-карбоновых кислот, в условиях, когда не происходит межмолекулярного сшивания белковых молекул. Далее изучают зависимость стабилизационного эффекта от длины бифункционального реагента. Обычно такие зависимости имеют вид кривой с максимумом. Дело в том, что при модификации бифункциональным реагентом наряду с образованием «сшивок» происходит одноточечная модификация функциональных групп белка. Соотношение этих двух процессов тем сильнее сдвинуто в сторону реакции сшивания, чем больше на поверхности белковой глобулы пар функциональных групп, расстояние между которыми примерно равно длине сшивающего агента. Именно в этом случае наблюдаются максимальные стабилизационные эффекты.
Следует отметить, что эмпирический характер поиска оптимального сшивающего агента несколько снижает ценность метода внутримолекулярного сшивания белков для практических целей. Действительно, для каждого вновь взятого белка или при использовании нового гомологического ряда бифункциональных реагентов работу по подбору наилучшего сшивающего агента надо проводить заново.
Тем не менее метод сшивок весьма полезен, поскольку позволяет получать водорастворимые стабилизированные производные ферментов с относительно низкой молекулярной массой (сравнимой с молекулярной массой самого фермента). Такие препараты предпочтительны в некоторых прикладных областях, в члетмоети в медицине
 2015-08-13
2015-08-13 625
625








