Інфекційний мононуклеоз (mononucleosis infectiosa, хвороба філатова — Пфейфера) — вірусне контагіозне захворювання, яке передається повітряно-крапельним, а можливо, й аліментарним шляхом, і характеризується класичною тріадою: гарячка, ангіна, аденоспленомегалія.
Вхідними ворітьми інфекції є зів і носова частина глотки. Вірус поширюється лімфогенним і гематогенним шляхами.
Клініка. Інфекційний мононуклеоз трапляється частіше навесні та восени. Хворіють діти та молоді люди, рідше — люди похилого віку.
Інкубаційний період становить від 7—15 до 49 діб. Захворювання починається гостро. Одним із перших і досить постійних
симптомів є поліаденіт. Особливо чітко збільшуються задньо-шийні та підщелепні лімфовузли. Поряд з цим значно збільшуються і стають щільними печінка та селезінка. Закономірним симптомом хвороби Філатова є гарячка. У більшості хворих температура тіла швидко наростає до 39—41 °С, часто без продрому. Температурна крива буває постійного, ремітуючого або хвилеподібного типу. Високі показники температури тіла можуть утримуватись від 3—4 до 20 діб і більше, спадає вона поступово.
Зів різко гіперемійований, інколи з ціанотичним відтінком, як прояв аденопатії має місце гіперплазія мигдаликів. Ангіна (катаральна, лакунарна, фолікулярна, некротична, плівчаста) може розвинутися в різних стадіях хвороби, має стійкий тривалий перебіг і не піддається лікуванню антибіотиками. На 3-тю — 4-ту добу захворювання на межі твердого і м'якого піднебіння з'являються петехії.
Залежно від тяжкості перебігу інфекційного мононуклеозу може розвинутися катаральний, герпетичний або виразково-некротичний стоматит, який нерідко супроводжується пете-хіальними крововиливами на CO та шкірі. Язик обкладений сірувато-білим нальотом, відзначається виражена гіперплазія грибоподібних сосочків та язикового мигдалика. Обличчя хворих набрякле (одутле), носове дихання утруднене, можливі носові кровотечі. Інколи, з перших днів захворювання, на обличчі, кінцівках і тулубі можлива поява яскравого поліморфного розе-ольозного висипу.
Діагностика. Крім клінічних ознак, важливе значення в діагностиці мононуклеозу має гемограма. Уже з перших днів хвороби (інколи з 12—14-го дня) спостерігаються лейкоцитоз, збільшення всіх одноядерних клітин (лімфоцитів і моноцитів), поява плазматичних клітин та досить великої кількості (15—30% клітин і більше) атипових мононуклеарів (широкоплазмових одноядерних клітин з ексцентричне розміщеним ядром, широким поясом протоплазми та наявністю в ній зернистості). Еозинофіли майже відсутні. Вміст гемоглобіну та еритроцитів близький до норми, ШОЕ становить 20—30 мм/год.
Диференціальна діагностика. Проводять розмежування з дифтерією (розрізняють за картиною крові та наявністю аденоспле-номегалії), агранулоцитозом (супроводжується анемією, лейкопенією, геморагічним синдромом та виразково-некротичною агранулоцитарною ангіною), лейкозом (у картині крові відсутні зміни, характерні для гострого чи хронічного лейкозу).
Лікування. Специфічної терапії мононуклеозу не існує. У тяжких випадках з метою впливу на вторинну мікрофлору призначають антибіотики або антибіотики в поєднанні з середніми дозами кортикостероїдних засобів, протигістамінні засоби та комплекс вітамінів.
Місцеве лікування полягає у зрошенні та полосканні зіва та ротової порожнини (риванол, фурацилін, етоній, мікроцид, ек-терицид та ін.). Виразково-некротичні ускладнення на СОПР лікують, як стоматит Венсана.
ЯЩУР
Ящур (aphthae epizooticae) викликається фільтрівним вірусом. Зараження, в основному, відбувається при вживанні молочних продуктів та м'яса хворих на ящур тварин. Вірус проникає в організм людини крізь ушкоджену шкіру та CO.
Інкубаційний період становить близько 3 діб. Захворювання починається гостро, з ознобу; температура тіла протягом 3—4 год підвищується до 38,5—39 °С. Типовими ознаками є загальна слабість, біль голови, у суглобах, м'язах. З'являються відчуття печіння в роті та надмірне слиновиділення.
Через 1—2 доби на гіперемійованій і набряклій CO виникають невеликих розмірів пухирці, які лопаються, і на їх місці утворюються афтоподібні елементи. Можливе одночасне ураження CO носа, очей, статевих органів. Ураження СОПР часто супроводжується подібним до нього ураженням шкіри біля крил носа, а також міжпальцевих складок, основ нігтів, підошов. Одужання настає через 2—3 тиж.
Диференціальна діагностика. Ящур треба диференціювати від герпетичного стоматиту, синдрому Бехчета, БЕЕ, медикаментозної алергії, виразково-некротичного стоматиту Венсана та ін.
Лікування. Стоматолог проводить місцеву терапію, як при герпетичному стоматиті.
СНІД
Синдром набутого імунодефіциту (СНІД, AIDS - syndromum immunodefectionis aguisitae) — контагіозне імунне захворювання вірусної етіології.
Етіологія. СНІД спричиняється вірусом, що належить до родини ретровірусів, підродини лентивірусів. Таксономічним комітетом ВООЗ він був названий HIV (Human immunodeficit virus), українською — вірус імунодефіциту людини (ВІЛ). Відкрив його французький вірусолог Л.Монтаньє 1983 p. Виявлено 3 різновиди вірусу.
ВІЛ малостійкий у зовнішньому середовищі: при нагріванні до 56 °С він гине протягом ЗО хв, його вбивають усі дез-інфікуючі засоби, сонячне проміння. При температурі 25 °С інфекційність вірусу зберігається протягом 15 діб, при 37 °С — 11 діб, при кімнатній температурі — 47 діб.
Проникаючи в багато які клітини різних тканин (не лише у лімфоцити) ВІЛ розвивається в них. Травний канал взагалі час-
то буває первинними ворітьми проникнення ВІЛ (особливо у гомосексуалістів). ВІЛ уражає ЦНС та розвивається в її клітинах. Значний відсоток хворих мають кардіологічні зміни, які не зумовлені кардіотропними опортуністичними інфекціями. Одним із перших проявів ВІЛ-інфекції є ураження сітківки ока. Окрім Т-лімфоцитів, ВІЛ виявлений у моноцитах (макрофагах із крові, лімфатичних вузлів, тканини легень), отриманих від заражених хворих. Крім крові та клітин тканин, вірус міститься в спинномозковій рідині, вагінальному секреті, сльозах, слині, грудному молоці, поті. Однак вміст його в біологічних рідинах набагато нижчий, ніж у крові, тому й можливість зараження через них значно менша.
Традиційно вважають, що вірус передається з біологічними рідинами організму трьома основними шляхами: 1) під час статевих контактів; 2) при переливанні крові та її продуктів і при повторному використанні нестерильних голок та інших інструментів; 3) внутрішньоутробно — від матері до плоду.
Проте шкіра і CO фактично можуть бути ворітьми інфекції:
оскільки до ВІЛ чутливі клітини Лангерганса шкіри та CO, то для того щоб відбулося зараження, вірусу не обов'язково потрапляти в кров. Такий спосіб переносу ВІЛ веде до інфікування людини значно раніше, ніж статеві контакти. Але за такої передачі інфекції кількість вірусів, що переносяться в організм здорової людини, у сотні (або навіть тисячі) разів менша, а відтак інфікування організму людини можливе лише у разі особливої чутливості його до ВІЛ. Ризик захворювання зумовлюється двома чинниками — кількістю вірусів, що потрапили в організм, та схильністю організму до захворювання.
На основі результатів епідеміологічних досліджень установлені групи ризику: гомосексуалісти, повії, хворі на наркоманію, гемофілію, новонароджені діти жінок, хворих на СНІД, а також особи, що мешкають в ендемічній зоні, медперсонал. За даними Американської асоціації дантистів, лікарі-стоматологи посідають 2-ге місце серед представників інших медичних професій за небезпекою зараження на СНІД. Ось чому знання основних клінічних проявів СНІДу, особливо уражень порожнини рота, є актуальним для широкого кола стоматологів та інших медичних працівників, пов'язаних у своїй діяльності зі стоматологією.
Проникнувши в організм, ВІЛ здатний розмножуватися практично у будь-яких клітинах тканин організму, викликаючи його загальне ураження. Ступінь ураженості клітин різний.
Після потрапляння в організм людини та інтеграції до її геному ВІЛ деякий час може бути неактивним або малоактивним, а згодом починає функціонувати на повну силу. В останньому випадку клітина стає «фабрикою» вірусу. У період активності лімфоцити периферичної крові продукують протягом З днів до 2,5 млн копій вірусної РНК, при цьому до 40% білків, що син-
тезуються, є вірусними. І цією «фабрикою» вірусу є, по суті, не окрема клітина, а весь організм. Лімфоцити після напруженого продукування вірусу гинуть Але це не зупиняє «фабрику». Зі стовбурових клітин (в них вірус якщо й наявний, то в неактивній формі) утворюються попередники (вони теж не продукують вірус у помітних кількостях), і з них, зрештою, диференціюються лімфоцити, які вибухають вірусним синтезом і змінюються новими лімфоцитами.
Таким чином, на відміну від інших вірусів, для яких їх вибухова продукція завершується разом із загибеллю продукуючих клітин, ВІЛ може надалі функціонувати у такому вибуховому режимі багато місяців — весь активний період хвороби. Як наслідок, вірусний матеріал і для інфекції, і для еволюції утворюється з надлишком
Згідно з поширеною думкою, механізмом СНІДу є руйнування ВІЛ імунної системи внаслідок інфікування та загибелі Т-хелперів (Ї4), на цитоплазматичній мембрані яких є білок СД-4, що слугує рецептором для ВІЛ.
Т-хелпери у нормі становлять 60—80% циркулюючих у крові Т-лімфоцитів, або 800 в 1 мм3. Співвідношення Т-хелпери/Т-супресори становить 2:1. При вторгненні в клітину вірус необоротно змінює її, використовуючи генетичний матеріал клітини для власної репродукції: утворена ДНК включається в хромосоми клітин і перетворюється на провірус, який може перебувати в неактивній формі або проявити себе, синтезуючи вірусні білки. У разі активації, що відбувається при загальному ослабленні імунітету, ВІЛ починає швидко розмножуватись, захоплюючи Т-хелпери, і викликає їх загибель. Унаслідок порушення рівноваги в системі Т-хелпери—Т-супресори останні починають пригнічувати імунітет.
Крім кількісних порушень у системі Т-лімфоцитів наступають численні якісні зміни. Механізм пригнічення клітинного імунітету включає цитопатичну дію ВІЛ, токсичну дію його компонентів, а також цитотоксичну дію макроорганізму на власну СД-4 фракцію Т-лімфоцитів, що набули антигенних властивостей.
На цьому фоні організм стає беззахисним щодо опортуністичних інфекцій, розвиток яких і складає клінічну картину СНІДу.
Проте це уявлення про СНІД, як і багато інших, тільки частково висвітлює реальну ситуацію. Крім безпосереднього ураження частини клітин імунної системи (СД-4 фракція Т-лімфоцитів), ВІЛ впливає на імунітет і за іншими механізмами. Так, на С-кінці оболонкового білка ВІЛ є гексапептид, ідентичний домену інтерлейкіну-2, який взаємодіє з його рецептором. Як наслідок, білок оболонки ВІЛ блокує рецептори медіатора клітинного імунітету інтерлейкіну-2. порушуючи таким чином утворення Т-лімфоцитів (інтерлейкін-2 є чинником росту Т-лімфоцитів).
Білок р18, продукт протеолізу білка gag ВІЛ, має ділянку, гомологічну тимозину осі. Внаслідок цього відбувається блокування рецепторів до тимозину а,, який відповідає за активацію імунних клітин. Білок nef ВІЛ-1 має ділянку, гомологічну позаклітинному домену В-ланцюга антигенів гістонесумісності класу II. Це стимулює утворення антитіл до даного антигену та розвиток автоімунного процесу, що руйнує імунну систему. ВІЛ-2 не має подібної гомології і це відповідає його більш низькій патогенності.
Нарешті, ВІЛ здатний безпосередньо уражувати не лише клітини імунної системи. Фрагмент Сір-120 білка оболонки ВІЛ гомологічний нейролейкіну і спроможний об'єднуватися з його рецепторами в мозку. Це призводить до конкуренції з нейро-лейкіном і порушує нервові функції.
Білок-трансактиватор tat ВІЛ на С-кінці має ділянку, що специфічно зв'язується із синаптосомальними мембранами мозку. Це сполучення є високонейротоксичним і спричиняє загибель нервових клітин. Сам білок tat, крім того, справляє ще й прямий гіперпластичний вплив на клітини шкіри. Унаслідок його дії відбувається гіперплазія, подібна до саркоми Капоші, що спостерігається у хворих на СНІД.
Наслідком інфекції ВІЛ є продукування розчинного чинника (поки що не ідентифікованого), який порушує еритропоез. Під впливом ВІЛ зменшується кількість макрофагів, виникає лейкоцитоз, що переходить у лейкопенію, розвивається лімфо- і тромбоцитопенія або анемія, збільшується кількість циркулюючих імунних комплексів.
Дуже важливу роль (у багатьох випадках визначальну) як у інфікованих індивідуумів, так і в заражених у разі переходу хвороби з латентної форми у клінічну відіграють різноманітні гете-рологічні (тобто не ВІЛ-кодуючі) чинники, їх умовно можна поділити на три групи — неспецифічні, специфічні організмені та специфічні вірусні.
До першої групи належать усі чинники, що викликають ослаблення, загальне пригнічення організму, їх врахування дає змогу прогнозувати для ослаблених людей (і цілих популяцій) підвищену сприйнятливість інфекції та більш ранній початок активної фази хвороби. Найвідомішими конкретними неспецифічними чинниками СНІДу є наркотики (як супресори імунітету) та алкоголь у великих дозах. Можна вважати, що саме серед хворих на наркоманію та алкоголізм (разом з гомосексуалістами, у яких статеві зв'язки самі по собі спричинюють пригнічення імунітету) пройшов адаптацію прабатько ВІЛ, перш ніж зміг перейти в пандемію.
З-поміж специфічних організмених чинників СНІДу найбільше значення мають деякі лімфокіни, серед яких чинник некрозу пухлин має найбільшою мірою виявлену ВІЛ-активу-ючу функцію. Цей лімфокін утворюється у відповідь на різно-
манітні інфекції як захисний агент організму. З цієї причини будь-яке інфекційне захворювання, що не взаємодіє з ВІЛ, виявлятиме стимулюючу дію на СНІД через індукцію чинника некрозу пухлин (і меншою мірою деяких інших лімфокінів).
Специфічними вірусними (гетерологічними) чинниками СНІДу є трансактиватори вірусу гепатиту В та всіх вірусів групи герпесу. До 90% людей є довічними носіями вірусу герпесу в ЦНС. Різні герпесвіруси персистують у різних тканинах (у ЦНС, системі кровотворення, CO). Носіями вірусу гепатиту В у різних регіонах є десятки відсотків населення, і цей вірус пер-систує не тільки в клітинах печінки. Таким чином, для свого розвитку в організмі людини ВІЛ використовує не тільки потужність власного геному, а й геноми найпоширеніших, постійно присутніх в організмі людей вірусів. Нарешті, продукти, що синтезуються деякими вірусами, є допоміжними посттранс-крипційними активаторами ВІЛ. Так поводиться білок BMLF1 вірусу Епштейна — Барра (група герпесвірусів), PHKV4 аденовірусу тощо.
Отже, ВІЛ несе інформацію, необхідну для власного розвитку та подолання захисних сил організму. Він використовує вади людини й допомагає використовувати проти неї всю сукупну потужність різноманітних вірусів. Це досягається двома шляхами. З одного боку, ВІЛ та його геномна ДНК-копія мають структури, що впізнають трансактиватори різних вірусів, а це надзвичайно підсилює можливості ВІЛ. З іншого боку, ВІЛ (сам і через підсилення його функцій іншими вірусами) пригнічує захисні функції організму, відкриваючи в такий спосіб шлях собі та іншим вірусам, що активують його ще дужче.
Таким чином, ВІЛ під час свого розвитку в організмі людини може викликати ураження різних тканин навіть без зв'язку з опортуністичними інфекціями. Але разом з ними виникає той симптомокомплекс, який загалом описують як СНІД.
Особливе значення для розуміння незвичайності СНІДу та прогнозу його розвитку у вигляді пандемії має надзвичайно високий темп мінливості ВІЛ. Він визначається двома групами подій — мутаціями та рекомбінаціями. За темпом мутації ВІЛ не має собі рівних — швидкість його мінливості безпрецедентна. Мутації в геномі ВІЛ з'являються в 1 млн разів частіше, ніж у геномі ДНК-вірусів, і набагато частіше, ніж у всіх інших РНК-вірусів. Мінливість збільшується ще й через особливості структури геному ВІЛ. Незважаючи на невеликі розміри, геном ВІЛ має 9 генів — gag, pol, vif, vp/vpx, vpr, tat, rev, env, nef і безліч регуляторних сайтів.
Клініка. Для СНІДу характерна фазність перебігу. Тривалість інкубаційного періоду коливається від 6—8 міс до кількох років. Приблизно у 50% хворих він становить 4 роки.
Центр контролю за захворюваннями (Джорджія, США) і ВООЗ (1988) запропонували таку класифікацію клінічних стадій СНІДу:
I. Інкубація.
II. Гостра ВІЛ-інфекція.
III. Вірусоносійство: а) персистуюча інфекція; б) генералізована інфекція.
IV. Лімфаденопатія.
V. СНІД-асоційований комплекс.
VI. СНІД з розвитком інфекцій та пухлин.
Класифікація В.І.Покровського (1989) виділяє 4 стадії перебігу ВІЛ-інфекції:
І. Інкубація.
II. Стадія первинних проявів: а) фаза гострої гарячки; б) безсим-птомна фаза; в) персистуюча генералізована лімфаденопатія.
III. Стадія вторинних захворювань.
А. Втрата маси тіла менше ніж 10%, поверхневі грибкові, бактеріальні або вірусні ураження шкіри і CO, оперізувальний лишай, повторні фарингіти, синусити.
Б. Прогресуюча втрата маси тіла понад 10%, неясного генезу діарея, гарячка тривалістю більше 1 міс, волосяна лейкоплакія, туберкульоз легень, повторні або сталі бактеріальні, грибкові, вірусні та протозойні ураження шкіри і CO, повторний або дисемінований herpes zoster, локалізована саркома Калоші.
В. Генерал ізован і бактеріальні, вірусні, протозойні паразитарні захворювання, пневмоцистна пневмонія, кандидоз стравоходу, атиповий мікобактеріоз, позалегеневий туберкульоз, кахексія, дисемінована саркома Калоші, ураження ЦНС різної етіології.
IV. Термінальна стадія.
Рефлілл і Берке (1988) як об'єктивну основу розподілу симптомів і стадій хвороби, виявлення ступеня її тяжкості пропонують використовувати кількість Т4-лімфоцитів в 1 мм3 крові і виділяють 7 стадій:
І. Інкубація.
II. Безсимптомна.
III. Хронічна лімфаденопатія (ЛАП) протягом 3—5 років — пре-СНІД.
IV. Субклінічні порушення імунітету (в 1 мм3 крові міститься 400 Т4-лімфоцитів).
V. Поява алергічних реакцій на шкірні проби (число Т4-лімфоцитів у 1 мм3 крові менше 300).
VI. Імунодефіцит з ураженням шкіри й CO — відсутня гіпер-чутливість сповільненої дії (кількість Т4-лімфоцитів — менша ніж 200).
VII. Генералізовані прояви імунодефіциту — розвиваються ВІЛ-індикаторні опортуністичні інфекції, злоякісні пухлини ^-лімфоцитів менше 100).
Клініка СНІДу насамперед зумовлена дефіцитом Т-клітинного імунітету. Зниження активності імунної системи призводить до активації сапрофітної мікрофлори. Тому пік захворювання характеризується тяжкими інфекціями, спричиненими грибами, цитомегаловірусом, вірусом Епштеина — Барра, вірусом герпесу тощо, що не піддаються терапії (опортуністичні інфекції), або розвитком пухлин (саркома Калоші, лімфома не Ходжкіна та ін.). Встановлено, що СНІД може одночасно поєднуватися з герпетичною інфекцією та гепатитом В. Поряд із загальними симптомами досить часто у хворих на СНІД спостерігаються різні ураження порожнини рота. Вони мають значну діагностичну цінність, оскільки дозволяють легше і вірогідніше виявити прояви СНІДу у пацієнта й уникнути зараження медперсоналу. Прояви СНІДу в порожнині рота досить різноманітні, що викликає труднощі в їх систематиці.
У серпні 1990 p. в Амстердамі робочою групою провідних стоматологів з різних країн Європи було висунуто класифікацію проявів у порожнині рота, пов'язаних з ВІЛ-інфекцією. Запропоновано розрізняти три групи проявів на основі ступеня вірогідного зв'язку з ВІЛ-інфекцією.
Перша група — ураження СОПР, які найтісніше пов'язані з ВІЛ:
І. Кандидоз (еритематозний, гіперпластичний, псевдомембранозний).
2. Волосяна лейкоплакія (вірус Епштеина — Барра).
3. ВІЛ-гінгівіт.
4. Виразково-некротичний гінгівіт
5. ВІЛ-пародонтит.
6. Саркома Капоші.
7. Лімфома не Ходжкіна.
Друга група — ураження, що меншою мірою пов'язані з ВІЛ-інфекцією:
1. Атипові виразки (орофарингеальні).
2. Ідіопатична тромбоцитопенічна пурпура.
3. Захворювання слинних залоз (ксеростомія, одно- чи двобічне збільшення слинних залоз).
4. Вірусна інфекція (відмінна від зумовленої вірусом Епштеина — Барра): спричинена цитомегаловірусом, вірусом herpes simplex, людським папіломавірусом (бородавчасті ураження — кондилома гострокінцева, фокальна епітеліальна гіперплазія, бородавка звичайна), вірусом вітряної віспи (оперізувальний лишай, вітряна віспа)
Третя група — ураження, які, можливо, пов'язані з ВІЛ-інфекцією:
1. Бактеріальні інфекції (включаючи гінгівіт, пародонтит), актиномікоз, туберкульоз, а також спричинені Enterobacter cloacae, Echerichia coli, Klebsiella pneumoniae, Mycobactenum avium mtracellulare.
2. Хвороба котячої подряпини.
3. Загострення апікального періодонтиту.
4. Грибкова інфекція некандидозної етіології (криптококоз, геотрихоз, гістоплазмоз, мукоромікоз).
| Мал. 55 Гіперпластич-ний кандидоз v хворого на СНІД |
5 Меланінова гіперпп \існтація
6 Неврологічні порушення (тригемінальна невралгія, параліч лицьового нерва) 7. Остеомієліт 8 Синусит
9. Запалення підщелепної жирової клітковини (абсцес, флегмона) 10 Плоскоклітинна карцинома 11. Токсичний епідермоліз
Більшість авторів вважають, що першим проявом СНІДу після інфікування є ураження СОПР; на думку інших, порожнина рота уражається в термінальній стадії СНІДу, коли кількість Т4-лімфоцитів у 1 мм3 крові зменшується до 200. Спостерігаються швидкопрогресуючий пародонтит, гострий виразково-некротичний пнгівостоматит, ангулярний хейліт. Вогнища в перюдонті мають тенденцію до розвитку остеомієліту, досить часто розвивається бурхлива реакція на ендодонтичні втручання. Поява цих ознак може свідчити про неблагополуччя в осіб групи ризику задовго до таких проявів, як кандидоз та волосяна лейкоплакія.
За частотою наитіоширеніші захворювання СОПР розподіляються так: кандидоз (88%), герпетичні ураження (11—17%), ксеростомія (19—28%), ексфоліативний хейліт (9%), виразки (7%), десквамативний глосит (6%), волосяна лейкоплакія (5%), саркома Капоші (від 4 до 50%), геморагії.
Кандидоз СОПР у хворих на СНІД має декілька форм перебігу: псевдомембранозну, при якій спостерігається значна кількість м'яких білих вогнищ, що нагадують пластівці звурдженого
98і'іі 129
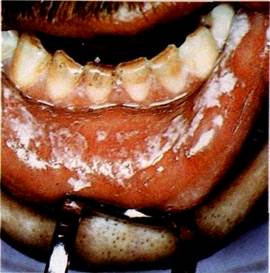
| Мал. 56 Атрофічний кандидоз слизової оболонки твердого піднебіння (й), СПИНКИ язика (б) v хворого на СН1Д |
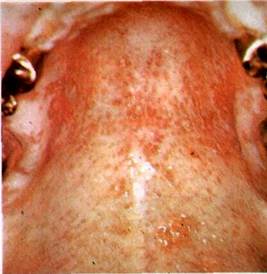
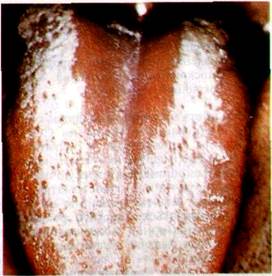
молока і легко знімаються при зіскрібанні; пперпластичну — на-гадує лейкоплакію, супроводжується наявністю щільних білих уражень, спаяних з поверхнею СОПР, і атрофічну (еритематозну) Остання форма характеризується виникненням еритематозних плям, на фоні яких спостерігаються псевдомембранозні зміни без нальоту, місцями — плями гіперкератозу (мал. 55, 56)
| Мал. 57 Виразково-некротичний стоматит при СНІДі |
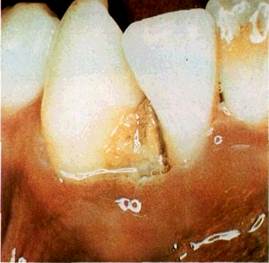
Із бактеріальних інфекцій має місце фузоспірохетоз, що зумовлює появу гострого виразково-некротичного гінгівіту у фронтальній ділянці Він трапляється у хворих на СНІД, носіїв антитіл, а також в осіб, у яких відзначаються позитивні серологічні реакції. В останньому випадку, крім того, виникає загострення вогнищ вторинної інфекції в періапікальних тканинах, а в пародонті можливі деструктивні зміни аж до секвестрації альвеолярної кістки (мал. 57).
Вторинні вірусні агенти викликають волосяну лейкоплакію. До цієї групи належать віруси герпесу, бородавок і кондилом. Волосяна лейкоплакія нагадує м'яку форму лейкоплакії і являє собою білясті волосяні розростання, які не знімаються при зіскрібанні. Вони розміщуються в основному по краю язика і дещо подібні до хронічного гіперпластичного кандидозу (мал. 58)
Гістологічна характеристика волосяної лейкоплакії: ниткоподібні кератинові утворення, паракератоз, блюдцеподібні клітини (як показники вірусної інфекції). Вважають, що волосяна лейкоплакія викликається вірусом Епштейна — Барра Ультраструктурними дослідженнями установлено, що волосяна лейкоплакія асоціюється з інфекцією бородавок та герпесу. Наявність цього ураження розцінюють як несприятливий чинник, що свідчить про перехід лімфаденопатії в СНІД
Виразки та афти в порожнині рота у хворих на СНІД частіше локалізуються на піднебінні і зумовлені Cryptococcus neoformans (дріжджі, що брунькуються і не утворюють міцелію) Інколи спостерігають поодинокі слизові капсули.
У гомосексуалістів-чоловіків раннім (першим) проявом СНІДу в порожнині рота може бути виникнення болючих виразок
| 9* |
| Мал. 58 Волосяна (м'яка) V лейкоплакія бічної поверхні язика при СНІДі |
| Мал. 59 Герпетичний стоматит у хворого на СНІД |
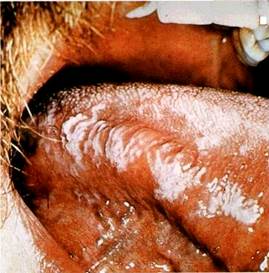
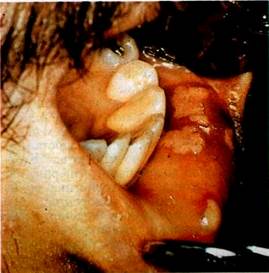
на CO піднебіння та язика, пов'язаних з цитомегаловірус-ною інфекцією (група вірусів герпесу), з характерним повільним, затяжним перебігом, рецидивуванням, відсутністю ефективності лікування за загальноприйнятими методиками Одночасно спостерігаються виразкове герпетичні ураження губ в зоні Клейна та CO носа (мал 59) Встановлено, що всі ранні
| Мал. 60 Саркома Калоші твердого піднебіння (а), ясен (б) при СНІДі |
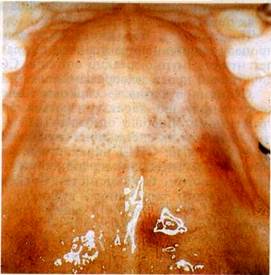
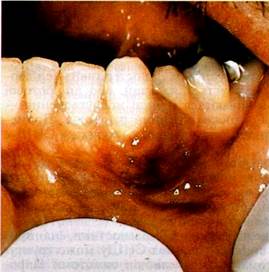
прояви СНІДу в порожнині рота характеризуються сталим перебігом і лікування їх малоефективне
Зазначені ВІЛ-індикаторні опортуністичні інфекції вважають маркерами певних стадій СНІДу Так, Candida albicans виявляють у більшості хворих у стадії лімфаденопатії і в розпал захво рювання
В осіб групи ризику інфекцію Candida albicans можна розглядати як початковий симптом СНІДу.
Поєднання в порожнині рота кандидозу та інфекційного процесу, спричиненого різними вірусами, свідчить про некомпетентність імунної реакції епітелію CO рота і розцінюється як початковий прояв захворювання на СНІД.
Судинна пухлина — саркома Капоші — трансмісивне захворювання, що характеризується багатьма пігментованими ураженнями. Вперше описана 1872 p. угорським дерматологом M.Kaposi як специфічне захворювання.
У хворих на СНІД виявляється в основному в порожнині рота (в 76% випадків) на піднебінні і характеризується екзо-фітним ростом, безболісністю, пухкою консистенцією (у вигляді м'якого синюшного вузлика), великою частотою ма-лігнізації. М'які тканини мають забарвлення від бурого до синювато-червоного (мал.60).
Гістологічна характеристика: у ранній період виявляють атиповий судинний конгломерат з проліферацією через клітини ендотелію та скупченням еритроцитів уздовж судин, у пізніший період — вузли, що складаються в основному із склеєних веретеноподібних клітин.
Лімфома Беркітта локалізується на нижній щелепі. Перед її утворенням хворі скаржаться на зубний біль, виразкування CO, збільшення підщелепних лімфатичних вузлів. При рентгенологічному дослідженні в цей період виявляють резорбцію кісткової тканини.
В осіб, що зловживають курінням, спостерігають епідер-моїдну карциному, яка локалізується на язиці або дні ротової порожнини. При СНІД розвиваються й інші новоутворення — лімфоретикулярна саркома, плоскоклітинний рак тощо. Променева і хіміотерапія зазначених новоутворень у хворих на СНІД є неефективними.
Діагностика. Рання діагностика СНІДу вкрай важлива, оскільки латентний період між інфікуванням і появою клінічних ознак СНІДу може бути досить тривалим. Ось чому стоматологи мають бути поінформовані про клінічну картину захворювання і шляхи передачі цієї небезпечної інфекції.
Враховуючи складність лабораторної діагностики, на пропозицію ВООЗ, у деяких випадках діагноз СНІДу може грунтуватися на клінічній симптоматиці. Всі клінічні симптоми запропоновано поділяти на дві групи: серйозні та незначні (ВООЗ, 1986).
У дорослих СНІД діагностують за наявності щонайменше двох серйозних симптомів у поєднанні з хоча б одним незначним симптомом за відсутності відомих причин імуносупресії, таких як рак, тяжка форма недостатності харчування або інші стани встановленої етіології.
1. Серйозні симптоми:
а) зниження маси тіла на 10% і більше;
6) хронічна діарея тривалістю понад 1 міс;
в) гарячка тривалістю більше ніж 1 міс (перемінна або постійна).
2. Незначні симптоми:
а) сталий кашель тривалістю понад 1 міс;
б) генералізований багатовогнищевий дерматит;
в) рецидивний оперізувальний герпес;
г) кандидоз порожнини рота і глотки;
д) хронічний прогресуючий і дисемінований простий герпес;
е) генералізована лімфаденопатія.
За наявності однієї лише саркоми Капоші або криптококового менінгіту встановлюють діагноз СНІДу.
Особливості діагностики СНІДу у дітей. Підозра на СНІД виникає, коли у дитини спостерігаються щонайменше два серйозних симптоми у поєднанні з не менш ніж двома незначними симптомами за відсутності відомих причин імуносупресії, таких як рак, тяжка форма недостатності харчування або інші стани установленої етіології.
1. Серйозні симптоми:
а) втрата маси тіла або затримка росту;
б) хронічна діарея тривалістю понад 1 міс;
в) гарячка тривалістю понад 1 міс.
2. Незначні симптоми:
а) генералізована лімфаденопатія;
б) кандидоз порожнини рота і глотки;
в) звичайні рецидивні інфекції (отит, фарингіт тощо);
г) тривкий кашель;
д) генералізований дерматит;
е) підтверджена інфекція СНІД у матері.
Показаннями до обстеження на СНІД є:
І. Злоякісні новоутворення (саркома Капоші, лімфома). II. Інфекції:
11.1. Гриби: а) кандидоз, який спричинює ураження СОПР та порушення функції стравоходу; б) криптококоз, що зумовлює захворювання легень, ЦНС і розсіяну інфекцію.
11.2. Бактеріальні інфекції («атиповий» мікобактерюз, викликаний видами, відмінними від збудників туберкульозу і лепри).
[1.3. Вірусні інфекції: а) цитомегаловірус, який зумовлює захворювання легень, травного каналу, ЦНС; б) вірус герпесу, що викликає хронічну інфекцію CO з виразками, підвищення температури тіла протягом 1 міс і більше; в) прогресуюча енцефалопатія, що викликана, як вважають, паповавірусом; г) віруси HTIV, які спричинюють злоякісні переродження Т-клітин.
11.4. Найпростіші і гельмінти: а) пневмонія, що викликана Pneumocystis carini; б) токсоплазмоз, який зумовлює пневмонію чи ураження ЦНС; в) криптоспоридюз, кишкова форма з діареєю тривалістю понад 1 міс; г) стронгілоідоз
З метою доведення наявності вірусу в організмі застосовують З методи: культивації вірусу, ідентифікації вірусних AT, виявлення титру AT до вірусних АГ (тест ELISA — enzime linked immunosorbent assay). Останній метод економічно більш вигідний, але дає багато хибнопозитивних результатів і потребує у випадках позитивних реакцій контролю за допомогою методу Western—Blot, що грунтується на використанні імунофорезу.
Стоматологічні аспекти профілактики СНІДу. З огляду на особливості клінічного перебігу СНІДу стоматолог може бути першим лікарем, що запідозрив це захворювання. Більше того, лікар-стоматолог повинен займати активну позицію у виявленні ВІЛ-інфікованих і хворих, а для цього йому необхідно бути добре обізнаним з ознаками захворювання, уважно аналізувати історію хвороби, проводити пальпацію лімфовузлів голови. Хоч в слині інфікованих та хворих на СНІД ВІЛ знаходиться в незначній кількості, стоматолог повинен усвідомлювати, що він (як і інші фахівці, що контактують з рідинами організму хворих на СНІД) входить до групи професійного ризику.
Для стоматологів існує ризик зараження ВІЛ при випадкових укусах хворими на СНІД чи носіями вірусу, потраплянні їхньої слини на ушкоджену шкіру чи CO лікаря, при пораненні інструментарієм, який застосовувався при лікуванні хворих. Крім цього, застосування турбінної бормашини може стати причиною госпітальної інфекції, такої як СНІД та гепатит В.
Зважаючи на можливість контакту лікарів-стоматологів із хворими на СНІД чи вірусоносіями, їм рекомендують такі застережні заходи:
— одержання інформації про можливі фактори ризику у хворого;
— антисептичне оброблення шкіри рук і робота в гумових рукавичках;
— застосування (по можливості) інструментів, матеріалів та голок разового використання;
— бездоганна стерилізація і дезінфекція матеріалів, що використовуються повторно.
Спеціалісти свідчать, що адекватні засоби профілактики дають можливість уникнути інфікованості ВІЛ навіть у разі роботи з групою ризику. Тому особистий захист має здійснювати увесь медичний персонал (застосування гумових рукавичок, спеціальних окулярів, пластикових масок, спецхалатів та шапочок).
Необхідно уникати незначних поранень інструментами, що контактували з кров'ю та слиною хворого. Для значного змен-
шення утворення аерозолів не рекомендовано користуватись турбінною бормашиною, краще застосовувати наконечники з меншою кількістю обертів. Значно зменшує аерозольне забруднення повітря робочої зони застосування кофердаму.
Рукавички і маски бажано змінювати після приймання кожного хворого, у крайньому разі — щогодини. Руки слід мити під струменем води після обстеження чи лікування кожного хворого і обробляти 4% розчином хлоргексидину. Халати повинні мати якомога менше швів і наглухо закривати груди. Бажано використовувати разові халати із синтетичної тканини.
Стерилізація інструментарію. ВІЛ швидко інактивується при застосуванні сухої і вологої стерилізації. Стоматологічний інструментарій багаторазового використання (у тому числі відтискні ложки) попередньо замочують у розчині гіпохлориту натрію, а потім піддають холодному оброблянню розчином глютаральдегіду або стерилізують в автоклаві з оксидом етилену. Перед направленням відтисків у лабораторію їх треба помістити на 15 хв у розчин глютаральдегіду чи гіпохлориту натрію.
Запропонований такий склад розчинів: 40% етиловий спирт, 1% лізол, 5% фенол, 2% формалін, 200 ммоль гіпохлориту натрію. Для дезінфекції: 1% розчин глютаральдегіду, 25% розчин етилового спирту з пропіонлактоном у співвідношенні 1:400, 0,2% розчин гіпохлориту натрію з 0,35% розчином формаліну. Термін обробляння — 5 хв. Обробляння інструментів проводять у рукавичках.
При температурі 56 °С вірус інактивується протягом ЗО хв. Необхідне ретельне дотримання умов, що гарантують повну інактивацію вірусу. Поліпшує передстерилізаційну підготовку застосування апарата ультразвукового очищення «Серьга». Для забезпечення повного контролю за додержанням стандарту на температуру і час стерилізації (180 °С протягом 60 хв), враховуючи вимоги ДСТ України 1992 p., фірма «Довіра» випускає термочасовий індикатор стерилізації, який являє собою паперову смужку розміром 10 х 40 мм з нанесеним на неї індикаторним шаром. Її вкладають у пакет разом з інструментами і вносять у стерилізатор. У разі дотримання режиму стерилізації колір індикаторного шару стійко змінюється і збігається з еталонним. Біоптати та інший операційний матеріал необхідно вміщувати в подвійні захисні бікси, а транспортувати в спеціальних контейнерах.
Лікування. Для боротьби зі СНІДом створюються нові підходи. Вони грунтуються на фундаментальних розробках, пов'язаних із концепціями, які з'явилися нещодавно і швидко розвиваються, а також на нових технологіях (внутрішньоклітинного імунітету, генної терапії). Ці технології щодо СНІДу розробляють у трьох напрямах. Перший напрям полягає у введенні гена, що синтезує продукт, який потім виділяється з
клітини. Так, при введенні гена, що синтезує фрагмент рецепторного білка СД-4, продукт виходить з клітин і захищає сусідні клітини від ВІЛ-інфікування.
Другий напрям пов'язаний із синтезом пептидів. Вони не виходять за межі клітини і конкурентне блокують ключові для розвитку ВІЛ процеси. Так, мутантні білки (або їх фрагменти) — аналоги продуктів регуляторних генів rev і tat — блокують дію останніх, пригнічуючи розвиток ВІЛ. Пептид зі зміненими сай-тами, що є в зоні, яка прилягає до послідовності, розпізнається й розщеплюється вузькоспецифічною вірусною протеазою, пригнічує пресинг білків, що кодуються генами gag і рої.
Третій напрям грунтується на введенні в клітини генів, що кодують антисенси і рибозими, які відповідно блокують або руйнують вірусну РНК.
Серед робіт із різнобічного вивчення СНІДу, які нині виконуються, найцікавіші результати отримані в галузі створення засобів профілактики та лікування СНІДу, а також лікування супутніх хвороб. Це одна з найважливіших стратегічних проблем. Вона також має велике потенційне значення для пошуку засобів лікування й інших хвороб. Роботи розпочато в двох напрямах. Перший напрям — розроблення принципово нових технологій лікування та профілактики, що грунтуються на нещодавно сформованій концепції про внутрішньоклітинний імунітет. Другий напрям пов'язаний з хімічним та біотехно-логічним синтезом нових лікарських засобів. Серед препаратів, що вже використовують у світовій практиці для боротьби зі СНІДом, найпоширенішим є азидотимідин. В Україні розробляється новий спосіб його синтезу. Переданий на клінічні випробовування для лікування СНІД-асоційованих інфекцій ре-комбінантний інтерферон о^ людини. Його перше застосування для лікування хворих на саркому Капоші дало змогу значно знизити кількість цитостатичних засобів, що їх звичайно призначають цим хворим, і при цьому різко підвищити терапевтичний ефект.
Серед лікарських засобів, що наявні в арсеналі препаратів для лікування цього контингенту хворих, крім азидотимідину широко застосовують сурамін, НРА-23, ацикловір, коректори імунітету (інтерлейкін-2, гамма-глобулін, стимулятор функції Т-лімфоцитів ізопринозин). З метою підтримання імунного статусу проводять пересаджування кісткового мозку. Для стоматолога при лікуванні таких хворих основним є надання їм симптоматичної лікувальної допомоги та санація ротової порожнини.
Прогноз. Для прогнозу СНІДу важливе значення має виявлення рівня Т-хелперних лімфоцитів і співвідношення T4/Tg. Якщо рівень Ї4 менший ніж 200 в 1 мм3 крові, то в перший рік після прояву клінічних симптомів СНІДу смертність перевищує 50%. Спонтанна ремісія не описана. Хвороба невпинно прогресує і завершується летально.
 2015-09-06
2015-09-06 1478
1478








