Критичні значення об’єму, температури та тиску можна пов’язати з параметрами 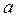 та
та 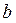 , що входять до рівняння Ван-дер-Ваальса:
, що входять до рівняння Ван-дер-Ваальса:
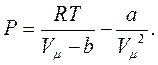 |
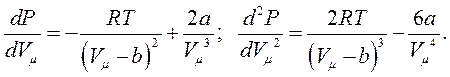 Диференціюючи це рівняння по об’ємі, отримаємо:
Диференціюючи це рівняння по об’ємі, отримаємо:
В критичному стані, тобто при 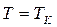 ,
, 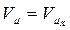 ,
, 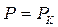 останні два рівняння мають перетворюватися на нуль, тобто:
останні два рівняння мають перетворюватися на нуль, тобто:
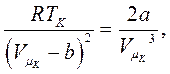 (8.13)
(8.13)
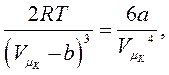 |
(8.14)
а рівняння Ван-дер-Ваальса матиме вигляд:
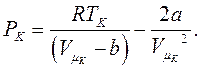 |
(8.15)
На підставі рівнянь (8.13) – (8.15) після незначних перетворень отримаємо, що:
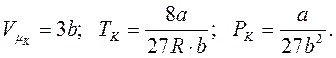 (8.16)
(8.16)
На підставі рівняння (8.16) знаходимо, що:
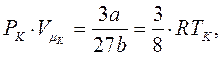 (8.17)
(8.17)
тоді як для ідеального газу було б:
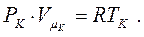 (8.18)
(8.18)
Введемо так звані зведені параметри:
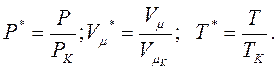 |
(8.19)
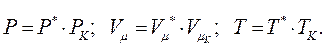 |
Тоді
(8.20)
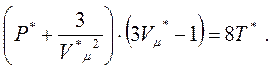 На підставі рівняння (8.10) та системи (8.20) запишемо рівняння Ван-дер-Ваальса для одного моля газу:
На підставі рівняння (8.10) та системи (8.20) запишемо рівняння Ван-дер-Ваальса для одного моля газу:
(8.21)
У рівняння (8.21) не входять параметри 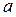 та
та 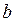 , тобто у критичному стані рівняння є однаковим для всіх речовин, незалежно від їх природи. Це положення називають законом відповідних станів.
, тобто у критичному стані рівняння є однаковим для всіх речовин, незалежно від їх природи. Це положення називають законом відповідних станів.
При температурі, вищій за критичну, речовина перебуває лише в газоподібному стані, а при меншій за критичну – може бути перетвореною на рідину. Це довів у 1860 році Д.І. Мендєлєєв.
 2015-09-06
2015-09-06 400
400








