Внутрішня енергія 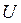 реального газу складається з кінетичної енергії
реального газу складається з кінетичної енергії 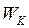 теплового руху молекул та потенціальної енергії
теплового руху молекул та потенціальної енергії 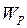 взаємодії між молекулами.
взаємодії між молекулами.
Кінетична енергія теплового руху молекул є не що інше, як внутрішня енергія ідеального газу. Згідно з теорією ідеального газу (див. § 6.6) її можна визначити за співвідношенням:
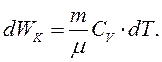 (8.22)
(8.22)
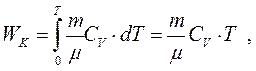 Приймаючи, що при
Приймаючи, що при 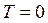 кінетична енергія
кінетична енергія 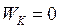 , знаходимо:
, знаходимо:
(8.23)
де 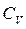 – молярна теплоємність газу при сталому об’ємі.
– молярна теплоємність газу при сталому об’ємі.
Потенціальну енергію взаємодії між молекулами знайдемо на підставі таких міркувань. Для того, щоб розширити газ, необхідно виконати роботу проти сил притягання між молекулами. Ця робота витрачається на зміну потенціальної енергії системи, а величина її визначається співвідношенням:
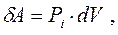 (8.24)
(8.24)
де 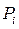 – внутрішній тиск газу.
– внутрішній тиск газу.
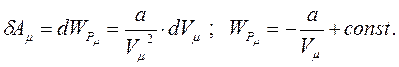 Згідно з моделлю Ван-дер-Ваальса для одного моля
Згідно з моделлю Ван-дер-Ваальса для одного моля 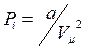 , і тоді:
, і тоді:
(8.25)
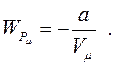 При збільшенні об’єму до нескінченності реальний газ наближається до ідеального (
При збільшенні об’єму до нескінченності реальний газ наближається до ідеального (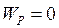 ). Виходячи з цього, приймаємо, що стала інтегрування
). Виходячи з цього, приймаємо, що стала інтегрування 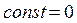 . Тоді потенціальна енергія одного моля реального газу:
. Тоді потенціальна енергія одного моля реального газу:
(8.26)
Таким чином, внутрішня енергія одного моля реального газу дорівнює:
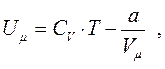 |
(8.27)
а внутрішня енергія довільної маси 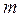 реального газу:
реального газу:
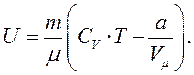 |
(8.28)
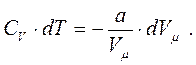 При адіабатній зміні об’єму газу без виконання ним роботи проти зовнішніх сил, внутрішня енергія газу, згідно з першим законом термодинаміки (2.13), має залишатись незмінною. На підставі рівняння (8.27) знаходимо, що:
При адіабатній зміні об’єму газу без виконання ним роботи проти зовнішніх сил, внутрішня енергія газу, згідно з першим законом термодинаміки (2.13), має залишатись незмінною. На підставі рівняння (8.27) знаходимо, що:
(8.29)
Отже, при адіабатному розширенні газу без виконання ним роботи проти зовнішніх сил температура газу мусить зменшуватися, а при стисканні – збільшуватися. Це явище використовують в техніці зрідження газів та досягнення низьких температур.
 2015-09-06
2015-09-06 1292
1292