В однокомпонентных системах фазы состоят из одного вещества (компонента) в различных агрегатных состояниях. Согласно правилу фаз Гиббса при К = 1 и n = 2 (р, Т) число степеней свободы составит:
С = 1 ─ Ф + 2 = 3 ─ Ф. (3.4)
Таким образом, число равновесных фаз в однокомпонентной системе не может быть больше трёх, то есть могут существовать системы: однофазные, двухфазные и трёхфазные.
Диаграмма, выражающая зависимость состояния системы и фазовых равновесий в ней от внешних условий или от её состава, называется диаграммой состояния или фазовой диаграммой. Диаграммы состояния однокомпонентных систем представляют в координатах р = f(T) или T = f(p).
На рис.3.1 и рис.3.2 приведены фазовые диаграммы состояния различных однокомпонентных систем.
Кривые разбивают диаграмму на поля, каждое из которых отвечает одному агрегатному состоянию вещества: твердое, жидкое и газообразное. Сами кривые отвечают равновесию между соответствующими двумя фазами.
Кривая ОС характеризует зависимость давления насыщенного пара над жидкостью и называется кривой испарения; кривая ОВ ─ зависимость температуры плавления твердого вещества от внешнего давления и называется кривой плавления; кривая ОА ─ зависимость давления насыщенного пара над твердым веществом от температуры и называется кривой возгонки; кривая OD определяет давление насыщенного пара над переохлажденной водой (метастабильное состояние). Эти же кривые характеризуют и обратные равновесные соответствующие процессы: конденсации, кристаллизации и сублимации.
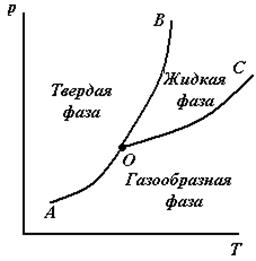 | 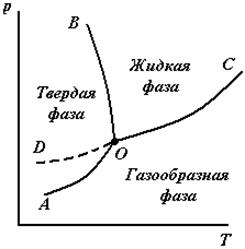 |
| Рис.3.1. Диаграмма состояния однокомпонентной системы. | Рис.3.2. Диаграмма состояния воды. |
 2015-10-13
2015-10-13 2933
2933
