1. Что называют гальваническими элементами?
2. Что называют анодом в электрохимии?
3. Что называют катодом в электрохимии?
4. Как возникает в гальваническом элементе напряжение между катодом и анодом?
5. Чему равен потенциал стандартного водородного электрода?
6. Относительно какого электрода определяют стандартные окислительно-восстановительные потенциалы?
7. Потенциал анодом в гальваническом элементе (больше, меньше, равен) потенциала катода?
8. Каким уравнением или законом описывается зависимость величины потенциала металлического электрода от концентрации его ионов в растворе?
9. Сравните электродный потенциал никеля в растворе его соли с концентрацией 0,001 моль/л с его стандартным электродным потенциалом.
10. Как изменяется потенциал металлического электрода с уменьшением концентрации ионов металла в растворе?
11. Как изменяется с увеличением рН раствора потенциал водородного электрода?
12. Чему равен потенциал водородного электрода при рН раствора, равном 8?
13. Как изменится потенциал электрода Fe / Fe2+ при пропускании через раствор сероводорода?
14. Как изменится потенциал стандартного никелевого электрода при разбавлении раствора, в который он погружен, в пять раз?
15. Как изменится потенциал стандартного алюминиевого электрода при замене электролита на 0,05 молярный раствор?
16. При какой концентрации ионов Fe2+ потенциал железного электрода равен -0,5 В?
17. Чему равен электродный потенциал цинка в 0,0016 М растворе Zn(NO3)2?
18. Потенциал водородного электрода равен - 0,452 В. Чему равен рН раствора, в который он погружен?
19. Степень диссоциации Cu(NO3)2 в 1 М растворе равна 0,83. Чему равен потенциал медного электрода (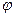 0 = 0,34 В) в этом растворе?
0 = 0,34 В) в этом растворе?
20. Составьте схему кобальт-кадмиевого гальванического элемента
21. Напишите анодный процесс, который протекает при работе гальванического элемента, составленного из стандартных магниевого и титанового электродов
22. Напишите катодный процесс, который протекает при работе гальванического элемента Pt, H2 / HNO3 // ZnSO4 / Zn при стандартных концентрациях электролитов
23. Напишите катодный процесс, который протекает при работе гальванического элемента, составленного из водородного электрода, погруженного в раствор с рН =12, и стандартного оловяного электрода
24. Алюминиевая и серебряная пластины соединены внешним проводником и погружены в раствор соляной кислоты. Составьте анодный и катодный процессы такого гальванического элемента
25. Составьте суммарная реакцию при работе гальванического элемента из стандартных железного и медного электродов
26. Какую реакцию называют токообразующей в гальваническом элементе?
27. Как определить ЭДС гальванического элемента?
28. Как изменится ЭДС гальванического элемента Mg / MgSO4 // FeSO4 / Fe при уменьшении концентрации FeSO4?
29. Как изменится ЭДС гальванического элемента, составленного из водородного и стандартного серебряного электродов при увеличении рН раствора соляной кислоты?
30. Рассчитайте ЭДС гальванического цинк-свинцового элемента при использовании 0,01 молярных растворов
31. Составьте концентрационный никель-никелевый гальванический элемент
32. Как изменится ЭДС кобальт-серебряного гальванического элемента при уменьшении концентрации ионов кобальта и серебра в 3 раза?
33. В каком случае будет работать гальванический элемент, электроды которого сделаны из одного и того же металла?
34. ЭДС гальванического элемента, составленного из никелевого электрода и стандартного железного электрода, погруженного в раствор FeSO4, равна нулю (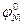 = - 0,25 В,
= - 0,25 В, 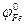 = - 0,44 В). Чему равна концентрация ионов никеля в растворе?
= - 0,44 В). Чему равна концентрация ионов никеля в растворе?
35. Серебряная и никелевая пластины соединены внешним проводником и погружены в раствор соляной кислоты. Какой газ и на какой пластине выделится через некоторое время?
36. Сравните напряжение на клеммах гальванического элемента и ЭДС
 2015-10-14
2015-10-14 774
774







