СОСТАВ, СВОЙСТВА И КЛАССИФИКАЦИИ НЕФТЕЙ
Цель изучения – получить знание о нефти как сложной коллоидной системе, состоящей из углеводородных и неуглеводородных (гетероатомных) компонентов разного фазового состояния, содержащих биологические метки (хемофоссилии) и способной изменять свой состав и свойства вслед за изменением термобарических и геохимических условий.
Задачи – изучить:
ü элементный и компонентный состав;
ü фракционный состав;
ü факторы, влияющие на изменение состава и свойств нефтей.
Уметь:
ü определять физические свойства и товарные качества нефтей по их компонентному составу и содержанию: серы, светлых фракций, содержанию масел, содержанию параина;
ü определять фракционный состав нефтей по пределам температур кипения;
ü определять химический тип нефтей по групповому составу.
Элементный и компонентный состав нефтей
Нефть – это сложная коллоидная гидрофобная система, состоящая из углеводородов различного строения и гетероатомных или неуглеводородных соединений (кислородных, сернистых, азотистых и высокомолекулярных металлорганических смолисто-асфальтеновых соединений), которая распространена в породах осадочного чехла и фундамента осадочных бассейнов. Среди углеводородных и неуглеводородных компонентов нефти содержатся так называемые реликтовые структуры или хемофоссилии, которые по своему составу близки к некоторым биологическим веществам или их фрагментам. Обычно нефть имеет черный или темно-коричневый цвет, иногда, при солнечном свете, зеленовато-желтый оттенок и реже она почти бесцветная.
При химическом анализе нефти определяют её элементный, изотопный, компонентный и фракционный состав.
В нефтях обнаружено свыше 70 элементов таблицы Д.И. Менделеева, которые разделяются на главные и основные элементы, а также на микроэлементы.
Главными химическими элементами нефти являются углерод и водород. Содержание углерода составляет 82-87 %, а водорода 12-14 %. В сумме их содержание составляет 96-99 %.
Основные элементы представлены кислородом, серой и азотом. Их общее содержание составляет от 0,5 до 2 %, но может достигать 8 % и более, главным образом, за счет серы.
Микроэлементы содержатся в количестве от одной десятой до одной десятимиллионной доли процента. В сумме они составляют менее 1 %. Главное место среди микроэлементов занимают металлы - это: ванадий (V), никель (Ni), железо (Fe), цинк (Zn) и другие металлы. Содержатся также и неметаллы - галогены: хлор (Cl), бром (Br), йод (I) и другие элементы-неметаллы: фосфор (P), кремний (Si), мышьяк (Аs). Наибольшим содержанием выделяется: фосфор, до 0,1 %, ванадий (V) - 0,03-0,004 %, никель (Ni) - 0,03-0,05 %, железо (Fe) - 0,012-0,0003 % и цинк (Zn) - 0,0036-0,0004 %. При этом ванадий и никель концентрируются в золе некоторых нефтей в количествах, соизмеримых с их содержанием в промышленных рудах.
В изотопном составе соединений нефтей преобладают легкие изотопы элементов.
В общем, в нефтях определено около 1300 индивидуальных химических соединений, которые разделяются на две группы: углеводородную, состоящую примерно из 900 индивидуальных УВ и неуглеводородную, состоящую примерно из 370 гетероорганических соединений. В обобщённом виде состав нефтей представлен в таблице 2.
Основными компонентами нефти являются углеводороды, которые представлены алкановыми, нафтеновыми, ароматическими и гибридными соединениями. В последнее время в некоторых нефтях обнаружены этиленовые УВ или алкены.
Алкановые УВ, они же метановые, парафиновые, алифатические УВ или алканы (Al) соответствуют общей формуле CnH2n+2, где n – количество атомов углерода, которое может изменяться от одного до нескольких десятков. Их содержание в нефтях составляет от 10 до 70 %.
Химическое строение простейших алканов – метана, этана и пропана – показывают их структурные формулы, из которых видно, что в алканах имеются два типа химических связей: С–С и С–Н. Образование ковалентных связей в алканах за счет общих электронных пар атомов углерода и водорода можно показать с помощью электронных формул:

Пространственное строение зависит от направленности атомных орбиталей (АО). В углеводородах главную роль играет пространственная ориентация атомных орбиталей углерода, поскольку сферическая 1s-АО атома водорода лишена определенной направленности.
Насыщенный атом углерода в алканах связан с четырьмя другими атомами. Каждая из четырех sp3-гибридных АО углерода образует s-связи С-Н или С-С.
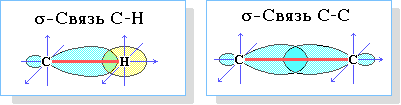
Четыре s-связи углерода направлены в пространстве под углом 109о28', что соответствует наименьшему отталкиванию электронов. Поэтому молекула простейшего представителя алканов – метана СН4 – имеет форму тетраэдра, в центре которого находится атом углерода, а в вершинах – атомы водорода:
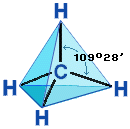
Валентный угол Н-С-Н равен 109о28'. Пространственное строение метана можно показать с помощью объемных (масштабных) и шаростержневых моделей.
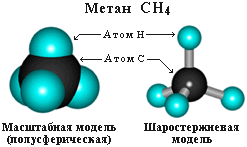 |
Для записи удобно использовать пространственную (стереохимическую) формулу.
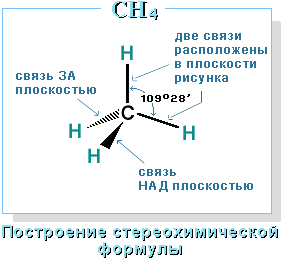
В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3-атома углерода образуют более сложную пространственную конструкцию:
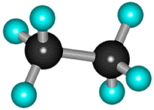
Для молекул алканов, содержащих свыше 2-х атомов углерода, характерны изогнутые формы. Это можно показать на примере н-бутана или н-пентана:
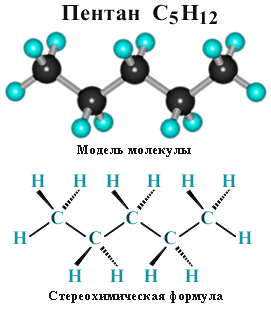
Алканы кроме н-алканов содержат и изо-алканы. При этом среди изо-алканов выделяются изопреноидные алканы, метильные группы СН3, которых имеют регулярное чередование, что видно на примере пристана: (С19Н40):
СН3-СН-СН2-СН2-СН2-СН-СН2-СН2-СН2-СН-СН2-СН2-СН2-СН-СН3.
| | | |
СН3 СН3 СН3 СН3.
Если атом углерода в молекуле связан с четырьмя различными атомами или атомными группами, то возможно существование двух соединений с одинаковой структурной формулой, но отличающихся пространственным строением. Молекулы таких соединений относятся друг к другу как предмет и его зеркальное изображение и являются оптическими изомерами или оптическими антиподами:
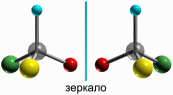
Молекулы оптических изомеров несовместимы в пространстве (как левая и правая руки), в них отсутствует плоскость симметрии. Таким образом, оптическими изомерами называются пространственные изомеры, молекулы которых относятся между собой как предмет и несовместимое с ним зеркальное изображение. Оптические изомеры имеют одинаковые физические и химические свойства, но различаются отношением к поляризованному свету. Такие изомеры обладают оптической активностью (один из них вращает плоскость поляризованного света влево, а другой - на такой же угол вправо). Различия в химических свойствах наблюдаются только в реакциях с оптически активными реагентами. Оптическая изомерия проявляется в органических веществах различных классов и играет очень важную роль в химии природных соединений.
Алканы, содержащие от одного до четырех атомов углерода (С1-С4), при нормальных условиях являются газами, от пяти до 15 (С5-С15) – жидкостями, больше 16 (С16) - твердыми веществами. При этом твердые алканы от С16-С32 называются парафинами, а от С32 и выше церезинами.
Таблица 2. Состав нефти (В.В. Доценко; 2007)
| Элементный состав | |||||
| Главные элементы: С – 82-87 %, Н – 12-14 % | Основные гетероэлементы: S – до 6-8 %, О – до 3,6 %, N - до 1,7 % S+О+N – от 0,5-2 до 8 и более % | Микро- гетероэлементы: Металлы: V, Ni, Fe, Zn, Mо, Co, W, Hg, U, и др. Галогены: Cl, Br, I Неметаллы: Р, Si, Аs Всего более 70 элементов, с содержанием от 10-1 до 10-7 % | |||
| Компонентный (групповой) состав (около 1300 химических соединений) | |||||
| Углеводородные (УВ) компоненты (более 900 химических соединений): алканы – от 10 до 70 %, цикланы – от 25 до 80 %, арены – от 10 до 25 %, иногда до 50 %, гибридные УВ – от 20 до 50 %, алкены (олефины) – иногда до 8-10 % | Неуглеводородные компоненты (около 370 химических соединений): сернистые соединения (более 250), кислородные соединения (более 70), азотистые соединения (более 50), смолы, асфальтены | ||||
| Реликтовые соединения (хемофоссилии) | |||||
| Углеводородные структуры: нормальные и изопреноидные алканы; полициклические изопреноидные УВ (стераны, терпаны, гопаны) | Неуглеводородные структуры: металлопорфирины | ||||
| Фракционный состав | |||||
| Легкие светлые фракции УВ (температура кипения (т.к.) 35-350 °С): бензин – УВ С5-С10 (т.к.35-200 °С), керосин – УВ С11-С13 (т.к.200-250 °С), газойль – УВ С14-С21 (т.к.250-350 °С) | Тяжелые темные фракции или мазут (температура кипения (т.к.) 350-600 °С): масла соляровые - УВ С22-С25, масла смазочные - УВ С26-С35, гудрон или нефтяной пек - смолы, асфальтены и УВ С36-С60 и более | Остаток после термической обработки гудрона: технический битум, кокс | |||
Алканы обладают сильным токсическим и наркотическим действием, особенно нормальные алканы с короткой углеродной цепью.
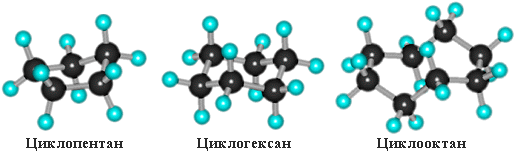
Нафтеновые УВ, они же циклановые, циклоалкановые, циклопарафиновые, полиметиленовые УВ или нафтены (Nf) состоят из замкнутых в цикл метиленовых групп СН2.
Атомы углерода в циклоалканах, как и в алканах, находятся в sp3–гибридизованном состоянии и все их валентности полностью насыщены.
Простейший циклоалкан – циклопpопан С3Н6 – представляет собой плоский трехчленный карбоцикл:
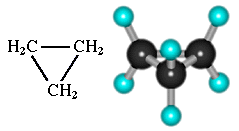
Остальные циклы имеют неплоское строение вследствие стремления атомов углерода к образованию тетраэдрических валентных углов.
По правилам международной номенклатуры в циклоалканах главной считается цепь углеродных атомов, образующих цикл. Название строится по названию этой замкнутой цепи с добавлением приставки "цикло" (циклопропан, циклобутан, циклопентан, циклогексан и т.д.). При наличии в цикле заместителей нумерацию атомов углерода в кольце проводят так, чтобы ответвления получили возможно меньшие номера. Так, соединение
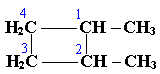
следует назвать 1,2-диметилциклобутан, а не 2,3-диметилциклобутан, или 3,4-диметилциклобутан.
Молекулы циклоалканов содержат на два атома водорода меньше, чем соответствующие алканы. Напpимеp, бутан имеет фоpмулу С4Н10, а циклобутан – С4Н8. Поэтому общая формула циклоалканов СnH2n. Структурные формулы циклоалканов обычно изображаются сокращенно в виде правильных многоугольников с числом углов, соответствующих числу атомов углерода в цикле.
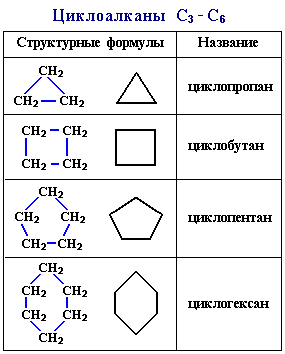
Нафтены имеют моноциклическое би-, три- и полициклическое строение. В моноциклической молекуле может быть от трех до шести метиленовых групп.

Общая формула моноциклических нафтенов имеет вид: CnH2n, а би- и трициклических структур: CnH2n-2 и CnH2n-4 соответственно.
Нафтены, кроме моноциклических могут иметь неконденсированное и конденсированное строение. В неконденсированных структурах нафтеновые циклы отделены (изолированы) друг от друга метиленовыми группами (СН2), которых может быть несколько. Смежные структуры конденсированных нафтенов содержат два общих атома углерода и состоят из различных комбинаций пяти- и шестичленных циклов, которые часто содержат также ароматические кольца и алкильные цепи. Нафтены С3-С4 являются газами, С5-С7 жидкостями, С8 и выше – твердыми веществами.
Содержание нафтенов в нефтях колеблется в широких пределах, от 25 до 80 %. Среди соединений нефти нафтены наименее токсичны и даже обладают стимулирующим действием на живые организмы.
- Ароматические УВ или арены (Аr) – это класс УВ, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Простейшие представители (одноядерные арены):
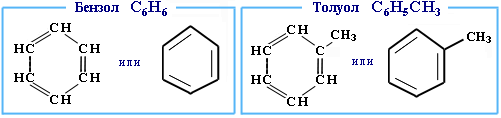
Многоядерные арены: нафталин С10Н8, антрацен С14Н10 и др.
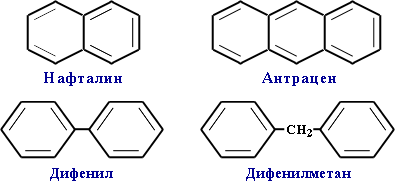
Термин "ароматические соединения" возник давно в связи с тем, что некоторые представители этого ряда веществ имеют приятный запах. Однако в настоящее время в понятие "ароматичность" вкладывается совершенно иной смысл.
Ароматичность молекулы означает ее повышенную устойчивость, обусловленную делокализацией p-электронов в циклической системе.
Бензол С6Н6 – родоначальник ароматических углеводородов.
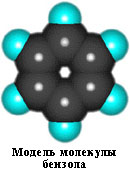 Каждый из шести атомов углерода в его молекуле связан с двумя соседними атомами углерода и атомом водорода тремя s-связями. Валентные углы между каждой парой s-связей равны 120°. Таким образом, скелет s-связей представляет собой правильный шестиугольник, в котором все атомы углерода и все s-связи С-С и С-Н лежат в одной плоскости:
Каждый из шести атомов углерода в его молекуле связан с двумя соседними атомами углерода и атомом водорода тремя s-связями. Валентные углы между каждой парой s-связей равны 120°. Таким образом, скелет s-связей представляет собой правильный шестиугольник, в котором все атомы углерода и все s-связи С-С и С-Н лежат в одной плоскости:
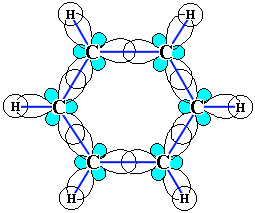
р-Электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2р-АО, расположенных перпендикулярно плоскости s-скелета бензольного кольца. Они образуют единое циклическое p-электронное облако, сосредоточенное над и под плоскостью кольца.
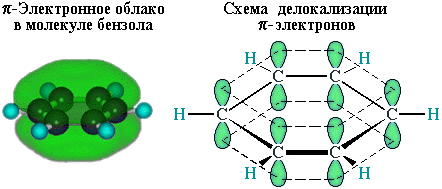
Все связи С-С в бензоле равноценны, их длина равна 0,140 нм, что соответствует промежуточному значению между длиной простой связи (0,154 нм) и двойной (0,134 нм). Это означает, что в молекуле бензола между углеродными атомами нет чисто простых и двойных связей (как в формуле, предложенной в 1865 г. немецким химиком Ф.Кекуле), а все они выровнены (делокализованы). Поэтому структурную формулу бензола изображают в виде правильного шестиугольника (s-скелет) и кружка внутри него, обозначающего делокализованные p-связи:
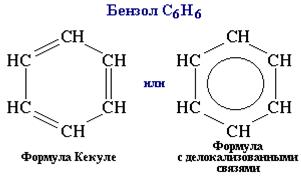
Формула Кекуле также нередко используется, но при этом учитывается, что она лишь условно передает строение молекулы.
Арены моноциклические, би-, три- и полициклические представлены на рисунке (рис. 3).
Арены, по сравнению с алканами и нафтенами содержатся в нефти, как правило, в меньших количествах, в основном от 10 до 25 %. Иногда их содержание достигает 50 %. Ароматические УВ являются наиболее токсическими компонентами нефтей. Например, при концентрации в воде всего 1% они убивают все водные растения.
Гибридные УВ. В молекулах УВ гибридного (смешанного) строения находятся различные структурные элементы: ароматические кольца, нафтеновые циклы и алкильные цепи (см. рис. 3). Сочетание этих структурных элементов может быть самым разнообразным. Гибридное строение в нефтях имеет от 20 до 50 % высокомолекулярных УВ.
Этиленовые УВ или алкены, олефины. Это - непредельные (ненасыщенные) УВ с открытой цепью, в молекулах которых между углеродными атомами имеется одна двойная связь. Как и предельные УВ, алкены образуют свой гомологический ряд с общей формулой CnH2n. Простейшим представителем этого ряда и его родоначальником является этилен С2Н4 (Н2С=СН2).
Алкены обнаружены во многих образцах нефтей только в конце ХХ века в количестве до 8-10 %. Образуются они в результате радиолитического дегидрирования алканов при воздействии естественного радиоактивного излучения в недрах.
Неуглеводородные компоненты нефти являются производными углеводородов и разделяются на две группы.
 В первую группу входят гетероорганические соединения, которые описываются точной химической формулой. Называются они по содержащемуся или преобладающему в них гетероатому и представлены сернистыми, кислородными и азотистыми соединениями.
В первую группу входят гетероорганические соединения, которые описываются точной химической формулой. Называются они по содержащемуся или преобладающему в них гетероатому и представлены сернистыми, кислородными и азотистыми соединениями.
Во вторую группу веществ входят высокомолекулярные соединения, структура которых сложна, и поэтому определяется неоднозначно. Эта группа представлена смолами и асфальтенами или смолисто-асфальтеновыми веществами (САВ).
Смолы и асфальтены - это высокомолекулярные конденсированные циклические структуры, которые содержат гетероатомы и боковые алкильные цепи, состоящие из одновалентных радикалов: метила (СН3), этила (С2Н5), пропила (С3Н7) и других.
Смолы имеют молекулярную массу от 500 до 2000 единиц и обладают хорошей растворимостью в органических растворителях и УВ.
Асфальтены – это продукты конденсации нескольких молекул смол, поэтому они являются твердыми веществами с кристаллоподобной структурой и не растворяются в алканах. Их молекулярная масса лежит в пределах от 1000-5000 до 10000 единиц. Однако имеются сведения, что она может доходить до сотен тысяч и даже миллионов единиц.
Сернистые соединения. В нефтях содержится более 250 индивидуальных органических и неорганических соединений, содержащих серу. Неорганические соединения представлены элементной серой – S и сероводородом - H2S. Основное количество серы, от 70 до 90 %, связано со смолами и асфальтенами.
Пределы изменения концентраций серы в элементном составе нефтей очень широки: от сотых долей процента до 6-8 %, и более.
Сернистые компоненты нефтей разделяются на агрессивные и неагрессивные соединения. Присутствие агрессивных соединений весьма нежелательно, так как они активно корродируют металлы, являются сильнейшими каталитическими ядами, экологически опасны и придают нефти неприятный запах. Например, нефть Ишимбайского месторождения, содержащая 3,4 % серы, вызывает коррозию нефтепромыслового и нефтезаводского оборудования, выполненного из углеродистой стали, со скоростью 6,88 мм в год. Агрессивная сера представлена органическими и неорганическими соединениями, которые обладают кислотными свойствами. К ним относятся: элементная сера - S, сероводород - H2S, и меркаптаны - тиолы и тиофенолы.
К неагрессивным сернистым соединениям относятся сульфиды, дисульфиды, тиофан, тиофен и тиопиран – С5Н10S.
Кислородные компоненты нефтей представлены 70 индивидуальными соединениями кислого и нейтрального характера, которые содержат кислород в виде различных функциональных групп: гидроксила (-ОН), карбоксила (-СООН), карбонила (>СО), метоксила (ОСН3), оксигрупы (=О), пероксигруппы (-О-О-) и других. Кислород содержится в нефти в элементном составе в количестве от 0,05 до 3,6 %, что соответствует примерно от 0,5 до 36 % кислородных соединений.
Соединения кислого характера представлены кислотами и фенолами. Кислоты имеют различное строение: алифатическое (Аl-СООН), нафтеновое (Nf-СООН или Nf-(СН2)n-СООН), в том числе и стероидное строение, а также ароматическое и гибридное строение.
Кроме фенола С6Н5ОН в нефтях присутствуют его гомологи, содержащие до шести конденсированных колец.
Кислородные соединения нейтрального характера представлены спиртами, алифатическими и циклическими кетонами и пероксидами.
Азотистые компоненты нефтей составляют более 50 индивидуальных соединений, которые разделяются на три группы.
Первая группа - это азотистые основания, которые реагируют с кислотами, образуя органические соли, поэтому сравнительно легко выделяются из нефти. Представлены они ароматическими гетероциклами: пиридином (С5Н5N), анилином (С6Н5NН2), хинолином (С9Н7N), акридиномом (С13Н9N) и их гомологами.
Вторая группа - это нейтральные соединения, которые представлены ароматическими гетероциклами: пирролом (С4Н4NН), индолом (С8Н6NН), карбазолом (С12Н8NН) бензокарбазолом (С16Н10NН), а также их гомологами и производными.
Третья группа - это порфирины, которые представляют собой сложные циклические металлоорганические азотсодержащие соединения.
Содержание азотистых соединений в нефти обычно не превышает нескольких процентов от её состава, а концентрация азота в элементном составе нефти находится в пределах от 0,01 до 1,7 %.
Реликтовые соединения или хемофоссилии. Эти соединения представляют особую группу веществ, которые одновременно присутствуют в углеводородном и в неуглеводородном составе нефтей, а также в ОВ осадочных пород.
 Реликтовые химические соединения по своей структуре близки к некоторым биологическим веществам или их фрагментам: стероидам, терпенам и терпеноидам, порфиринам (хлорофилл, гем крови), аминокислотам и другим. Ниже на рисунках представлены химическая структура ванадилпорфирина, присутствующего в неуглеводородном составе нефтей
Реликтовые химические соединения по своей структуре близки к некоторым биологическим веществам или их фрагментам: стероидам, терпенам и терпеноидам, порфиринам (хлорофилл, гем крови), аминокислотам и другим. Ниже на рисунках представлены химическая структура ванадилпорфирина, присутствующего в неуглеводородном составе нефтей
 и его предшественника – хлорофилла.
и его предшественника – хлорофилла.
Хемофоссилии являются устойчивыми соединениями, поэтому они почти в неизменном виде поступают из химических остатков организмов в осадки, сохраняются при литогенезе и переходят в состав нефтей. В ходе литогенеза в строении этих биологических веществ происходит небольшая перестройка углеродной структуры молекул и потеря функциональных групп. Поэтому хемофоссилии несут информацию об условиях образования и преобразования нефтематеринского ОВ и заключающих их осадков и горных пород.
Из УВ к хемофоссилиям относятся высокомолекулярные нормальные и изопреноидные алканы, а также полициклические нафтены, а из неуглеводородных компонентов нефти - порфирины, амиды кислот.
 2015-10-13
2015-10-13 6199
6199







