В мерный цилиндр отбирают 20 см3 раствора йодида калия (с (KI) = 0.025 моль/дм3). Быстро переносят его в колбу 1, раствор перемешивают и засекают время начала реакции (включают секундомер и не выключают его до конца опыта). Оставляют раствор на 2 минуты, в течение которых его не перемешивают. Затем добавляют 2 ÷ 4 капли раствора крахмала (w(R) = 1 %) и выделившийся йод быстро оттитровывают раствором тиосульфата натрия (с (1/zNa2S2O3) = 0.01 моль/дм3, z =?) до исчезновения синей окраски:
2 Na2S2O3 + I2 = Na2S4O6 + 2 NaI. (81)
Отмечают объем добавленного раствора тиосульфата натрия и ждут появления синей окраски раствора. Фиксируют время окрашивания раствора в светло-синий цвет. Оставляют раствор на 2 минуты, в течение которых не перемешивают.
Через 2 минуты в тот же раствор добавляют вторую порцию раствора тиосульфата натрия до обесцвечивания системы, фиксируют общий объем добавленного раствора тиосульфата натрия и время окрашивания раствора в светло-синий цвет.
Опыт продолжают, пока не добавлено не менее 5 порций раствора тиосульфата натрия.
В момент появления синей окраски количество эквивалентов добавленного тиосульфата натрия равно количеству эквивалентов выделившегося йода:
Следовательно:
с (1/zNa2S2O3) Vi = сi (1/zI2)(V c+ Vi -1), z =? (82)
где с (1/zNa2S2O3) – молярная концентрация эквивалентов тиосульфата натрия в титранте, моль/дм3;
V . i – объем раствора тиосульфата натрия, добавленный к исследуемой системе в момент времени t, см3;
сi (1/zI2) – молярная концентрации эквивалентов йода в исследуемой смеси в момент времени t, моль/дм3;
(V c + Vi -1) – объем исследуемой смеси с учетом предыдущей добавки титранта, см3.
Из закона эквивалентов (82) рассчитывают сi (1/zI2).
Докажите, что для исследуемой системы выполняется равенство:
сi (1/zI2) = сi (Fe2+), моль/дм3. (83)
Результаты измерений и расчетов представляют в таблице 6.2.
Описанные выше процедуры повторяют с растворами в колбах
2 ÷ 4 и заполняют таблицы 6.3 ÷ 6.5, аналогичные таблице 6.2.
Таблица 6.2 – Результаты кинетических измерений для раствора 1:
с (Fe3+) = … моль/дм3; с (I-) = … моль/дм3
| Время измерения | Объем титранта | Объем исследуемой смеси | Молярная концентрация ионов железа (II) | 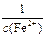 , дм3/моль , дм3/моль | 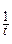 , с-1 , с-1 |
| t, с | V т i, см3 | (V c + Vi -1), см3 | с (Fe2+), моль/дм3 |
2.3 Расчет частного порядка реакции по отношению к Fe3+
Рассчитывают начальную молярную концентрацию ионов железа (III) в четырех исследуемых системах.
Для каждой из систем методом наименьших квадратов оценивают значения коэффициентов a и b зависимости (76):
Результаты расчетов представляют в таблице 6.6.
Таблица 6.6 – Характеристики скорости реакции при различной молярной концентрации ионов железа (III) и постоянной – йодид-ионов
| Номер раствора | Молярная концентрация ионов железа (III) в начальный момент времени, с о(Fe3+), моль/дм3 | lg с о(Fe3+) | b | 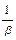 | 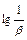 |
Методом наименьших квадратов, используя зависимость (79),
рассчитывают значение частного порядка реакции по отношению к ионам Fe3+: n 1 и S (n 1).
 2015-10-22
2015-10-22 1134
1134








