Для окислительно-восстановительной реакции:
2 Fe3+ + 2 I– → 2 Fe2+ + I2 (68)
предложен механизм:
Fe3+ + 2I- 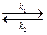 Fe2+ + I2-,
Fe2+ + I2-,
 Fe3+ + I2-
Fe3+ + I2- 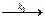 Fe2+ + I2. (69)
Fe2+ + I2. (69)
Методом маршрутов или квазистационарных концентраций выведите уравнения для скорости реакции по её участникам Fe3+, Fe2+ и I2 и запишите полученные выражения для начальной скорости. Укажите теоретические значения частных порядков. Докажите достоверность предложенного механизма реакции, определив экспериментально значения частных порядков дифференциальным методом Вант-Гоффа для начальных скоростей.
Основы м етода Вант-Гоффа
Начальную скорость реакции можно оценить по изменению в течение промежутка времени молярной концентрации продукта реакции – ионов Fe2+:
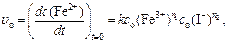 (70)
(70)
где u о – скорость реакции в начальный момент времени, моль/(дм3×с);
c (Fe2+) – молярная концентрация ионов железа (II), моль/дм3;
ki – константа скорости реакции в начальный момент времени, 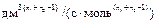 ;
;
c о(Fe3+) – начальная молярная концентрация ионов железа (III), моль/дм3;
c о(I-) – начальная молярная концентрация йодид-ионов, моль/дм3;
n 1 и n 2 – частные порядки реакции по ионам Fe3+ и I-, соответственно.
После логарифмирования уравнения (70) получаем:
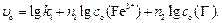 (71)
(71)
Если в серии опытов изменяют начальную концентрацию ионов Fe3+, а I- сохраняют постоянной, то уравнение (71) можно записать:
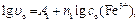 (72)
(72)
где 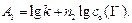 (73)
(73)
Если в серии опытов изменяют начальную концентрацию ионов I-, а Fe3+ сохраняют постоянной, то уравнение (71) можно записать:
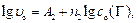 (74)
(74)
где 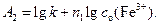 (75)
(75)
Для нахождения скорости реакции в начальный момент времени используют эмпирическое уравнение:
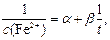 (76)
(76)
где с (Fe2+) – молярная концентрация иона, по которому оценивают скорость реакции, в момент времени t, моль/дм3;
t – время протекания реакции, с;
a и b – коэффициенты линейной зависимости: 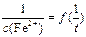 .
.
Из уравнения (76) следует:
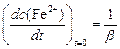 (77)
(77)
Следовательно:
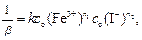 (78)
(78)
при постоянной молярной концентрации йодид-ионов:
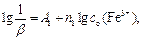 (79)
(79)
при постоянной молярной концентрации ионов железа (III):
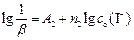 . (80)
. (80)
Выполнение измерений
 2015-10-22
2015-10-22 2632
2632