Процессом называют переход тела из одного состояния в другое. Рассмотренные процессы в газах (изотермический, изобарический, изохорический, адиабатический) характерны тем, что при их осуществлении в окружающих телах никаких изменений не происходит, энергия системы не передается другим телам. Поэтому возможно и осуществление обратного перехода через последовательность тех же промежуточных состояний. Такие процессы называют обратимыми. Обратимые тепловые процессы всегда являются идеализацией в той или иной степени. Они возможны лишь при условии, что изменение параметров состояния происходит очень медленно и сама система каждый раз находится в состоянии равновесия, т.е. когда параметры всюду одинаковы. Лишь при этом возможен обратный процесс, когда система проходит ту же последовательность промежуточных состояний, что и в прямом процессе. Процесс, состоящий из ряда равновесных состояний, называют равновесный. Таким образом, все обратимые процессы - равновесные. Они изображаются графически плавной линией (АВ, рис. 10.1). Рассмотрим работу расширения и сжатия при обратимом и необратимом процессах. При быстром расширении процесс не будет обратимым и изобразится ступенчатой линией АаВ, аналогично при быстром сжатии ВвА. Таким образом, как видно из рис. 10.1,
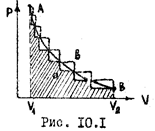
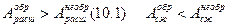
В равновесном состоянии в системе самопроизвольно никакие процессы не возникают. Если же ее вывести из этого состояния, то она в течение некоторого времени будет возвращаться в равновесное состояние. Причем из-за хаотичного движения молекул такой процесс будет необратимым. Таким образом, все самопроизвольные процессы протекают в направлении приближения системы к равновесному состоянию. Количественная формулировка этого положения составляет содержание второго начала термодинамики.
 2015-10-22
2015-10-22 633
633








