| Формула | Систематическое название | Международное название |
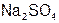 | тетраоксосульфат (VI) натрия (I) | сульфат натрия |
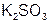 | триоксосульфат (IV) калия (II), | сульфит калия |
 | триоксокарбонат (IV) кальция (II), | карбонат кальция |
 | тетраоксофосфат (V) аммония | фосфат аммония |
 | хлорид фосфония | – |
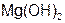 | гидроксид магния (II) | гидроксид магния |
● Кислородсодержащие кислоты
Названия этого класса соединений строятся из группового слова «кислота» и прилагательного, которое составляется из русского корня названия элемента, окончания -ая- и суффиксов, указывающих, насколько степень окисления кислотообразующего элемента отличается от максимальной.
Приставки орто- и мета- применяют, чтобы различать названия кислот, молекулы которых отличаются только «содержанием воды».
 – орто мышьяковистая кислота;
– орто мышьяковистая кислота;  – мета мышьяковистая кислота.
– мета мышьяковистая кислота.
Для высшей или единственной степени окисления применяют суффиксы -н-, -ов-, -ев-:
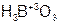 – бор н ая кислота;
– бор н ая кислота; 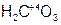 – уголь н ая кислота;
– уголь н ая кислота;
 – кремни ев ая кислота;
– кремни ев ая кислота; 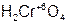 – хром ов ая кислота;
– хром ов ая кислота;
 – азот н ая кислота;
– азот н ая кислота;  – рени ев ая кислота;
– рени ев ая кислота;
 – метафосфор н ая кислота;
– метафосфор н ая кислота;  – ортофосфор н ая кислота.
– ортофосфор н ая кислота.
Если возможны две степени окисления, то для низшей используют суффиксы -ист-, -овист-:
 – селен ист ая кислота;
– селен ист ая кислота;  – теллур ист ая кислота;
– теллур ист ая кислота;
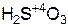 – серн ист ая кислота.
– серн ист ая кислота.
В случае трех возможных степеней окисления кислотообразующего элемента, помимо упомянутых суффиксов, для самой низкой (обычно +1) применяется составной суффикс -новатист-:
 – фосфорн оватист ая кислота;
– фосфорн оватист ая кислота;
 – хлорнов атист ая кислота.
– хлорнов атист ая кислота.
В названиях кислот с четырьмя различными степенями окисления последовательно используют суффиксы -н-, -новат-, -ист- и -новатист-:
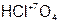 – хлор н ая кислота;
– хлор н ая кислота;  – хлор новат ая кислота;
– хлор новат ая кислота;
 – хлор ист ая кислота;
– хлор ист ая кислота; 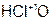 – хлорн оватист ая кислота.
– хлорн оватист ая кислота.
Для того чтобы различить кислоты, содержащие разное количество атомов кислотообразующего элемента в одной степени окисления, применяют числовые приставки:
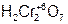 – ди хромовая кислота;
– ди хромовая кислота; 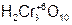 – три хромовая кислота;
– три хромовая кислота;
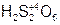 – ди сернистая кислота;
– ди сернистая кислота; 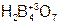 – тетра борная кислота.
– тетра борная кислота.
Систематические названия кислот составляется так, будто кислота – соль водорода: H2SO4 тетраоксосульфат (VI) водорода, H2CO3 триоксокарбонат (IV) водорода. Но для наиболее известных кислот номенклатурные правила допускают применение их тривиальных названий, которые вместе с названиями соответствующих анионов приведены в табл. 12.
Таблица 12
 2015-10-22
2015-10-22 956
956








