Автор: преподаватель, И.П. Кураев, Преподаватель, Московский государственный университет. Тип материала: Учебное пособие
Жизненный цикл медиаторов нервной системы включает следующие «стандарные» стадии: синтез, загрузку в везикулы и транспорт в пресинаптическое окончание; выделение в синаптическую щель; связывание с рецептором на постсинаптической мембране; инактивацию.
Образование медиатора часто происходит непосредственно в пресинаптическом окончании. Это возможно тогда, когда процесс синтеза является химически относительно простым (осуществляется в 1—2 стадии) и не требует каких-либо труднодоступных предшественников. Если эти условия не выполняются, образование медиатора идет в теле нейрона (рис. 3.18). Это наиболее характерно для пептидных медиаторов, возникающих в результате «вырезания» из более крупных белковых молекул.
С синтезом каждого конкретного медиатора связаны специфические ферменты, осуществляющие соответствующие реакции. От их количества и активности в конечном счете зависит активность медиаторной системы. Другой важный фактор — наличие молекул-предшественниц. В этом случае дефицит медиаторов, образуемых из незаменимых веществ (тех, которые можно получить только с едой), может иметь пищевое происхождение.
Синтезированные в теле нейрона молекулы медиатора переносятся сначала в ЭПС, а затем в комплекс Гольджи, который обеспечивает экзоцитоз медиаторов, предварительно упаковывая их в мембранные пузырьки-везикулы. Размер пузырьков и количество в них молекул медиатора стабильны в каждом конкретном нейроне.
| Рис. 3.18. Синтез медиатора: а — в теле нейрона; б — в пресинаптическом окончании; 1 — ядро клетки; 2 — ЭПС; 3 — везикулы с медиатором; 4 — молекулы медиатора; 5 — комплекс Гольджи; 6 — пустые везикулы |  |
Образовавшиеся везикулы переносятся в пресинаптические окончания. Ключевую роль в этом процессе играют направляющие микротрубочки. Пузырьки с медиатором движутся по этим «рельсам» с помощью механизмов, сходных с работой сократимых мышечных белков. Скорость такого транспорта довольно велика — до нескольких см/ч.
В случае, когда медиатор синтезируется сразу в пресинаптическом окончании, комплекс Гольджи способен формировать пустые везикулы, которые аналогичным образом переносятся по аксону. Заполнение таких пузырьков медиатором осуществляется непосредственно в пресинаптическом окончании (за счет работы специальных молекулярных насосов (рис. 3.18, б)).
Везикулы — это не только удобная форма транспорта веществ, но и способ упорядочить, сделать количественно стабильным выброс медиатора в синаптическую щель. Число скапливающихся в пресинаптическом окончании везикул измеряется десятками тысяч, что также стабилизирует процессы передачи сигналов; истощение запасов медиатора даже при интенсивном проведении информации происходит весьма редко (обычно на фоне действия специальных фармакологических агентов).
Каждый нейрон производит только один основной медиатор (ацетилхолин, дофамин и т. п.). Однако нередко можно обнаружить присутствие в пресинаптическом окончании и других веществ, способных к передаче нервных сигналов. Это комедиаторы (например, пептиды); они обнаруживаются в очень небольших количествах и обычно находятся в везикулах, отличающихся по форме и размеру от пузырьков с основным медиатором.
Выброс содержимого везикул запускается в момент прихода в пресинаптическое окончание потенциала действия и реализуется в несколько этапов. Первый из них заключается в открытии потенциал-зависимых Ca2+- каналов, которые расположены на «внешней» мембране пресинаптического окончания и открываются при его деполяризации в момент прихода ПД (рис. 3.19). В результате наблюдается вход в клетку определенной порции ионов Ca2+, и их содержание внутри окончания возрастает в 10—100 раз. Чем выше концентрация Ca2+ во внешней среде, тем больше число вошедших ионов; через эти же каналы способны проникать ионы Mg2+, конкурируя с кальцием. Следовательно, появление в межклеточной среде магния уменьшает итоговое число вошедшего в окончание кальция.
Основное назначение ионов Ca2+ в пресинаптическом окончании — это воздействие на сложный белковый комплекс, встроенный в мембрану везикул. Этот комплекс включает белки, ответственные за фиксацию пузырька в цитоплазме и за его контакт с пресинаптической мембраной. Под действием Ca2+ (для этого нужно четыре иона) везикула приходит в движение. Достигая пресинаптической мембраны, пузырек «слипается» с ней, в результате чего медиатор попадает в синаптическую щель. Весь этот процесс протекает очень быстро — в течение 1—5 мс, а примерно через 10 с можно наблюдать процесс восстановления везикул: они отделяются от мембраны и возвращаются в пресинаптическое окончание. В дальнейшем эти пустые пузырьки могут быть вновь заполнены медиатором.
 | |
| Рис. 3.19. Основные этапы выброса медиатора из пресинаптического окончания: 1 — потенциал действия, открывающий Ca2+-каналы; 2 — вход ионов Ca2+ в пресинаптическое окончание; 3 — ионы Ca2+, соединяющиеся с мембраной везикул; 4 — везикулы; 5 — взаимодействие везикулы с мембраной и выброс медиатора в синаптическую щель; 6 — снижение концентрации ионов Ca2+ в синаптическом окончании; 7 — митохондрия; 8 — ЭПС; o — ионы Ca2+, × — медиатор |
Запустить выброс содержимого везикул чрезвычайно важно, но не менее важно быстро остановить этот процесс. Только в этом случае возможно точное соответствие между числом пришедших в пресинаптическое окончание ПД и количеством выделившегося медиатора. Функцию остановки выброса выполняют особые молекулярные насосы, удаляющие ионы Ca2+ из цитоплазмы окончания. Такие насосы находятся на мембранах каналов ЭПС и митохондрий. Перенося кальций внутрь этих органоидов, они прекращают его действие на везикулы.
Отравление Ca2+-насосов ведет к гиперактивности синапса, продолжающейся до полного истощения запасов медиатора. Аналогичное действие оказывают токсины, блокирующие потенциал-зависимые Ca2+-каналы в открытом положении.
Токсин ботулиновой бактерии (ботулотоксин) известен как соединение, вызывающее тяжелейшие пищевые отравления. Проникая в синапс, он блокирует белки, отвечающие за контакт везикулы с пресинаптической мембраной, в результате чего прекращается всякая передача нервного сигнала, развиваются параличи.
Попав в синаптическую щель, медиатор менее чем за 1 мс вступает во взаимодействие с пресинаптической мембраной, соединяясь с встроенными в нее специализированными белковыми рецепторами. Пространственная организация рецептора предусматривает существование у него активного центра — углубления в белковом клубке, имеющего определенную форму и распределение зарядов. Ему строго соответствует пространственная конфигурация медиатора и распределение зарядов на его молекуле. В результате активный центр рецептора и медиатор способны формировать комплекс. Непосредственным следствием этого является возбуждение рецептора, а затем — развитие постсинаптических потенциалов и запуск ПД.
Выделяют два типа рецепторов — ионотропные и метаботропные.
Возбуждение метаботропного рецептора выражается в изменении внутриклеточного метаболизма, т. е. течения биохимических реакций. С внутренней стороны мембраны к такому рецептору присоединен целый ряд других белков, выполняющих ферментативные и частью передающие («посреднические») функции (рис. 3.20). Белки-посредники относятся к G-белкам. Под влиянием возбужденного рецептора G-белок воздействует на белок-фермент, обычно переводя его в «рабочее» состояние. В результате запускается химическая реакция: молекула-предшественник превращается в сигнальную молекулу — вторичный посредник.
 | |
| Рис. 3.20. Схема строения и функционирования метаботропного рецептора: 1 — медиатор; 2 — рецептор; 3 — ионный канал; 4 — вторичный посредник; 5 — фермент; 6 — G-белок; →— направление передачи сигнала |
Вторичные посредники — это мелкие, способные к быстрому перемещению молекулы или ионы, передающие сигнал внутри клетки. Этим они отличаются от «первичных посредников» — медиаторов и гормонов, передающих информацию от клетки к клетке. Наиболее известным вторичным посредником является цАМФ (циклическая аденозинмонофосфорная кислота), образуемая из АТФ с помощью фермента аденилатциклазы. Похожа на него цГМФ (гуанозинмонофосфорная кислота). Другими важнейшими вторичными посредниками являются инозитолтрифосфат и диацилглицерол, образуемые из компонентов клеточной мембраны под действием фермента фосфолипазы С. Чрезвычайно велика роль Ca2+, входящего в клетку снаружи через ионные каналы или высвобождающегося из особых мест хранения внутри клетки («депо» кальция). В последнее время много внимания уделяется вторичному посреднику NO (оксиду азота), который способен передавать сигнал не только внутри клетки, но и между клетками, легко преодолевая мембрану, в том числе от постсинаптического нейрона к пресинаптическому.
Заключительный шаг в проведении химического сигнала — воздействие вторичного посредника на хемочувствительный ионный канал. Это воздействие протекает либо непосредственно, либо через дополнительные промежуточные звенья (ферменты). В любом случае происходит открытие ионного канала и развитие ВПСП либо ТПСП. Продолжительность и амплитуда их первой фазы будет определяться количеством вторичного посредника, которое зависит от количества выделившегося медиатора и длительности его взаимодействия с рецептором.
Таким образом, механизм передачи нервного стимула, используемый метаботропными рецепторами, включает в себя несколько последовательных этапов. На каждом из них возможна регуляция (ослабление либо усиление) сигнала, что делает реакцию постсинаптической клетки более гибкой и адаптированной к текущим условиям. Вместе с тем это же приводит к замедлению процесса передачи информации. Вот почему в ходе эволюции возникла потребность в более быстром пути проведения сигналов, в результате чего появились ионотропные рецепторы.
В случае ионотропного рецептора чувствительная молекула содержит не только активный центр для связывания медиатора, но также ионный канал (рис. 3.21). Воздействие «первичного посредника» на рецептор приводит к быстрому открыванию канала и развитию постсинаптического потенциала.
| Рис. 3.21. Схема строения и функционирования ионотропного рецептора: 1 — медиатор; 2 — рецептор |  |
| Рис. 3.22. Пути инактивации медиатора в синапсе |  |
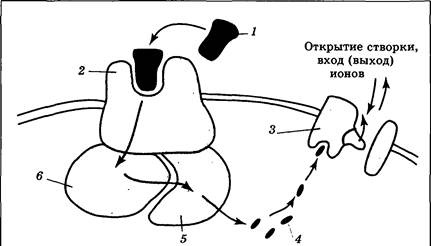
Инактивация — заключительный этап жизненного цикла медиатора. Смысл этой стадии состоит в прекращении его действия на рецептор (прерывание передачи сигнала). Процессы инактивации медиатора реализуются при участии специализированных ферментов и транспортных белков (рис. 3.22).
В более простом случае инактивация осуществляется прямо в синаптической щели, когда фермент 2 быстро разрушает все свободно «плавающие» молекулы медиатора. Кроме этого, медиатор может быть удален с активных центров постсинаптических рецепторов 1 еще двумя способами: путем обратного всасывания в пресинаптическое окончание, которое осуществляется особыми белками-насосами 3 и путем всасывания в глиальные клетки, которое также происходит за счет деятельности белков-насосов 5.
В случае переноса внутрь глиальных клеток медиатор разрушается специализированным ферментом.
В случае возврата в пресинаптическое окончание («обратный захват») он также может быть разрушен, но может и повторно «загружаться» в пустые везикулы 4. Это позволяет наиболее экономно расходовать те медиаторы, синтез которых связан с определенными проблемами (недостаток предшественника, длинная цепочка реакций).
Скорость процесса инактивации определяет общее время воздействия медиатора на рецептор, от которого в конечном итоге зависит амплитуда постсинаптических потенциалов, запуск ПД и продолжение проведения сигнала по нейронной сети. При повреждении элементов системы инактивации наблюдается значительное увеличение эффективности синаптической передачи, так как выделившийся медиатор существенно дольше воздействует на рецепторы и амплитуда ВПСП либо ТПСП заметно возрастает.
Вещества, влияющие на различные этапы жизненного цикла медиаторов, имеют огромное значение для жизни человека. Именно они образуют группу психотропных препаратов — соединений, влияющих на различные аспекты деятельности мозга: общий уровень активности, память, эмоциональные переживания. При этом наиболее часто используются вещества, изменяющие взаимодействие рецептора и медиатора, а также влияющие на хемочувствительные ионные каналы.
При введении молекул, сходных по структуре с медиатором, наблюдается их соединение с активными центрами соответствующих рецепторов и последующее возбуждение рецепторов (рис. 3.23). Медиатор 1 присоединяется к рецептору 2, что приводит к воздействию на ионный канал 3 (направление воздействия отмечено стрелкой; рис. 3.23, а); агонист 4 присоединяется к рецептору, что также приводит к передаче сигнала на ионный канал (рис. 3.23, б); конкурентный антагонист 5 не позволяет медиатору соединиться с рецептором (отмечено перечеркнутой стрелкой; рис. 3.23, в); неконкурентный антагонист 6 блокирует ионный канал, что также не позволяет развиться эффектам медиатора (отмечено перечеркнутой стрелкой; рис. 3.23, г). В результате эффект применяемого препарата оказывается аналогичен действию самого медиатора. Вещества такого рода называют агонистами медиатора, их влияние на синапс нередко оказывается очень длительным и эффективным. Это объясняется тем, что прочность связывания агониста с рецепторами нередко больше, чем у медиатора, а системы инактивации не способны быстро опознать агонист и убрать его из синаптической щели.
 |  | |
 |  | |
| Рис. 3.23. Механизмы деятельности агонистов и антагонистов медиаторов |
В более сложном случае вводимые молекулы лишь частично похожи на медиатор. Тогда, соединяясь с активными центрами рецепторов, они будут их занимать (прекращать к ним доступ медиатора; конкурировать с ним), но не будут возбуждать рецептор. В результате эффект применяемого препарата будет противоположен действию медиатора. Вещества такого рода называют конкурентными антагонистами медиатора. Существует также понятие неконкурентного антагониста (вводимый препарат мешает работе медиатора, блокируя хемочувствительные ионные каналы).
Часть агонистов и антагонистов медиаторов являются веществами природного происхождения. Их существование — результат длительных эволюционных процессов, в ходе которых одни живые организмы (особенно растения) «изобретали» вещества, защищающие их от поедания другими организмами. Природными психотропными препаратами являются также яды животных-охотников (змеи, пауки).
Вторая часть агонистов и антагонистов — синтетические соединения, создаваемые человеком. В ходе их разработки химикам и фармакологам приходится учитывать целый ряд требований. Во-первых, в структуре такого вещества должен присутствовать «ключевой» участок, соответствующий молекуле медиатора. Во-вторых, такой препарат должен быть устойчив к действию систем инактивации. В-третьих, он должен проникать через барьеры организма — гематоэнцефалический и желательно кишечный. Только в этом случае можно достичь мозга при системном введении — в виде таблетки либо инъекции. В настоящее время агонисты и антагонисты медиаторов (а также соединения, влияющие на синаптическую передачу другими путями) широко применяются в клинике. Вместе с тем в больших дозах многие из них являются наркотиками и ядами, что также свидетельствует о необходимости их серьезного изучения.
Ацетилхолин
По химическому строению ацетилхолин представляет собой соединение двух молекул — азотсодержащего холина и остатка уксусной кислоты:
 |
Холин является незаменимым витаминоподобным соединением, получаемым с пищей в достаточном количестве, и последствия его дефицита наблюдаются только в искусственных условиях. Синтез ацетилхолина осуществляется в основном в пресинаптических окончаниях с помощью фермента холинацетилтрансферазы. Затем медиатор переносится в пустые везикулы и хранится в них до момента выброса.
Ацетилхолин в качестве медиатора работает в трех функциональных блоках нервной системы: в нервно-мышечных синапсах, периферической части вегетативной нервной системы и некоторых областях ЦНС.
Ацетилхолин является медиатором мотонейронов нервной системы, которые расположены в передних рогах серого вещества спинного мозга и двигательных ядрах черепных нервов. Их аксоны направляются к скелетным мышцам и, разветвляясь, образуют нервно-мышечные синапсы. При этом один аксон может устанавливать контакт с сотнями мышечных волокон, но каждое мышечное волокно управляется только одним синапсом. Размер нервно-мышечных синапсов в десятки раз больше, чем синапсов в ЦНС, и пришедший по аксону мотонейрона даже одиночный ПД вызывает выделение значительного количества ацетилхолина (этап I, рис. 3.24). В результате развивающаяся на постсинаптической мембране деполяризация оказывается настолько велика, что всегда запускает ПД мышечной клетки (II), который приводит к выбросу Ca2+ из каналов ЭПС (III), активации двигательных белков и сокращению (IV).
Периферическое звено вегетативной нервной системы состоит из двух нейронов: тело первого (преганглионарного) находится в ЦНС, а аксон направляется к вегетативному ганглию; тело второго (постганглионарного) находится в ганглии, а аксон иннервирует гладкие мышечные или железистые клетки внутренних органов. Ацетилхолин в качестве медиатора вырабатывается во всех преганглионарных клетках, а также в постганглионарных клетках парасимпатической части вегетативной нервной системы (рис. 3.25). Некоторые постганглионарные симпатические волокна (активирующие потовые железы и вызывающие расширение сосудов) также секретируют ацетилхолин.
 | |
| Рис. 3.24. Этапы I—IV работы нервно-мышечного синапса: 1 — везикулы с ацетилхолином; 2 — поперечная трубочка, углубляющаяся в цитоплазму мышечной клетки; 3 — канал ЭПС; 4 — ионы Ca2+; 5 — двигательные белки мышечной клетки; 6 — никотиновый рецептор; 7 — пресинаптическое окончание |
В ЦНС ацетилхолин вырабатывается частью нейронов ретикулярных ядер моста и интернейронами полосатого тела базальных ганглиев и некоторых других локальных зон. Рассматривается роль этого медиатора в регуляции уровня бодрствования, а также в системах памяти, двигательных системах. Доказана эффективность применения антагонистов ацетилхолина при ряде двигательных нарушений.
Выделяясь из пресинаптического окончания, ацетилхолин действует на постсинаптические рецепторы. Эти рецепторы неоднородны и различаются локализацией и рядом свойств. Выделено два типа рецепторов (рис. 3.26): первый, помимо ацетилхолина, возбуждается под действием алкалоида табака никотина (никотиновые рецепторы), второй тип активируется ацетилхолином и токсином мухомора мускарином (мускариновые рецепторы).
 | |
| Рис. 3.25. Схема распределения медиаторов в периферической нервной системе: 1 — нейроны ЦНС, образующие двигательные нервы (мотонейроны); 2 — нейроны ЦНС, образующие преганглионарные волокна парасимпатической нервной системы; 3 — нейроны ЦНС, входящие в состав симпатической нервной системы (три варианта строения); 4 — мышца; 5 — орган (парасимпатическая система); 6 — орган (симпатическая система); 7 — надпочечник (симпатическая система); 8 — потовая железа (расширение сосудов, симпатическая система); м, н — мускариновые и никотиновые рецепторы;? — нейроны, вырабатывающие ацетилхолин;? — нейроны, вырабатывающие норадреналин |
Никотиновые рецепторы являются классическим примером ионотропных рецепторов: их ионный канал входит в состав рецептора и открывается сразу после присоединения ацетилхолина. Канал этот характеризуется универсальной проницаемостью для положительно заряженных ионов, но в обычных условиях (при открытии на фоне ПП) в связи с никотиновыми рецепторами наблюдается в основном входящий Na+-ток, вызывающий деполяризацию мембраны и возбуждение нейрона.
Никотиновые рецепторы расположены на постсинаптической мембране поперечно-полосатых волокон скелетных мышц (нервно-мышечные синапсы); в синапсах вегетативных ганглиев и в меньшем количестве, чем мускариновые рецепторы, в ЦНС. Областью, наиболее чувствительной к никотину, являются вегетативные ганглии, поэтому первые попытки курения приводят к значительным нарушениям в деятельности органов: скачкам артериального давления, тошноте, головокружению. По мере привыкания сохраняется в основном симпатический компонент действия: никотин начинает работать преимущественно как стимулятор многих систем организма. Присутствует также и центральное активирующее влияние (на головной мозг) ацетилхолина. Сверхдозы никотина (50 и более мг) вызывают резкое учащение сердцебиения, судороги и остановку дыхания.
 | |
| Рис. 3.26. Схемы никотинового (с) и мускаринового (б) рецепторов к ацетилхолину Ацх: 1 — рецептор; 2 — фермент; 3 — G-белок; 4 — вторичный посредник; 5 — ионный канал; * — место сужения (створка) ионного канала |
Во время курения никотин действует как слабый наркотический препарат-стимулятор, вызывая развитие не только привыкания, но и зависимости. Наркотическая зависимость — это ситуация, когда организм включает поступающий извне препарат в свой метаболизм, т. е. начинает «рассчитывать» на его постоянный приток. При отказе от препарата происходит сбой в использующих его системах мозга: наблюдается резкое ухудшение самочувствия, депрессия (абстинентный синдром или синдром отмены). Человеку, попавшему в зависимость, наркотик необходим уже не столько для того, чтобы почувствовать бодрость и эйфорию, сколько для возврата хотя бы к относительно нормальному уровню жизнедеятельности.
Наиболее известным антагонистом никотиновых рецепторов является тубокурарин — активное действующее начало яда некоторых южноамериканских растений. Основным «местом приложения» его влияния являются нервно-мышечные синапсы (рис. 3.27, вариант I). При этом происходит последовательное расслабление и паралич мышц пальцев, затем глаз, рук и ног, шеи, спины и, наконец, дыхательных.
Мускариновые рецепторы являются метаботропными (рис. 3.26, б); они связаны с G-белками, и присоединение к ним ацетилхолина приводит к синтезу вторичных посредников.
Выделяют две основные локализации мускариновых рецепторов: синапсы, образуемые постганглионарными (в основном парасимпатическими) вегетативными волокнами и ЦНС. В первом случае в качестве вторичных посредников используются инозитолтрифосфат и диацилглицерол; во втором — цГМФ. Ионные последствия возбуждения мускариновых рецепторов весьма разнообразны: в сердце наблюдается увеличение проводимости для ионов К+, что приводит к гиперполяризации и снижению частоты сокращений; в гладких мышцах отмечаются изменения проводимости как для К+, так и для Na+ (возможна гипер- или деполяризация в зависимости от конкретного органа).
В ЦНС отмечается снижение проницаемости мембраны для К+ (деполяризация; возбуждающее действие), но синапсы, содержащие мускариновые рецепторы, могут располагаться как на тормозных, так и на возбуждающих нейронах коры и базальных ганглиев. В связи с этим последствия блокады либо активации мускариновых рецепторов на поведенческом уровне оказываются очень индивидуальны; их выраженность и направленность зависит от конкретной химической структуры того или иного препарата.
Эффекты мускарина носят преимущественно парасимпатический характер: при отравлении мухоморами наблюдается тошнота, повышенное пото- и слюноотделение, слезотечение, боли в животе, снижение артериального давления и сердечной активности.
Классическим антагонистом мускариновых рецепторов является атропин — токсин белены и дурмана. Его периферические эффекты прямо противоположны действию мускарина: происходит снижение тонуса мышц желудочно-кишечного тракта, учащается сердцебиение, прекращается слюноотделение (сухость во рту), расширяются зрачки, наблюдаются и центральные эффекты (двигательное и речевое возбуждение, галлюцинации).
 | |
| Рис. 3.27. Варианты I—IV воздействия на работу нервно-мышечного синапса: I — на никотиновый рецептор (тубокурарин); II — на ацетилхолинэстеразу (прозерин); III — на выделение ацетилхолина (бета-нейротоксин); IV — путем выработки антител к никотиновому рецептору; 1 — везикулы с ацетилхолином; 2 — ацетилхолинэстераза; 3 — никотиновый рецептор |
Инактивация ацетилхолина происходит непосредственно в синаптической щели. Ее осуществляет фермент ацетилхолинэстераза, разлагающий медиатор до холина и остатка уксусной кислоты, затем холин всасывается в пресинаптическое окончание и может вновь использоваться для синтеза ацетилхолина.
Ацетилхолинэстераза имеет активный центр, узнающий холин, и один активный центр, «отрывающий» ацетильную группу от исходной молекулы. Последний часто является местом атаки специфических блокаторов (рис. 3.27, вариант II).
Примером подобного блокатора служит прозерин (неостигмин), применяемый при миастении, которая встречается примерно у трех человек на тысячу (чаще у женщин). Симптомами заболевания служат быстрая мышечная утомляемость, непроизвольное опускание век, замедленное жевание. Такие больные очень чувствительны к тубокурарину, а введение блокаторов ацетилхолинэстеразы ослабляет патологические проявления. В настоящее время известно, что у значительной части больных миастенией число никотиновых рецепторов примерно на 70% меньше, чем в норме. Причина этого состоит в том, что иммунная система больного вырабатывает антитела на никотиновые рецепторы. Эти антитела ускоряют разрушение рецепторов на мембране, ослабляя передачу в нервно-мышечном синапсе (рис. 3.27, вариант IV).
Прозерин и сходные с ним препараты называют обратимыми блокаторами ацетилхолинэстеразы, их действие прекращается через несколько часов после введения, кроме того, существуют необратимые блокаторы того же фермента. В этом случае вещество, нарушающее работу ацетилхолинэстеразы, вступает с белком в устойчивую химическую связь и выводит его из строя. Таким образом действуют фосфорорганические соединения, применяемые как препараты против насекомых (инсектициды): хлорофос, тиофос и сходные с ними соединения могут вызвать у человека сужение зрачков, потливость, снижение артериального давления, подергивания мышц.
Еще более сильными агентами-блокаторами являются различные нервно-паралитические газы (зарин): легко проникая через все барьеры организма, они вызывают судороги, потерю сознания и паралич. Смерть наступает от остановки дыхания. Для немедленного ослабления эффектов отравляющих газов рекомендуется использование атропина; для восстановления деятельности ацетилхолинэстеразы — особые вещества-реактиваторы, «отрывающие» блокатор от фермента.
Другим примером разрушительного действия на ацетилхолинергический (использующий ацетилхолин в качестве медиатора) синапс являются нейротоксины змей. Например, яд кобры содержит альфа-нейротоксин, необратимо связывающийся с никотиновым рецептором и блокирующий его, а также бета-нейротоксин, который тормозит выделение медиатора из пресинаптического окончания (рис. 3.27, варианты I, III).
Норадреналин
Медиатор норадреналин относится к катехоламинам — производным аминокислоты тирозина. Тирозин — одна из незаменимых аминокислот, которые мы получаем только с пищей. Цепочка химических превращений, ведущая к последовательному образованию трех катехоламинов — дофамина, норадреналина и адреналина, представлена ниже:
 |  |
 | |
| Рис. 3.28. Схема распределения в головном мозге нейронов, вырабатывающих норадреналин: 1 — голубое пятно моста; 2 — межножковое ядро среднего мозга; 3 — распределение аксонов по ЦНС |
Ключевая и наиболее медленная стадия — превращение тирозина в L-ДОФА (диоксифенилаланин), где особое значение имеет регулирующий фермент тирозингидроксилаза.
Адреналин является гормоном надпочечников, а дофамин — медиатором ЦНС. Норадреналин играет важную роль в центральной и периферической нервной системе.
На периферии норадреналин является медиатором большинства постганглионарных симпатических синапсов. Воздействуя на внутренние органы, он конкурирует с эффектами ацетилхолина. В ЦНС норадреналин вырабатывается нейронами голубого пятна (мост) и межножкового ядра (средний мозг). Аксоны клеток этих небольших ядер в дальнейшем можно встретить в различных структурах головного и спинного мозга (рис. 3.28).
Синтез норадреналина осуществляется в пресинаптических окончаниях, затем он переносится в пустые везикулы и хранится до момента выброса. Выделяясь в синаптическую щель, норадреналин действует на постсинаптические рецепторы, которые неоднородны и подразделяются на два типа — альфа- и бета-адренорецепторы. Оба они являются метаботропными, но разница состоит в том, что альфа-адренорецепторы в качестве вторичных посредников используют инозитолтрифосфат (ИТФ), диацилглицерол (ДАТ) и ионы Ca2+, а бета-адренорецепторы соединены с ферментом аденилатциклазой, продуцирующей циклический аденозинмонофосфат (цАМФ).
Именно исследование бета-адренорецепторов позволило в свое время выявить существование системы вторичных посредников и описать основные ее свойства. Следствием активации адренорецепторов может быть изменение как натриевой, так и калиевой проводимости (возбуждающие либо тормозящие эффекты в зависимости от конкретного места расположения). Классическим агонистом альфа-адренорецепторов является препарат фетанол, антагонистом — фентоламин (табл. 3.1). В случае бета-адренорецепторов наиболее известны агонист изадрин и антагонист пропранолол (синонимы — анаприлин, индерал, обзидан).
| Таблица 3.1 НЕКОТОРЫЕ СВОЙСТВА АЛЬФА- И БЕТА-АДРЕНОРЕЦЕПТОРОВ | ||
| Альфа-адренорецепторы | Бета-адренорецепторы | |
| Агонисты | Фетанол, эфедрин, нафтизин | Изадрин, эфедрин |
| Антагонисты | Фентоламин | Пропранолол |
| Вторичные посредники | ИТФ, ДАГ, Ca2+ | цАМФ |
| Примеры локализации | Сосуды (сужение), ЖКТ, ЦНС | Бронхи (расширение), сердце, ЖКТ, ЦНС |
| Токсины, повреждающие G-белки | Токсины коклюша и холеры |
В случае симпатической нервной системы на каждом внутреннем органе можно встретить альфа- или бета-адренорецепторы либо оба их типа. Альфа-рецепторы имеют большинство сосудов, которые сужаются под действием норадреналина и агонистов альфа-адренорецепторов, в результате чего повышается артериальное давление. Агонистами альфа-адренорецепторов являются также препараты нафтизин (синоним — санорин) и галазолин: при нанесении на слизистую носа они сужают сосуды, прекращая насморк. Фентоламин, напротив, расширяет сосуды и снижает артериальное давление.
Органами, содержащим только бета-адренорецепторы, являются сердечная мышца и гладкие мышцы бронхов: норадреналин и изадрин стимулируют деятельность сердца и расширяют бронхи (последний эффект используется для ослабления приступов бронхиальной астмы). С другой стороны, пропранолол является эффективным средством для лечения заболеваний, связанных с нарушениями сердечного ритма и гипертонической болезнью.
Кратко перечислим влияния вегетативной нервной системы на некоторые другие органы. Работа желудочно-кишечного тракта усиливается под действием парасимпатической системы и ослабляется под действием симпатической (участвуют альфа- и бета-адренорецепторы). Сфинктеры (запирающие мышцы) кишечника и мочевого пузыря под влиянием симпатической нервной системы сокращаются (альфа-адренорецепторы). Выделение секрета слезных, слюнных и пищеварительных желез зависит в основном от парасимпатической нервной системы и очень слабо — от симпатической. Потоотделение управляется симпатической системой, но за счет постганглионарного выделения ацетилхолина.
Вегетативное действие норадреналина существенно дополняется гормональными эффектами адреналина, который секретируется надпочечниками и влияет на те же типы адренорецепторов. Выброс адреналина вызывается симпатической нервной системой. Следовательно, можно говорить о целостной реакции, которая возникает при стрессе, нагрузке, эмоциях, обусловлена катехоламинами и приводит системы организма в состояние готовности к оптимальному ответу.
Прямое подкожное или внутривенное введение адреналина вызывает активацию как альфа-, так и бета-адренорецепторов (сужение сосудов и рост артериального давления; стимуляция деятельности сердца); введение норадреналина — активацию преимущественно альфа-адренорецепторов (влияет в основном на давление). Внутривенное введение их предшественника дофамина приводит к росту возбуждения симпатических синапсов и используется при острой сердечной и сосудистой недостаточности, шоках и других патологических состояниях. При этом дофамин не проникает через гематоэнцефалический барьер и не влияет на головной мозг, где работает в норме в качестве медиатора.
Норадренергические (вырабатывающие норадреналин в качестве медиатора) нейроны расположены в голубом пятне и межножковом ядре среднего мозга, их аксоны образуют чрезвычайно широкую сеть проекций, в результате чего соответствующие синапсы можно обнаружить в большой концентрации в разных отделах ЦНС от спинного до конечного мозга, в том числе в коре мозжечка и больших полушарий (содержат как альфа-, так и бета-адренорецепторы). Перечислим основные группы функций, реализуемых с их участием:
1) создание определенного уровня активации бодрствующей ЦНС (за счет прежде всего торможения центров сна);
2) участие в тормозной регуляции сенсорных потоков; обезболивающее (анальгетическое) действие, способное ярко проявляться при сильном стрессе;
3) регуляция уровня двигательной активности: норадренергические проекции способны ее повышать, выключая тормозные интернейроны в моторных центрах;
4) участие в регуляции активности различных центров биологических потребностей и мотиваций (снижение уровня тревожности, повышение уровня агрессивности);
5) влияние на выраженность эмоциональных компонентов поведения: эмоции, возникающие в стрессовых условиях (опасность, значительная умственная и физическая нагрузка), и эмоции, соответствующие таким понятиям, как «азарт», «удовольствие от риска»; в зависимости от индивидуальной организации мозга значимость таких эмоций для конкретного человека может быть разной, но иногда — очень большой;
6) участие в процессах обучения (запоминания информации), протекающих в корковых зонах ЦНС; в этом случае активность норадренергических проекций регулируется центрами положительного и отрицательного подкрепления мозга; выделение медиатора приводит к долговременным изменениям свойств синапсов в нейронных сетях коры больших полушарий и мозжечка.
Основные функции норадренергической системы показывают, что, практически не участвуя в прямом проведении нервных сигналов, норадреналин способен модулировать потоки информации и регулировать общее состояние ЦНС. Легко представить последствия как избыточной, так и недостаточной активности норадренергической системы: в первом случае мы можем столкнуться с гиперактивностью и психотическими проявлениями, во втором — с апатией, депрессией, ухудшением памяти; в первом случае могут оказаться необходимыми препараты с нейролептическими свойствами, во втором — антидепрессанты.
Обе эти группы препаратов способны влиять на активность норадренергической системы, но ситуация осложняется тем, что в регуляции уровня эмоций и двигательной активности, кроме норадреналина, участвуют и другие медиаторы, в частности, дофамин и серотонин.
Большинство агонистов и антагонистов адренорецепторов являются синтетическими веществами, которые появились в результате работ с химически модифицированными молекулами адреналина и норадреналина. Из природных соединений, влияющих на эту медиаторную систему, известен эфедрин — алкалоид небольшого голосеменного кустарника эфедры, который действует как смешанный агонист альфа- и бета-адренорецепторов. В клинике он используется для повышения артериального давления, расширения бронхов, расширения зрачков, при насморке. При передозировке проявляются центральные эффекты эфедрина — нервное возбуждение, бессонница, дрожание конечностей; в токсических дозах — судороги. Длительное применение эфедрина может вызвать привыкание.
Обнаружено также, что симптомы коклюша и холеры развиваются через периферические адренорецепторы: токсины, вырабатываемые соответствующими микроорганизмами, выключают расслабляющее действие симпатической нервной системы на гладкую мускулатуру бронхов и кишечника. При этом непосредственной «мишенью» токсинов являются связанные с адренорецепторами G-белки и система синтеза вторичных посредников.
В отличие от ацетилхолина, катехоламины мало разлагаются в синаптической щели, а в основном всасываются в пресинаптическое окончание. Обратный захват норадреналина осуществляется особыми белками-насосами. Попав в пресинаптическое окончание, норадреналин может повторно «загружаться» в везикулы, но может и разлагаться с помощью фермента моноаминоксидазы (МАО). Инактивация происходит внутри митохондрий, на внутренней мембране которых располагается МАО. Чрезвычайно важно, что этот фермент осуществляет разложение и других моноаминов — дофамина и серотонина. Оказалось, что использование блокаторов МАО позволяет повысить активность всех трех медиаторных систем (антидепрессантные эффекты).
 | |
| Рис. 3.29. Схема регуляции деятельности норадренергического синапса: 1 — везикулы с норадреналином; 2 — постсинаптический рецептор; 3 — белок-насос, осуществляющий обратное всасывание норадреналина; 4 — пресинаптический рецептор, активизирующий тирозингидроксилазу (ТГ); 5 — молекулы норадреналина |
Еще одним важным свойством норадренергического синапса является наличие в нем пресинаптических адренорецепторов. Выделяемый в щель медиатор, воздействуя на них, тем самым активирует систему вторичных посредников, что приводит к активации тирозингидроксилазы и ускорению синтеза норадреналина (рис. 3.29). Наличие пресинаптических рецепторов — частое свойство синапсов; они позволяют осуществлять обратную регуляцию активности нервной передачи и увеличивать образование медиатора, если его выброс идет очень активно (как в случае норадреналина), либо, напротив, тормозить этот выброс (влияя на пресинаптические К+-каналы) в целях предохранения синаптической щели от перенасыщения медиатором.
Дофамин
Дофамин относится к катехоламинам. Дофаминергические нейроны встречаются в трех отделах головного мозга: черной субстанции (ее компактной части), покрышке среднего мозга и в различных ядрах гипоталамуса (рис. 3.30). В периферической нервной системе его практически нет.
| Рис. 3.30. Схема распределения в головном мозге нейронов, вырабатывающих дофамин, и распределение их аксонов: 1 — покрышка среднего мозга; 2 — черная субстанция среднего мозга; 3 — кора больших полушарий; 4 — ядра гипоталамуса; 5 — полосатое тело |  |
Нейроны черной субстанции направляют аксоны к конечному мозгу, где образуются синапсы на клетках полосатого тела (скорлупа и хвостатое ядро, относящиеся к базальным ганглиям). Функция этих проекций состоит в поддержании общего уровня двигательной активности, обеспечении точности выполнения моторных программ, устранении непроизвольных движений. В случае дегенерации черной субстанции развивается заболевание — паркинсонизм. Его основные симптомы состоят в затрудненном запуске движений (акинезия), патологически усиленном мышечном тонусе (ригидность), дрожании пальцев и головы (тремор). На начальной стадии заболевания преобладает один из симптомов; позже они комбинируются, образуя характерный комплекс двигательных нарушений.
Болезнь обычно прогрессирует в течение 10—20 и более лет. Причины дегенерации могут быть различными: генетические аномалии, образование токсических продуктов окисления дофамина, нарушение функции нейроглии и др. Известно, что риск развития паркинсонизма увеличивается с возрастом, а также в результате различных экстремальных воздействий на ЦНС (механические удары, отравления, клиническая смерть).
Препараты, применяемые для лечения паркинсонизма, не устраняют его причин, а лишь облегчают тяжесть состояния, ослабляют симптоматику. Они делятся на две группы. К первой относятся антагонисты центральных никотиновых и мускариновых рецепторов (например, циклодол и акинетон). Снижая активность ацетилхолинергических интернейронов полосатого тела, они способны значительно ослабить тремор.
Вторая группа препаратов — это L-ДОФА (L-диоксифенилаланин) и его производные (табл. 3.2).
| Таблица 3.2 ПСИХОТРОПНЫЕ ПРЕПАРАТЫ, ВОЗДЕЙСТВУЮЩИЕ НА ДОФАМИНЕРГИЧЕСКУЮ СИСТЕМУ | |
| Препарат | Механизм действия, применение |
| L-ДОФА | Препарат для лечения болезни Паркинсона |
| Апоморфин | D1-, D2-агонист |
| Бромкриптин | D2 -агонист |
| Фенамин, амфетамины | Стимуляторы выброса дофамина |
| Кокаин | Блокатор обратного захвата |
| Аминазин | Антагонист дофаминовых и норадреналиновых рецепторов, нейролептик |
| Галоперидол | D2 -антагонист, нейролептик |
L-ДОФА является непосредственным предшественником дофамина в цепочке синтеза катехоламинов, а также хорошо проходит гематоэнцефалический барьер. Превращаясь в дофамин непосредственно в базальных ганглиях, он восполняет недостаток медиатора, возникший в результате дегенерации черной субстанции. Влияние препарата распространяется преимущественно на симптомы ригидности и акинезии.
Проекции нейронов покрышки направляются к корковым областям, обонятельной (древней) коре, гиппокампу, ассоциативной лобной, премоторной, моторной, зрительной коре, часть аксонов контактирует с ядрами миндалины. Существование этой системы позволяет на структурном уровне подтвердить участие дофамина в поддержании не только общего уровня бодрствования мозга, но и тонуса высших центров, связанных с сенсорным восприятием, управлением движениями, памятью, эмоциями.
Дофаминергические нейроны гипоталамуса обладают короткими аксонами; они формируют три вида проекций: к субталамическим ядрам, нейроэндокринным зонам и потребностно-мотивационным центрам гипоталамуса.
В первом случае речь идет о регуляции общей интенсивности локомоции (т. е. ритмических движений, связанных с перемещениями в пространстве). Именно субталамические ядра отдают команду о начале локомоции, ее ускорении, переходе с шага на бег.
Второй тип проекций подразумевает влияние на уровень активности нейроэндокринных ядер самого гипоталамуса, а также гипофиза. Примером может служить тормозящее влияние дофамина на секрецию гормона пролактина.
Третий тип проекций отвечает за тормозящее влияние дофамина на различные биологически значимые потребности: пищевую, половую, оборонительную. Параллельно могут возникать положительные эмоциональные переживания (действие на центр положительного подкрепления гипоталамуса).
 | |
| Рис. 3.31. Схема эффектов дофаминергической системы в норме и патологии |
Несмотря на многообразие эффектов (рис. 3.31), наиболее очевидной задачей дофаминергической системы является регуляция двигательных функций. Управление возможно на уровне коры (ассоциативной и моторной), базальных ганглиев, субталамуса. В продолговатом мозге одна из врожденных моторных реакций — рвотный рефлекс также находится под контролем этой медиаторной системы. Эмоции, возникающие при активации дофаминергических синапсов, часто связаны с движениями: удовольствие, получаемое от танца и выполнения сложного спортивного упражнения, чувство гибкости и легкости, радость от снятия усталости.
Синтез дофамина протекает так же, как и норадреналина, но в дофаминергических нейронах цепочка химических превращений тирозина останавливается на одно звено раньше. Далее происходит перенос медиатора в везикулы и выброс в синаптическую щель по мере надобности.
В настоящее время обнаружено пять типов рецепторов к дофамину; все они являются метаботропными и связаны с аденилатциклазой. Наиболее распространены и важны первый и второй типы, названные соответственно D1-рецепторы и D2-peцепторы.
D1-рецепторы составляют около 3/4 всех дофаминовых рецепторов, их действие реализуется через активацию аденилатциклазы и рост синтеза цАМФ. У человека больше всего D1-рецепторов в полосатом теле; много их в бледном шаре, миндалине, новой коре, гиппокампе. D1-рецепторы примерно в 10 раз чувствительнее к дофамину, чем D2-рецепторы. Вместе с тем их блокада нейролептиками наступает при использовании доз в 100—1000 раз больших, чем в случае D2-рецепторов.
D2-рецепторы составляют около 1/5 всех дофаминовых рецепторов. Их влияние реализуется через торможение аденилатциклазы и снижение синтеза цАМФ. Больше всего D2-рецепторов также в полосатом теле; далее следуют бледный шар, миндалина, гиппокамп, таламус и новая кора. Несмотря на меньшее количество, роль D2-рецепторов в ЦНС очень важна. Именно через них реализуется влияние большинства нейролептиков. Описано взаимодействие D1- и D2-рецепторов: стимуляция первых усиливает последствия специфической активации вторых.
Агонисты дофаминовых рецепторов не всегда проявляют специфичность по отношению к D1 и D2-типам. Таков апоморфин, используемый как препарат, вызывающий рвоту и применяемый при пищевом отравлении (когда промывание желудка провести невозможно), а также для выработки условно-рефлекторной отрицательной реакции на алкоголь (при лечении алкоголизма).
Избирательный агонист D2-рецепторов бромокриптин (синоним — парлодел) применяется для подавления послеродовой лактации. Предложен он и для использования при паркинсонизме, а также для ослабления двигательных нарушений, вызываемых нейролептиками.
Первым нейролептиком стал аминазин (иначе — хлорпромазин), открытый в начале 50-х годов. Применение нейролептиков позволяет контролировать самые сложные типы психопатологии — психозы, часто сопряженные с опасностью больного для окружающих и самого себя (сильное возбуждение, в том числе маниакальное; агрессия, страхи, расстройства сознания), поэтому второе название нейролептиков — антипсихотические препараты.
Аминазин и сходные с ним соединения относятся к химической группе фенотиазинов и являются антагонистами дофаминергических и центральных норадренергических рецепторов. В связи с этим, кроме ослабления психотических проявлений, они вызывают также характерное снижение общего уровня активности ЦНС: введение аминазина вызывает уменьшение двигательной активности, эмоциональную тупость (индифферентность), запоздалые реакции на внешние стимулы, однако не наблюдается помрачения сознания и нарушения мышления. Большие дозы фенотиазинов создают фон для развития дремотного состояния, они способны вызвать депрессию и двигательные расстройства, сходные с проявлениями паркинсонизма.
Следующим шагом в поисках более избирательных нейролептиков стало открытие бутирофенонов, представителем которых является галоперидол — специфический антагонист D2-рецепторов. Его избирательность позволяет эффективно блокировать маниакальные состояния и острый бред, не вызывая у больных состояния вялости и апатии. Вместе с тем могут проявляться сходные с паркинсоническими двигательные расстройства, что требует соответствующей фармакологической коррекции (например, с помощью циклодола).
Существуют и другие группы нейролептиков, обладающие более «мягким» действием. Выбор конкретного препарата зависит от тяжести патологии, ее остроты, необходимости хронического или периодического применения, индивидуальной переносимости.
С данными о преимущественно дофаминергической природе активности нейролептиков перекликаются и представления о важной роли данной медиаторной системы в развитии шизофрении: посмертный анализ мозга больных показывает значительное увеличение связывания антагонистов дофамина в различных структурах переднего мозга, что обусловлено повышением плотности дофаминовых рецепторов D2 и D4. Следовательно, происходящие при шизофрении изменения, не затрагивая процессы синтеза и выброса дофамина, значительно (избыточно) повышают чувствительность к нему постсинаптической мембраны.
Особую группу психотропных препаратов составляют вещества, стимулирующие выброс дофамина из пресинаптического окончания, в связи с чем уровень возбуждения ЦНС усиливается, уменьшается чувство утомления и потребность в сне, улучшается настроение, ощущается прилив сил. Все это позволило отнести препараты данной группы к психомоторным стимуляторам. Их наиболее известным представителем является фенамин (сульфат амфетамина). Амфетамины усиливают выброс не только дофамина, но и норадреналина, а также ослабляют их обратный захват.
Войдя в медицинскую практику в начале века, амфетамины использовались для лечения ожирения (как средства, снижающие аппетит) и нарколепсии (болезни, при которой человек неконтролируемо засыпает). Во время Второй мировой войны они широко применялись как стимуляторы. Сейчас амфетамины используются в медицине редко, поскольку формирование привыкания и зависимости возникает примерно через 2 месяца. Кроме того, по механизму действия они не устраняют необходимости в отдыхе, а лишь позволяют использовать резервные силы организма, что быстро ведет к физическому и психическому истощению. Наконец, существует значительное количество побочных эффектов на уровне сердечно-сосудистой и эндокринной систем.
Более мягким действием по сравнению с амфетаминами обладает психомоторный стимулятор сиднокарб, усиливающий деятельность в основном норадренергических структур ЦНС; его используют при астенических состояниях, абстинентных синдромах, задержках умственного развития у детей, после травм и инфекций головного мозга. В настоящее время он практически полностью заменил фенамин.
Амфетамины же из разряда лекарств перешли в последние десятилетия в разряд допингов и наркотических препаратов. Первый всплеск употребления амфетаминов пришелся на 50-е (Япония, Швеция) и 60-е (США) годы. Употребление амфетаминов сначала вызывает ощущение физического благополучия, уверенности в себе; по мере привыкания человек вынужден увеличивать и учащать приемы препарата, переходить от таблеток к инъекциям, затем наблюдаются психотические проявления (рост агрессивности, ощущение постоянной угрозы извне), все более усиливается абстинентный синдром (синдром отмены). В случае отказа от приема длительность только острого периода абстинентного синдрома может составлять 2—3 месяца, часто происходит переход к «тяжелым» наркотикам — морфину и героину.
Отдельной группой наркотических препаратов являются метиловые амфетамины («экстази» и др.), по механизмам действия более близкие к галлюциногенам (см. следующую главу).
Кокаин — алкалоид, содержащийся в листьях южноамериканского кустарника Erythroxylon coca. Его ярко выраженное влияние на нервную систему включает два компонента — местноанестезирующий и центральный. Как местный анастетик, кокаин применяется в практике отоларингологов при небольших операциях, не получая широкого распространения из-за высокой токсичности. Используется он и при операциях на роговице.
В ЦНС кокаин функционирует как блокатор обратного захвата дофамина, в результате чего его эффекты оказываются сходными с эффектами амфетаминов. Еще в конце XIX века в аптеках свободно продавались стимулирующие вина и тоники из коки, однако в начале XX века за распространением кокаина был установлен строгий контроль. Причиной этого стали многочисленные случаи развития кокаиновой зависимости. В 70-е годы на наркотическом рынке появился сравнительно дешевый кокаин, производимый в Колумбии и ряде других стран. Кроме того, была изобретена особо активная форма кокаина, предназначенная для курения, — «крэк». Все это привело к тому, что сегодня кокаин превратился в один из самых опасных и распространенных наркотиков.
Попадая в организм через дыхательные пути, кокаин вызывает очень сильные и приятные ощущения, имеющие, однако, небольшую длительность, т. е. по сравнению с амфетаминами он действует сильнее, но более короткое время. Влияние малых доз кокаина и амфетаминов сходно еще в большей степени. В случае кокаина гораздо выше опасность передозировки; более выражен психологический компонент зависимости; менее ярок — физиологический. Амфетамины, как и кокаин, истощают пресинаптические запасы дофамина: первые — усиливая выброс медиатора; второй — не давая ему возвращаться в везикулы. В последнем случае значительная часть дофамина распадается прямо в синаптической щели.
 | |
| Рис. 3.32. Схема регуляции деятельности дофаминергического синапса: 1 — везикулы с дофамином; 2 — постсинаптический рецептор; 3 — белок-насос, осуществляющий обратное всасывание дофамина; 4 — пресинаптический рецептор |
В норме инактивация дофамина (рис. 3.32) осуществляется тем же способом, который описан для норадреналина (обратный захват, а затем повторная загрузка в везикулы либо разложение с помощью МАО). Отличие состоит в функции пресинаптических рецепторов. В случае дофамина их включение тормозит активность синапса, т. е. уменьшает дальнейший выброс медиатора. Этот механизм позволяет нервным клеткам экономно расходовать запасы дофамина, но подразумевается, что чувствительность пре- и постсинаптических рецепторов к дофамину тонко сбалансирована. Смещение этого баланса, вероятно, является причиной некоторых видов шизофрении, при которых пресинаптические рецепторы «опаздывают» с торможением выброса медиатора, поэтому оказывается полезным введение специфических агонистов пресинаптических рецепторов (например, апоморфина в малых дозах). С другой стороны, блокада пресинаптических рецепторов галоперидолом может увеличивать активность дофаминергической передачи (особенно если на постсинаптической мембране находится минимальное количество D2-рецепторов).
Серотонин
Серотонин — медиатор, относящийся к группе моноаминов, к ней же принадлежат катехоламины и гистамин (см. главу 3.12). Образуется серотонин в результате химического преобразования аминокислоты триптофана.
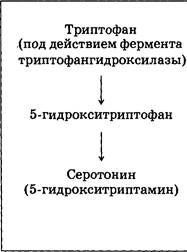 |  |
Триптофан является незаменимой пищевой кислотой, причем в растительных продуктах количество его незначительно; больше всего этого соединения в молочных продуктах. Ключевая стадия превращения триптофана в серотонин катализируется специальным ферментом триптофангидроксилазой.
Являясь медиатором ЦНС, серотонин одновременно выполняет важные функции в периферических органах: он работает как тканевой гормон, чья важнейшая функция — повышение тонуса гладкой мускулатуры. Наиболее известно сосудосуживающее действие серотонина: оно сопровождается повышением проницаемости капилляров, что может приводить к развитию отеков; сосудосуживающие эффекты серотонина, развивающиеся в мягкой мозговой оболочке, способны вызвать спазм артерий и развитие мигрени. Серотонин усиливает моторику желудочно-кишечного тракта, тонус матки, бронхов.
Много серотонина содержат тромбоциты — клетки крови, отвечающие за ее свертывание при повреждении сосуда. Выбрасываемый из тромбоцитов серотонин вызывает сужение сосуда в месте разрыва и способствует остановке кровотечения; ускоряет слипание тромбоцитов и формирование тромба; участвует в развитии воспалительного ответа на повреждение тканей и клеток.
В ЦНС серотонин синтезируют в основном нейроны, находящиеся в ядрах шва; последние расположены вдоль средней линии продолговатого мозга, моста и среднего мозга (рис. 3.33).
Большая часть аксонов из клеток направляется вперед к промежуточному и конечному мозгу, при этом особенно выделяются следующие пути: к полосатому телу, лобной, теменной и затылочной коре, поясной извилине; к миндалине, древней коре и гиппокампу; к медиальной зоне таламуса и ядрам гипоталамуса; к черной субстанции, четверохолмию и центральному серому веществу среднего мозга. Часть серотонинергических проекций заканчивается в спинном мозге.
Приведенный список структур ЦНС настолько велик, что позволяет предположить влияние серотонина практически на все существенно важные стороны деятельности мозга. Действительно, по имеющимся данным, серотонин участвует в управлении уровнем бодрствования, работе сенсорных систем, связан с обучением и эмоционально-мотивационной сферой. Одновременно происходит сложное взаимодействие с эффектами катехоламинов. Так, в рамках системы сон — бодрствование серотонин конкурирует с дофамином и норадреналином, вызывая снижение уровня возбуждения ЦНС. Ядра шва и связанное с ними центральное серое вещество рассматриваются как важнейшие центры сна, включение которых ведет в конечном итоге к общему торможению ЦНС.
| Рис. 3.33. Схема распределения в головном мозге нейронов, вырабатывающих в качестве медиатора серотонин: 1 — ядра шва; 2 — распределение аксонов ядер шва по структурам головного мозга; 3 — проекции в спинной мозг |  |
В случае сенсорных систем также наблюдается в основном тормозящее действие серотонинергических проекций. Известно анальгетическое (обезболивающее) влияние стимуляции ядер шва, дополняющее аналогичные эффекты норадреналина. При этом в задних рогах спинного мозга наблюдается активация тормозных интернейронов, в результате чего и осуществляется регуляция передачи болевой чувствительности. В корковых сенсорных зонах описаны серотонинергические проекции к нейронам, непосредственно проводящим зрительные, тактильные и прочие сигналы. Функция этих проекций состоит в предотвращении избыточного распространения сенсорного возбуждения по нейронным сетям («фокусировка» сигналов). Блокада этого механизма может сильно исказить процессы восприятия, вызвать сенсорные иллюзии и галлюцинации (см. ниже об эффектах ЛСД). Сходное действие серотонин оказывает и на ассоциативные зоны коры, делая процессы мышления более «организованными» (рис. 3.34). Каналы передачи информации (КПИ) коры взаимодействуют друг с другом при помощи коллатералей аксонов (прерывистые линии), оказывая взаимное возбуждающее влияние, которое является необходимым условием для нормального течения ассоциативных процессов. Аксоны клеток ядер шва контролируют эти влияния, удерживая нейронные сети коры в оптимальном для обработки информации состоянии. Область тормозных эффектов серотонинергических проекций на рис. 3.34 затемнена.
| Рис. 3.34. Схема тормозящего действия серотонина на передачу информации в нейронных сетя
Подборка статей по вашей теме:
|
 2015-10-22
2015-10-22 39052
39052
